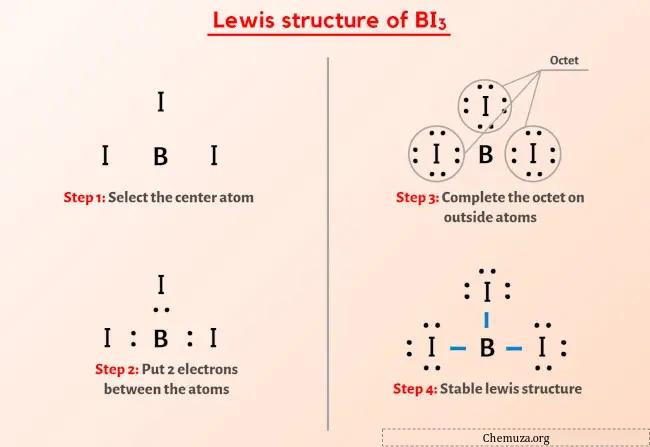
Sie haben das Bild oben also schon gesehen, oder?
Lassen Sie mich das obige Bild kurz erläutern.
Die BI3-Lewis-Struktur hat ein Boratom (B) im Zentrum, das von drei Jodatomen (I) umgeben ist. Zwischen dem Boratom (B) und jedem Jodatom (I) bestehen 3 Einfachbindungen.
Wenn Sie aus dem obigen Bild der Lewis-Struktur von BI3 nichts verstanden haben, dann bleiben Sie bei mir und Sie erhalten eine detaillierte Schritt-für-Schritt-Erklärung zum Zeichnen einer Lewis-Struktur von BI3 .
Fahren wir also mit den Schritten zum Zeichnen der Lewis-Struktur von BI3 fort.
Schritte zum Zeichnen der BI3-Lewis-Struktur
Schritt 1: Ermitteln Sie die Gesamtzahl der Valenzelektronen im BI3-Molekül
Um die Gesamtzahl der Valenzelektronen in einem BI3- Molekül zu ermitteln, müssen Sie zunächst die im Boratom und im Jodatom vorhandenen Valenzelektronen kennen.
(Valenzelektronen sind die Elektronen, die sich in der äußersten Umlaufbahn eines Atoms befinden.)
Hier erkläre ich Ihnen, wie Sie mithilfe eines Periodensystems ganz einfach die Valenzelektronen von Bor und Jod finden.
Gesamtvalenzelektronen im BI3-Molekül
→ Vom Boratom gegebene Valenzelektronen:
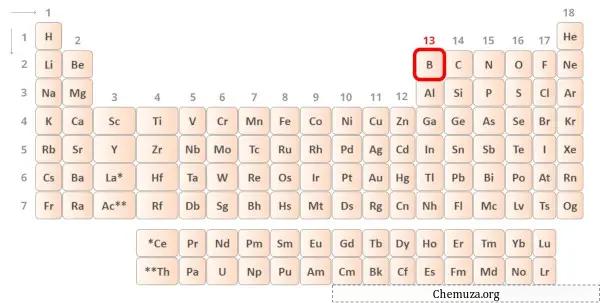
Bor ist ein Element der 13. Gruppe des Periodensystems. [1] Daher sind im Bor 3 Valenzelektronen vorhanden.

Sie können die drei im Boratom vorhandenen Valenzelektronen sehen, wie im Bild oben gezeigt.
→ Vom Jodatom gegebene Valenzelektronen:
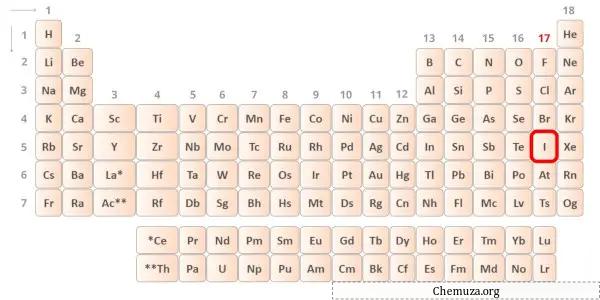
Jod ist ein Element der Gruppe 17 des Periodensystems. [2] Daher sind in Jod 7 Valenzelektronen vorhanden.
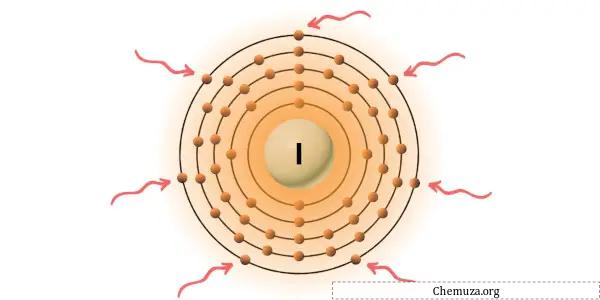
Sie können die 7 Valenzelektronen im Jodatom sehen, wie im Bild oben gezeigt.
Also,
Gesamte Valenzelektronen im BI3-Molekül = von 1 Boratom gespendete Valenzelektronen + von 3 Jodatomen gespendete Valenzelektronen = 3 + 7(3) = 24 .
Schritt 2: Wählen Sie das Zentralatom aus
Um das Zentralatom auszuwählen, müssen wir bedenken, dass das am wenigsten elektronegative Atom im Zentrum verbleibt.
Hier ist das gegebene Molekül BI3 und es enthält Bor- (B) und Jod- (I) Atome.
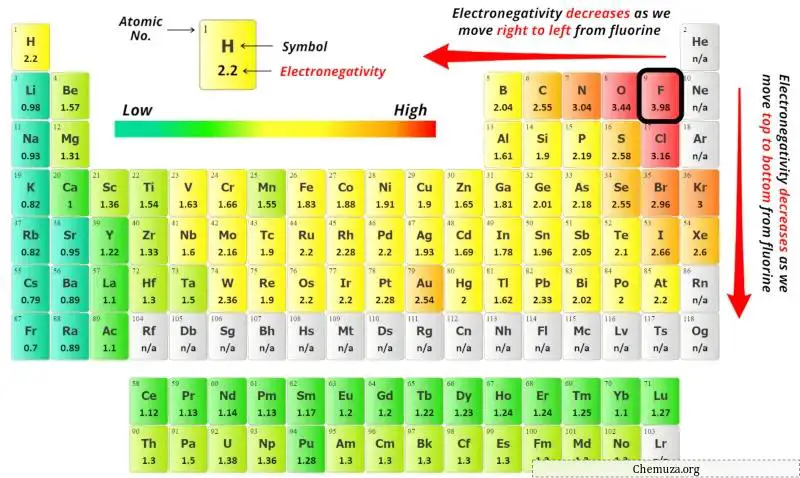
Sie können die Elektronegativitätswerte des Boratoms (B) und des Jodatoms (I) im obigen Periodensystem sehen.
Wenn wir die Elektronegativitätswerte von Bor (B) und Jod (I) vergleichen, ist das Boratom weniger elektronegativ .
Dabei ist das Boratom (B) das Zentralatom und die Jodatome (I) die Außenatome.
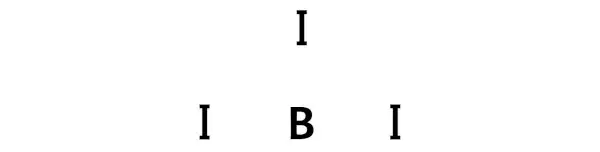
Schritt 3: Verbinden Sie jedes Atom, indem Sie ein Elektronenpaar zwischen ihnen platzieren
Jetzt müssen Sie im BI3-Molekül die Elektronenpaare zwischen dem Boratom (B) und den Jodatomen (I) platzieren.
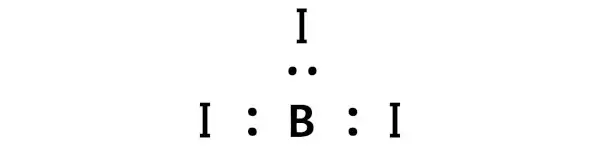
Dies weist darauf hin, dass Bor (B) und Jod (I) in einem BI3-Molekül chemisch aneinander gebunden sind.
Schritt 4: Machen Sie die externen Atome stabil
In diesem Schritt müssen Sie die Stabilität der externen Atome überprüfen.
Hier in der Skizze des BI3-Moleküls sieht man, dass die äußeren Atome Jodatome sind.
Diese externen Jodatome bilden ein Oktett und sind daher stabil.
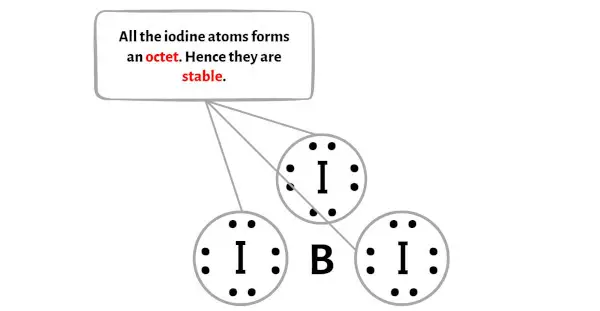
Zusätzlich haben wir in Schritt 1 die Gesamtzahl der im BI3-Molekül vorhandenen Valenzelektronen berechnet.
Das BI3-Molekül verfügt über insgesamt 24 Valenzelektronen und alle diese Valenzelektronen werden im obigen Diagramm von BI3 verwendet.
Es gibt daher keine Elektronenpaare mehr, die am Zentralatom festgehalten werden könnten.
Kommen wir nun zum nächsten Schritt.
Schritt 5: Überprüfen Sie die Stabilität der Lewis-Struktur
Jetzt sind Sie beim letzten Schritt angelangt, in dem Sie die Stabilität der Lewis-Struktur von BI3 überprüfen müssen.
Die Stabilität der Lewis-Struktur kann mithilfe eines formalen Ladungskonzepts überprüft werden.
Kurz gesagt, wir müssen nun die formale Ladung der Boratome (B) sowie der Jodatome (I) im BI3-Molekül ermitteln.
Um die formelle Steuer zu berechnen, müssen Sie die folgende Formel verwenden:
Formale Ladung = Valenzelektronen – (bindende Elektronen)/2 – nichtbindende Elektronen
Im Bild unten können Sie die Anzahl der bindenden und nichtbindenden Elektronen für jedes Atom des BI3-Moleküls sehen.
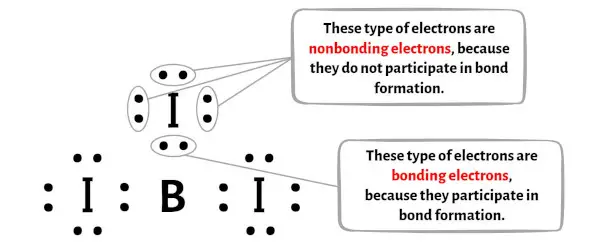
Für das Boratom (B):
Valenzelektronen = 3 (da Bor in Gruppe 13 ist)
Bindungselektronen = 6
Nichtbindende Elektronen = 0
Für das Jod(I)-Atom:
Valenzelektron = 7 (da Jod in Gruppe 17 ist)
Bindungselektronen = 2
Nichtbindende Elektronen = 6
| Formelle Anklage | = | Valenzelektronen | – | (Bindungselektronen)/2 | – | Nichtbindende Elektronen | ||
| B | = | 3 | – | 6/2 | – | 0 | = | 0 |
| ICH | = | 7 | – | 2/2 | – | 6 | = | 0 |
Aus den obigen Berechnungen der formalen Ladung können Sie erkennen, dass sowohl das Boratom (B) als auch das Jodatom (I) eine formale Ladung von „Null“ haben.
Dies weist darauf hin, dass die obige Lewis-Struktur von BI3 stabil ist und es keine weitere Änderung in der obigen Struktur von BI3 gibt.
In der obigen Lewis-Punkt-Struktur von BI3 können Sie jedes Bindungselektronenpaar (:) auch als Einfachbindung (|) darstellen. Dies führt zu der folgenden Lewis-Struktur von BI3.
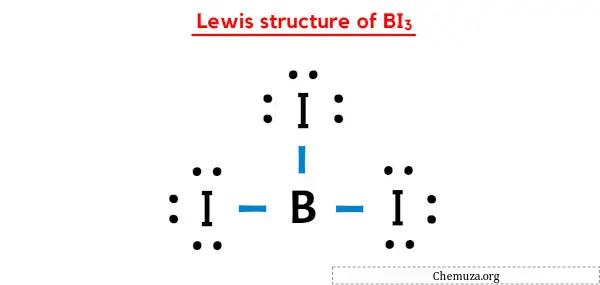
Ich hoffe, Sie haben alle oben genannten Schritte vollständig verstanden.
Für mehr Übung und ein besseres Verständnis können Sie andere unten aufgeführte Lewis-Strukturen ausprobieren.
Probieren Sie zum besseren Verständnis diese Lewis-Strukturen aus (oder sehen Sie sie sich zumindest an):
