Benzoylchlorid ist eine chemische Verbindung, die in verschiedenen Industrien verwendet wird. Es reagiert mit anderen Substanzen und bildet Derivate wie Benzoylperoxid, einen häufigen Bestandteil bei Aknebehandlungen.
| IUPAC-Name | Benzoylchlorid |
| Molekularformel | C7H5ClO |
| CAS-Nummer | 98-88-4 |
| Synonyme | Benzoesäure, Chlorid, Benzolcarbonylchlorid, Phenylcarbonylchlorid |
| InChI | InChI=1S/C7H5ClO/c8-6-7(9)4-2-1-3-5-7/h1-5H |
Eigenschaften von Benzoylchlorid
Benzoylchlorid-Formel
Die Formel für Benzoylchlorid lautet C7H5ClO. Es stellt die Anordnung der Kohlenstoff-, Wasserstoff-, Chlor- und Sauerstoffatome in der Verbindung dar. Die Formel liefert wertvolle Informationen über die elementare Zusammensetzung und strukturelle Zusammensetzung von Benzoylchlorid.
Molmasse von Benzoylchlorid
Die Molmasse von Benzoylchlorid wird durch Addition der Atommassen seiner Bestandteile berechnet. Dabei hat Kohlenstoff eine Molmasse von 12,01 g/mol, Wasserstoff eine Molmasse von 1,01 g/mol, Chlor eine Molmasse von 35,45 g/mol und Sauerstoff eine Molmasse von 16,00 g/mol. Addiert man diese Werte, ergibt sich eine Molmasse von Benzoylchlorid von etwa 140,57 g/mol.
Siedepunkt von Benzoylchlorid
Benzoylchlorid hat einen Siedepunkt von etwa 197–198 °C. Dies ist die Temperatur, bei der die flüssige Verbindung unter normalem Atmosphärendruck in den gasförmigen Zustand übergeht. Der Siedepunkt gibt Einblick in die Flüchtigkeits- und Verdampfungseigenschaften von Benzoylchlorid.
Schmelzpunkt von Benzoylchlorid
Der Schmelzpunkt von Benzoylchlorid liegt bei etwa -1°C. Damit ist die Temperatur gemeint, bei der die feste Form von Benzoylchlorid in den flüssigen Zustand übergeht. Der Schmelzpunkt gibt die physikalischen Eigenschaften der Verbindung und ihre Fähigkeit an, von einer Phase in eine andere überzugehen.
Dichte von Benzoylchlorid g/ml
Benzoylchlorid hat eine Dichte von etwa 1,21 g/ml. Unter Dichte versteht man die Masse eines Stoffes pro Volumeneinheit. Diese Eigenschaft gibt Auskunft über die Kompaktheit oder Konzentration von Benzoylchlorid in einem bestimmten Volumen.
Molekulargewicht von Benzoylchlorid
Das Molekulargewicht von Benzoylchlorid wird durch Addition der Atomgewichte aller Atome in einem Molekül berechnet. In diesem Fall beträgt das Molekulargewicht von Benzoylchlorid etwa 140,57 g/mol. Es ist ein wesentlicher Parameter, der bei stöchiometrischen Berechnungen und zur Bestimmung der Menge an Benzoylchlorid in chemischen Reaktionen verwendet wird.
Struktur von Benzoylchlorid
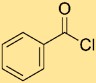
Die Struktur von Benzoylchlorid besteht aus einem Benzolring, der an eine Carbonylgruppe (-C=O) gebunden ist, und einem Chloratom (-Cl), das direkt an das Kohlenstoffatom der Carbonylgruppe gebunden ist. Diese Anordnung kann durch PhCOCl dargestellt werden, wobei „Ph“ den Benzolring darstellt. Die Struktur verdeutlicht die Konnektivität und Bindung von Atomen in Benzoylchlorid.
Löslichkeit von Benzoylchlorid
Benzoylchlorid ist in Wasser schlecht löslich. Es weist eine höhere Löslichkeit in organischen Lösungsmitteln wie Aceton, Ether und Benzol auf. Die Löslichkeitseigenschaften von Benzoylchlorid beeinflussen seine Anwendungen und Wechselwirkungen mit anderen Substanzen in verschiedenen chemischen Prozessen.
| Aussehen | Farblose bis hellgelbe Flüssigkeit |
| Spezifisches Gewicht | 1,21 g/ml |
| Farbe | Farblos bis hellgelb |
| Geruch | Reizender und stechender Geruch |
| Molmasse | 140,57 g/Mol |
| Dichte | 1,21 g/ml |
| Fusionspunkt | -1°C |
| Siedepunkt | 197-198°C |
| Blitzpunkt | 77°C |
| Löslichkeit in Wasser | Reagiert |
| Löslichkeit | Löslich in organischen Lösungsmitteln wie Aceton, Ether und Benzol |
| Dampfdruck | 4,95 mmHg bei 25°C |
| Wasserdampfdichte | 5.3 |
| pKa | 4.18 |
| pH-Wert | Nicht anwendbar (sauer beim Auflösen in Wasser) |
Sicherheit und Gefahren von Benzoylchlorid
Benzoylchlorid birgt einige Sicherheitsrisiken und sollte mit Vorsicht gehandhabt werden. Es reizt Haut, Augen und Atemwege stark und verursacht bei Kontakt Verbrennungen und starke Beschwerden. Das Einatmen der Dämpfe kann zu Reizungen der Atemwege und Lungenschäden führen. Bei der Arbeit mit Benzoylchlorid ist es wichtig, geeignete Schutzausrüstung wie Handschuhe, Schutzbrille und Atemschutzmaske zu tragen. Die Verbindung ist brennbar und kann sich bei Einwirkung von Hitze oder Flammen entzünden und giftige Dämpfe freisetzen. Darüber hinaus reagiert es heftig mit Wasser, Alkoholen und Basen, was zu Bränden oder Explosionen führen kann. Um Risiken zu minimieren, sollten ordnungsgemäße Lagerungs-, Handhabungs- und Entsorgungsverfahren befolgt werden.
| Gefahrensymbole | Ätzend, giftig |
| Sicherheitsbeschreibung | Kontakt mit Haut und Augen vermeiden. In einem gut belüfteten Bereich verwenden. Mit geeigneter Schutzausrüstung handhaben. |
| UN-Identifikationsnummern | Ein 1736 |
| HS-Code | 2916.31.00 |
| Gefahrenklasse | 8 (ätzend), 6,1 (giftig) |
| Verpackungsgruppe | II (Mittelstufe) |
| Toxizität | Sehr giftig und ätzend. |
Methoden zur Synthese von Benzoylchlorid
Es gibt verschiedene Methoden zur Synthese von Benzoylchlorid. Ein üblicher Ansatz besteht darin, Benzaldehyd mit einem geeigneten Oxidationsmittel wie Chlorgas oder Phosphorpentachlorid (PCl5) zu oxidieren. Bei dieser Methode mischt man unter kontrollierten Bedingungen Benzaldehyd mit dem Oxidationsmittel und es entsteht Benzoylchlorid.
Eine andere Methode beinhaltet die Reaktion zwischen Benzoylperoxid und Chlorwasserstoffgas . Benzoylperoxid wirkt als Radikalinitiator und fördert die Reaktion mit Chlorwasserstoff zu Benzoylchlorid.
Zur Herstellung von Benzoylchlorid kann Benzoesäure unter Rückflussbedingungen mit Thionylchlorid (SOCl2) oder Phosphortrichlorid (PCl3) behandelt werden. Bei der Reaktion entsteht als Zwischenprodukt ein Säurechlorid, das sich dann in Benzoylchlorid umwandelt.
Darüber hinaus kann die Reaktion von Benzoyltrichlorid mit Kohlenmonoxid (CO) in Gegenwart eines Katalysators wie Kupfer auch zur Synthese von Benzoylchlorid führen.
Es ist wichtig zu beachten, dass diese Methoden in einem gut belüfteten Bereich und unter Einhaltung angemessener Sicherheitsvorkehrungen durchgeführt werden sollten, da Benzoylchlorid eine gefährliche Verbindung ist. Um einen sicheren Syntheseprozess zu gewährleisten, sind eine sorgfältige Handhabung und die Einhaltung geeigneter Laborprotokolle erforderlich.
Verwendung von Benzoylchlorid
Benzoylchlorid findet aufgrund seiner vielseitigen chemischen Eigenschaften vielfältige Verwendungsmöglichkeiten in verschiedenen Branchen. Hier sind einige bemerkenswerte Apps:
- Pharmazeutische Industrie: Die pharmazeutische Industrie verwendet Benzoylchlorid als wichtiges Zwischenprodukt zur Synthese pharmazeutischer Verbindungen, einschließlich Analgetika, Antiseptika und Antihistaminika.
- Polymerindustrie: In der Polymerindustrie fungiert Benzoylchlorid als Monomer und trägt zur strukturellen Stabilität und thermischen Beständigkeit von Polymeren wie Polycarbonaten, Polyamiden und Polyestern bei.
- Organische Synthese: Benzoylchlorid dient als Reagens bei Acylierungsreaktionen und erleichtert die Einführung der Benzoylgruppe in organische Moleküle.
- Agrochemikalien: Benzoylchlorid spielt eine entscheidende Rolle im Pflanzenschutz und bei der Schädlingsbekämpfung, indem es zur Synthese von Herbiziden und Insektiziden beiträgt.
- Farbstoffherstellung: Benzoylchlorid ist ein Vorläufer für die Herstellung verschiedener Farbstoffe und Pigmente, die zum Färben von Textilien, Kunststoffen und Druckfarben unerlässlich sind.
- Parfümerie- und Parfümerieindustrie: Die Parfümerie- und Parfümerieindustrie verwendet Benzoylchlorid zur Synthese von Parfümen und Duftstoffverbindungen und verbessert dadurch deren aromatische Eigenschaften.
- Chemische Forschung: Forschungslabore verwenden Benzoylchlorid bei der Synthese neuer chemischer Verbindungen und tragen so zur Entwicklung innovativer Materialien und pharmazeutischer Produkte bei.
- Gummiindustrie: Die Gummiindustrie verwendet Benzoylchlorid als Vernetzungsmittel, um die Eigenschaften von Gummi zu modifizieren und dadurch seine Haltbarkeit und Festigkeit zu verbessern.
- Klebstoffherstellung: Hersteller verwenden Benzoylchlorid zur Herstellung von Klebstoffen und Dichtstoffen und verbessern so die Klebeeigenschaften.
- Textilindustrie: In der Textilindustrie fungiert Benzoylchlorid als Katalysator und Stabilisator bei der Herstellung synthetischer Fasern wie Nylon, Polyester und Elasthan und sichert deren Qualität und Leistung.
Diese verschiedenen Anwendungen zeigen die Bedeutung von Benzoylchlorid in verschiedenen Industriebereichen.
Fragen:
F: Welches der folgenden Reagenzien wandelt Benzoylchlorid in Phenylpropylketon um?
A: Das Reagenz, das Benzoylchlorid in Phenylpropylketon umwandelt, ist ein Grignard-Reagenz aus Phenylmagnesiumbromid (PhMgBr), gefolgt von einer Reaktion mit Propylhalogenid.
F: Welches Produkt würde bei der Reaktion von Benzoylchlorid mit 4-Chlorphenol entstehen?
A: Das Produkt, das bei der Reaktion von Benzoylchlorid mit 4-Chlorphenol entsteht, ist 4-Chlorbenzoylphenol.
F: Wie ermittelt man die Ausbeute der Ammonolyse von Benzoylchlorid?
A: Die Ausbeute der Ammonolyse von Benzoylchlorid kann bestimmt werden, indem die Menge des erhaltenen gewünschten Produkts durch die theoretische Ausbeute dividiert und mit 100 multipliziert wird, um sie als Prozentsatz auszudrücken.
F: Ist Benzoylchlorid oder Benzylchlorid elektrophiler?
A: Benzoylchlorid ist aufgrund der stark elektronenziehenden Carbonylgruppe elektrophiler als Benzylchlorid.
F: Welches der folgenden Reagenzien wird in der folgenden Reaktion verwendet? Benzoesäure zu Benzoylchlorid, Hydrolyse von Benzoylchlorid?
A: Das bei der Umwandlung von Benzoesäure in Benzoylchlorid verwendete Reagens ist Thionylchlorid (SOCl2) und für die Hydrolyse von Benzoylchlorid ist es Wasser oder eine wässrige Base.
F: Welche Produkte entstehen, wenn Benzoylchlorid mit Cyclohexanol reagiert?
A: Die bei der Reaktion von Benzoylchlorid mit Cyclohexanol entstehenden Produkte sind Cyclohexylbenzoat und Chlorwasserstoff (HCl).
F: Wie trocknet man Benzoylchlorid?
A: Benzoylchlorid kann durch Zugabe eines geeigneten Trocknungsmittels wie wasserfreiem Calciumchlorid oder wasserfreiem Magnesiumsulfat und anschließender Filtration getrocknet werden.
F: Was ist elektrophiler, Benzoylchlorid oder Benzylchlorid?
A: Benzoylchlorid ist aufgrund der Anwesenheit der Carbonylgruppe, die die Elektronendichte unterdrückt und die Elektrophilie erhöht, elektrophiler als Benzylchlorid.
F: Ist Benzoylchlorid wasserlöslich?
A: Nein, Benzoylchlorid ist nicht wasserlöslich. Es reagiert mit Wasser unter Bildung von Benzoesäure und Salzsäure.
