Benzoesäure ist ein farbloser kristalliner Feststoff, der als Lebensmittelkonservierungsmittel und als Vorstufe für viele andere organische Verbindungen verwendet wird. Es kann aus Toluol oder Benzol synthetisiert werden.
| IUPAC-Name | Benzoesäure |
| Molekularformel | C7H6O2 |
| CAS-Nummer | 65-85-0 |
| Synonyme | Carboxybenzol, Benzolameisensäure, Phenylameisensäure, Benzolcarbonsäure, E210 |
| InChI | InChI=1S/C7H6O2/c8-7(9)6-4-2-1-3-5-6/h1-5H,(H,8,9) |
Molmasse von Benzoesäure
Benzoesäure hat eine Molmasse von 122,12 g/mol. Es handelt sich um eine einfache organische Verbindung, die aus einem Benzolring besteht, der an eine funktionelle Carbonsäuregruppe gebunden ist. Die Molmasse wird berechnet, indem die Atommassen aller in einem einzelnen Molekül der Verbindung vorhandenen Atome addiert werden. Im Fall von Benzoesäure lautet die Formel C7H6O2, sodass die Molmasse wie folgt berechnet werden kann:
7(12,01) + 6(1,01) + 2(16,00) = 122,12 g/mol
Die Kenntnis der Molmasse ist wichtig, um die Menge an Benzoesäure zu bestimmen, die für chemische Reaktionen benötigt wird, und um andere Eigenschaften wie Konzentration und Dichte zu berechnen.
Struktur von Benzoesäure
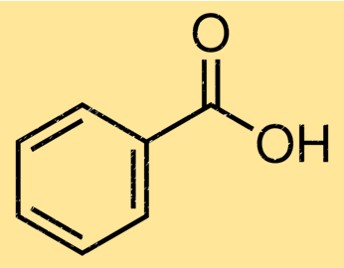
Die Struktur von Benzoesäure besteht aus einem Benzolring, der an eine funktionelle Carbonsäuregruppe gebunden ist. Der Benzolring ist ein sechsgliedriger Kohlenstoffring mit alternierenden Doppelbindungen, während die Carbonsäuregruppe aus einem Kohlenstoffatom besteht, das doppelt an ein Sauerstoffatom gebunden ist, und einer Einfachbindung an eine Hydroxylgruppe. Die Struktur der Benzoesäure ist wichtig für die Bestimmung ihrer chemischen und physikalischen Eigenschaften.
Benzoesäure-Formel
Die chemische Formel für Benzoesäure lautet C7H6O2. Diese Formel sagt uns, dass jedes Benzoesäuremolekül sieben Kohlenstoffatome, sechs Wasserstoffatome und zwei Sauerstoffatome enthält. Die Formel dient zur Bestimmung der Molmasse und des Molekulargewichts von Benzoesäure sowie des Verhältnisses der in der Verbindung vorhandenen Elemente.
Schmelzpunkt von Benzoesäure
Benzoesäure hat einen Schmelzpunkt von 122,4 °C. Dies ist die Temperatur, bei der die feste Form der Benzoesäure zu schmelzen und sich in eine Flüssigkeit umzuwandeln beginnt. Der Schmelzpunkt wird durch Faktoren wie Reinheit, Kristallstruktur und intermolekulare Kräfte beeinflusst. Benzoesäure hat aufgrund ihrer starken intermolekularen Kräfte, die durch Wasserstoffbrückenbindungen zwischen den Carbonsäuregruppen benachbarter Moleküle verursacht werden, einen relativ hohen Schmelzpunkt.
Siedepunkt von BzOH
Der Siedepunkt von BzOH beträgt 249°C. Dies ist die Temperatur, bei der die flüssige Form von BzOH zu verdampfen beginnt und sich in ein Gas verwandelt. Der Siedepunkt einer Substanz wird durch Faktoren wie intermolekulare Kräfte, Druck und das Vorhandensein von Verunreinigungen beeinflusst. BzOH hat aufgrund seiner starken intermolekularen Kräfte, die durch Wasserstoffbrückenbindungen zwischen den Carbonsäuregruppen benachbarter Moleküle verursacht werden, einen relativ hohen Siedepunkt.
BzOH-Dichte g/ml
Die Dichte von BzOH beträgt 1,265 g/ml. Dies ist die Masse eines Milliliters BzOH bei einer bestimmten Temperatur und einem bestimmten Druck. Die Dichte ist eine wichtige physikalische Eigenschaft zur Bestimmung der Masse einer Substanz in einem bestimmten Volumen. Die Dichte von BzOH wird durch Faktoren wie Temperatur und Druck beeinflusst.
Molekulargewicht BzOH
Das Molekulargewicht von BzOH beträgt 122,12 g/mol. Dies ist die Masse eines BzOH-Moleküls. Das Molekulargewicht wird verwendet, um die Anzahl der Moleküle in einer bestimmten Masse einer Substanz zu bestimmen. Sie wird durch Addition der Atommassen aller Atome im Molekül berechnet.
| Aussehen | Weiße Kristalle |
| Spezifisches Gewicht | 1.265 g/cm³ |
| Farbe | Farblos |
| Geruch | Schwach, angenehm |
| Molmasse | 122,12 g/Mol |
| Dichte | 1.265 g/cm³ |
| Fusionspunkt | 250°F |
| Siedepunkt | 249°C |
| Blitzpunkt | 121°C |
| Löslichkeit in Wasser | 3,8 g/L |
| Löslichkeit | Löslich in Ethanol, Ether, Benzol und Chloroform; leicht wasserlöslich |
| Dampfdruck | 0,00027 mmHg bei 25 °C |
| Wasserdampfdichte | 4,2 (Luft=1) |
| pKa | 4.2 |
| pH-Wert | 2,7 – 3,5 |
Sicherheit und Gefahren von Benzoesäure
Benzoesäure (BzOH) kann bei unsachgemäßer Handhabung gefährlich sein. Es ist haut- und augenreizend und kann bei Einatmen in hohen Konzentrationen Reizungen der Atemwege verursachen. Die Einnahme großer Mengen BzOH kann auch Übelkeit, Erbrechen und Bauchschmerzen verursachen. Die Verbindung ist brennbar und kann sich entzünden, wenn sie Hitze oder Flammen ausgesetzt wird. Es ist wichtig, mit BzOH vorsichtig umzugehen, geeignete Schutzausrüstung zu tragen und den Kontakt mit Haut, Augen und Schleimhäuten zu vermeiden. Im Falle einer versehentlichen Exposition sollten die betroffenen Bereiche mit Wasser gespült werden und gegebenenfalls ein Arzt aufgesucht werden. Um eine Kontamination der Umwelt zu vermeiden, müssen außerdem ordnungsgemäße Lagerungs- und Entsorgungsverfahren befolgt werden.
| Gefahrensymbole | XI |
| Sicherheitsbeschreibung | Kontakt mit Haut und Augen vermeiden; Schutzhandschuhe/Schutzbrille tragen; Bei Augenkontakt sofort mit reichlich Wasser spülen und einen Arzt konsultieren; An einem trockenen Ort, fern von Hitze und unverträglichen Materialien aufbewahren. Behälter dicht verschlossen halten. |
| AN-Kennungen | UN 3077 (ADR/RID), UN 1220 (IMDG), UN 3077 (ICAO) |
| HS-Code | 2916.31.00 |
| Gefahrenklasse | 9 (Verschiedene gefährliche Materialien und Gegenstände) |
| Verpackungsgruppe | III |
| Toxizität | Benzoesäure ist relativ ungiftig, mit einer oralen LD50 bei Ratten von 1700 bis 1940 mg/kg. Bei Einatmen hoher Konzentrationen kann es zu Haut- und Augenreizungen sowie Reizungen der Atemwege kommen. Auch die Einnahme größerer Mengen kann zu Magen-Darm-Beschwerden führen. |
Methoden zur Synthese von Benzoesäure
Benzoesäure (BzOH) kann auf verschiedene Weise synthetisiert werden.
Eine übliche Methode ist die Oxidation von Toluol oder Benzylchlorid mit Kaliumpermanganat oder Chromsäure. Eine andere Methode besteht darin, Benzol mit Kohlendioxid und einem Metallkatalysator wie Kupfer- oder Magnesiumoxid in Gegenwart von Hitze und Druck zur Reaktion zu bringen.
BzOH kann durch Hydrolyse von Benzamid, Benzoylchlorid oder Benzotrifluorid unter Verwendung einer starken Base wie Natriumhydroxid erhalten werden. Dieser Prozess ergibt BzOH und das entsprechende Amin oder Alkohol. Alternativ kann BzOH durch Reaktion von Benzylalkohol mit Kaliumpermanganat oder Natriumdichromat erhalten werden.
Zur Synthese von BzOH kann ein Grignard-Reagenz verwendet werden, das durch Reaktion von Magnesium und einem Alkyl- oder Arylhalogenid mit Kohlendioxid entsteht. Um die resultierende Carbonsäure in BzOH umzuwandeln, kann die Lösung angesäuert werden.
BzOH kann durch Oxidation von Toluol in Gegenwart eines Kobalt- oder Mangankatalysators hergestellt werden. Diese Methode eignet sich besonders für die Produktion in großem Maßstab.
Jede dieser Synthesemethoden hat je nach spezifischer Anwendung und Produktionsumfang Vor- und Nachteile. Es ist wichtig, die am besten geeignete Methode auf der Grundlage von Faktoren wie Kosten, Wirksamkeit und Umweltauswirkungen auszuwählen.
Verwendung von Benzoesäure
- Menschen verwenden häufig Benzoesäure (BzOH) als Lebensmittelkonservierungsmittel, da sie das Wachstum von Bakterien und Pilzen hemmen kann.
- Hersteller verwenden es als Zwischenprodukt bei der Synthese verschiedener Chemikalien, darunter Farbstoffe, Parfüme und Pharmazeutika.
- Hersteller verwenden BZOH bei der Herstellung von Weichmachern wie Benzylbenzoat, die bei der Herstellung von PVC und anderen Kunststoffen verwendet werden.
- Es spielt eine wesentliche Rolle bei der Herstellung von Phenol, das zur Herstellung von Harzen, Klebstoffen und Desinfektionsmitteln verwendet wird.
- Hersteller fügen Tierfutter BZOH hinzu, um das Wachstum von Schimmel und Bakterien zu verhindern.
- Es fungiert als Vorstufe von Benzoylperoxid, das zur Behandlung von Akne eingesetzt wird.
- Hersteller verwenden BZOH bei der Herstellung verschiedener Arten von Polymeren, darunter Polyester, Nylon und Polyurethan.
- Die Industrie nutzt es als Lösungsmittel für verschiedene organische Verbindungen, darunter Harze, Öle und Wachse.
- Hersteller verwenden BZOH bei der Herstellung verschiedener Arten von Salzen, wie z. B. Natriumbenzoat, die als Lebensmittelkonservierungsmittel und antimikrobielle Wirkstoffe verwendet werden.
- BZOH wird bei der Herstellung verschiedener Arten von Waschmitteln verwendet, darunter Waschmittel, Geschirrspülmittel und Reinigungsmittel.
Fragen:
F: Ist Benzoesäure wasserlöslich?
A: BzOH ist in Wasser schlecht löslich, mit einer Löslichkeit von 3,4 g/L bei 25 °C. Allerdings ist es in organischen Lösungsmitteln wie Ethanol und Aceton besser löslich.
F: Ist Benzoesäure eine starke Säure?
A: Nein, BzOH ist eine schwache Säure. In Wasser dissoziiert es teilweise unter Bildung von Hydroniumionen und Benzoationen. Seine Dissoziationskonstante (Ka) beträgt 6,5 x 10^-5, was auf seine schwach saure Natur hinweist.
F: Eine Lösung von 0,20 M Benzoesäure (C6H5COOH) hat einen pH-Wert von 2,45. Was ist Ka für Benzoesäure?
A: Der Ka von BzOH kann anhand des pH-Werts der Lösung und der Konzentration der Säure berechnet werden. Unter Verwendung des pH-Werts von 2,45 und der BzOH-Dissoziationsgleichung wird der Ka-Wert zu 6,5 x 10^-5 berechnet.
F: Ist Benzoesäure polar oder unpolar?
A: Benzoesäure ist ein polares Molekül, da die funktionelle Carbonsäuregruppe ein elektronegatives Sauerstoffatom enthält, das ein Dipolmoment erzeugt.
