Ethylbenzol (C8H10) ist eine organische Verbindung mit süßem Geruch. Es wird als Lösungsmittel in verschiedenen Industriezweigen verwendet, unter anderem in der Kunststoff- und Gummiindustrie. Es kommt auch in Benzin vor und wird in der Zusammensetzung bestimmter Haushaltsprodukte verwendet.
| IUPAC-Name | Ethylbenzol |
| Molekularformel | C8H10 |
| CAS-Nummer | 100-41-4 |
| Synonyme | Ethylbenzol, EB, Phenylethan, Ethylphenyl, 2-Phenylethan, Alpha-Methyltoluol, 1-Phenylethan, Ethylbenzol, Styrolverdünner |
| InChI | InChI=1S/C8H10/c1-2-8-6-4-3-5-7-8/h3-7H,2H2,1H3 |
Eigenschaften von Ethylbenzol
Ethylbenzol-Formel
Die Summenformel für Ethylbenzol lautet C8H10, was bedeutet, dass es aus acht Kohlenstoffatomen und zehn Wasserstoffatomen besteht. Die chemische Struktur von Ethylbenzol weist einen Benzolring auf, der an eine Ethylgruppe gebunden ist.
Molmasse von Ethylbenzol
Die Molmasse von C8H10 beträgt 106,17 g/mol. Dies wird berechnet, indem die Atommassen aller Atome in einem C8H10-Molekül addiert werden.
Siedepunkt von Ethylbenzol
Der Siedepunkt von C8H10 beträgt 136,2 °C (277,2 °F). Dies ist die Temperatur, bei der sich die flüssige Form von C8H10 in ein Gas verwandelt. C8H10 hat im Vergleich zu anderen aromatischen Kohlenwasserstoffen einen relativ niedrigen Siedepunkt, was es als Lösungsmittel in verschiedenen Industrien nützlich macht.
Schmelzpunkt von Ethylbenzol
Der Schmelzpunkt von C8H10 beträgt -95,2 °C (-139,4 °F). Dies ist die Temperatur, bei der die feste Form von C8H10 in eine Flüssigkeit übergeht. C8H10 hat im Vergleich zu anderen aromatischen Kohlenwasserstoffen einen relativ niedrigen Schmelzpunkt und eignet sich daher als Rohstoff für die Herstellung anderer Chemikalien.
Ethylbenzoldichte g/ml
Die Dichte von C8H10 beträgt 0,867 g/ml bei 20 °C (68 °F). Das bedeutet, dass ein Milliliter C8H10 bei dieser Temperatur 0,867 Gramm wiegt. C8H10 hat eine geringere Dichte als Wasser, was bedeutet, dass es auf der Wasseroberfläche schwimmt, wenn die beiden Flüssigkeiten gemischt werden.
Molekulargewicht von Ethylbenzol
Das Molekulargewicht von C8H10 beträgt 106,17 g/mol. Dies ist die Masse eines C8H10-Moleküls, die durch Addition der Atommassen aller Atome im Molekül berechnet werden kann.
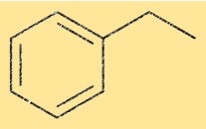
Struktur von Ethylbenzol
Die Struktur von C8H10 besteht aus einem Benzolring, der an eine Ethylgruppe gebunden ist. Die Ethylgruppe ist an eines der Kohlenstoffatome des Benzolrings gebunden. Diese Struktur wird auch als Phenylethan bezeichnet.
Löslichkeit von Ethylbenzol
C8H10 ist in Wasser unlöslich, aber in organischen Lösungsmitteln wie Alkoholen, Ethern und Chloroform löslich. Das bedeutet, dass sich C8H10 nicht in Wasser löst, wohl aber in anderen Flüssigkeiten mit ähnlichen chemischen Eigenschaften. Die Löslichkeit von C8H10 in verschiedenen Lösungsmitteln hängt von Faktoren wie Temperatur, Druck und chemischen Eigenschaften des Lösungsmittels ab.
| Aussehen | Farblose Flüssigkeit |
| Spezifisches Gewicht | 0,867 g/ml bei 20 °C |
| Farbe | Farblos |
| Geruch | Süßes Aroma |
| Molmasse | 106,17 g/Mol |
| Dichte | 0,867 g/ml bei 20 °C |
| Fusionspunkt | -95,2 °C (-139,4 °F) |
| Siedepunkt | 136,2 °C (277,2 °F) |
| Blitzpunkt | 11,1 °C (52 °F) |
| Löslichkeit in Wasser | 0,30 g/L bei 20°C |
| Löslichkeit | Löslich in organischen Lösungsmitteln wie Alkoholen, Ethern und Chloroform |
| Dampfdruck | 10,7 mmHg bei 20°C |
| Wasserdampfdichte | 3.7 |
| pKa | 10.17 |
| pH-Wert | Unzutreffend |
Sicherheit und Gefahren von Ethylbenzol
C8H10 kann gefährlich sein, wenn bei der Handhabung und Verwendung nicht die entsprechenden Vorsichtsmaßnahmen getroffen werden. Es wird als brennbare Flüssigkeit eingestuft und kann sich entzünden, wenn es Hitze oder Flammen ausgesetzt wird. C8H10 kann auch schädlich sein, wenn es eingeatmet oder eingenommen wird. Die Exposition gegenüber hohen Konzentrationen von C8H10 kann Schwindel, Kopfschmerzen und Reizungen der Atemwege verursachen. Eine langfristige Exposition gegenüber C8H10 wurde mit Leber- und Nierenschäden in Verbindung gebracht. Bei der Arbeit mit C8H10 sollten Sicherheitsvorkehrungen getroffen werden, z. B. das Tragen von Schutzkleidung und Handschuhen, das Arbeiten in gut belüfteten Bereichen und die Lagerung an einem sicheren, kühlen und trockenen Ort.
| Gefahrensymbole | Entzündlich, gesundheitsschädlich |
| Sicherheitsbeschreibung | Von Hitze, Funken, offenen Flammen und heißen Oberflächen fernhalten. Explosionsgeschützte Geräte verwenden. Einatmen von Staub/Rauch/Gas/Nebel/Dampf/Spray vermeiden. Nach der Handhabung gut waschen. |
| UN-Identifikationsnummern | UN 1175 |
| HS-Code | 2902.90.20 |
| Gefahrenklasse | 3 (Brennbare Flüssigkeiten) |
| Verpackungsgruppe | II (mittlere Gefahr) |
| Toxizität | Ethylbenzol gilt als mäßig giftiger Stoff. Bei längerer Exposition oder in hohen Konzentrationen kann es zu Augen- und Hautreizungen, Atemwegserkrankungen und Schädigungen des Nervensystems führen. |
Methoden zur Synthese von Ethylbenzol
Die am häufigsten verwendete Methode zur Synthese von C8H10 ist die katalytische Dehydrierung von Ethylcyclohexan. Bei diesem Verfahren wird eine Mischung aus Ethylcyclohexan und Wasserstoffgas über einem Katalysator bei hoher Temperatur erhitzt, wodurch sich die Wasserstoffatome von der Ethylgruppe trennen und C8H10 entsteht.
Eine weitere Methode zur Synthese von C8H10 beinhaltet die Alkylierung von Benzol mit Ethylengas . Diese Reaktion erfordert einen Katalysator, normalerweise Aluminiumchlorid, und führt zur Bildung von C8H10 und Chlorwasserstoff als Nebenprodukt.
Eine alternative Methode zur Herstellung von C8H10 beinhaltet die Reaktion von Benzol mit Ethylchlorid in Gegenwart eines Lewis-Säure-Katalysators, wie etwa Aluminiumchlorid. Bei diesem Prozess entstehen C8H10 und Chlorwasserstoff als Nebenprodukt.
Neben den genannten Methoden entwickeln Forscher auch neue Methoden zur Synthese von C8H10, beispielsweise die Verwendung ionischer Flüssigkeiten als Lösungsmittel für die Ethylenalkylierung von Benzol . Diese Methoden haben das Potenzial, Vorteile hinsichtlich Effizienz und Umweltverträglichkeit zu bieten. Ihre industrielle Nutzung ist jedoch noch nicht weit verbreitet.
Verwendung von Ethylbenzol
C8H10 hat mehrere wichtige Anwendungen in verschiedenen Branchen. Einige seiner Hauptanwendungen sind:
- Styrolproduktion: Die Produktion von Styrol, das zur Herstellung einer Vielzahl von Kunststoffen, Harzen und synthetischem Kautschuk verwendet wird und an C8H10 als wichtiges Zwischenprodukt gebunden ist.
- Lösungsmittel: Wird häufig als Lösungsmittel für verschiedene Anwendungen verwendet, darunter Tinten, Beschichtungen, Klebstoffe und Reinigungsmittel.
- Kraftstoffzusatz: Wird dem Benzin zugesetzt, um dessen Oktanzahl zu verbessern und so die Motorleistung zu verbessern.
- Chemisches Zwischenprodukt: Wird als Rohstoff für die Synthese anderer Chemikalien wie Phenylethanol und Diethylbenzol verwendet.
- Polymerproduktion: Wird zur Herstellung verschiedener Arten von Polymeren verwendet, beispielsweise Polystyrol und Acrylnitril-Butadien-Styrol-Harze (ABS).
- Landwirtschaft: Wird auch als Pestizid und Herbizid verwendet.
- Medizinische Anwendungen: Wird als Lokalanästhetikum sowie als Lösungsmittel für pharmazeutische Produkte verwendet.
Fragen:
F: Wie viele Signale würden Sie im 1H-NMR-Spektrum von Ethylbenzol erwarten?
A: Das 1H-NMR-Spektrum für C8H10 hätte vier Signale: zwei für die Protonen am Benzolring (die als Dublett erscheinen würden) und zwei für die Protonen an der Ethylgruppe (die als Triplett erscheinen würden).
F: Welche Anteile an Benzol und Ethylbenzol sollten gemischt werden?
A: Die zu mischenden Anteile von Benzol und C8H10 hängen von der gewünschten Konzentration von C8H10 in der Mischung ab. Das Benzol/C8H10-Verhältnis kann je nach Anwendung zwischen 10:1 und 1:1 variieren.
F: Was ist Ethylbenzolnitrierung?
A: Bei der Nitrierung von C8H10 erfolgt die Reaktion von C8H10 mit einer Mischung aus Salpetersäure und Schwefelsäure, was zur Einführung einer oder mehrerer Nitrogruppen am Benzolring von C8H10 führt. Diese Reaktion wird häufig bei der Herstellung von Industriechemikalien wie Nitrobenzol und Phenylethylaminen verwendet.
F: Ist Ethylbenzol polar?
A: C8H10 ist aufgrund der symmetrischen Struktur des Benzolrings eine unpolare Verbindung, die jegliche Polarität der Ethylgruppe zunichte macht. Daher weist C8H10 eine geringe Wasserlöslichkeit auf und ist im Allgemeinen in unpolaren Lösungsmitteln wie Hexan und Toluol löslich.
F: Wie wechselt man von Ethylbenzol zu Styrol?
A: C8H10 kann durch den Dehydrierungsprozess in Styrol umgewandelt werden, bei dem zwei Wasserstoffatome aus der Ethylgruppe mithilfe eines Katalysators wie Eisenoxid oder Chromoxid entfernt werden. Bei diesem Prozess entstehen als Nebenprodukt Styrol und Wasserstoffgas. Das resultierende Styrol kann dann gereinigt und zur Herstellung verschiedener Industriematerialien wie Kunststoffe, Harze und Synthesekautschuk verwendet werden.
