Tetrachlorethylen (C2Cl4) ist eine farblose, nicht brennbare Flüssigkeit, die üblicherweise in der chemischen Reinigung verwendet wird. Bei übermäßigem Verzehr oder Einatmen kann es zu gesundheitlichen Problemen wie Schwindel, Kopfschmerzen und Leberschäden kommen.
| IUPAC-Name | Tetrachlorethen |
| Molekularformel | C2Cl4 |
| CAS-Nummer | 127-18-4 |
| Synonyme | Perchlorethylen, PCE, Tetrachlorethen, Tetrachlorkohlenstoffdimer, 1,1,2,2-Tetrachlorethylen |
| InChI | InChI=1S/C2Cl4/c3-1(4)2(5)6 |
Eigenschaften von Tetrachlorethylen
Tetrachlorethylen-Formel
Tetrachlorethylen, auch Perchlorethylen oder PCE genannt, hat die chemische Formel C2Cl4. Das bedeutet, dass jedes Tetrachlorethylen-Molekül aus zwei Kohlenstoffatomen und vier Chloratomen besteht. Die Formel ist wichtig, weil sie uns hilft, die molekulare Struktur und die Eigenschaften von Tetrachlorethylen zu verstehen.
Tetrachlorethylen Molmasse
Die Molmasse von C2Cl4 beträgt 165,83 g/mol. Das bedeutet, dass ein Mol C2Cl4, was 6,022 x 10^23 Molekülen entspricht, 165,83 Gramm wiegt. Die Molmasse ist bei chemischen Berechnungen wichtig und kann dabei helfen, zu bestimmen, wie viel C2Cl4 für eine bestimmte Reaktion benötigt wird.
Siedepunkt von Tetrachlorethylen
Der Siedepunkt von C2Cl4 beträgt 121,1 °C (250 °F). Das bedeutet, dass sich C2Cl4 bei einer Temperatur von 121,1 °C von flüssig in gasförmig umwandelt. Der Siedepunkt ist eine wichtige Eigenschaft, da er das Verhalten von C2Cl4 in verschiedenen Umgebungen beeinflusst.
Schmelzpunkt von Tetrachlorethylen
Der Schmelzpunkt von C2Cl4 beträgt -22,94 °C (-9,31 °F). Das bedeutet, dass sich C2Cl4 bei einer Temperatur unter -22,94 °C von einem Feststoff in eine Flüssigkeit umwandelt. Der Schmelzpunkt ist wichtig für die Bestimmung des physikalischen Zustands von C2Cl4 bei verschiedenen Temperaturen.
Tetrachlorethylen-Dichte g/ml
Die Dichte von C2Cl4 beträgt bei Raumtemperatur 1,62 g/ml. Das bedeutet, dass C2Cl4 dichter ist als Wasser, das eine Dichte von 1 g/ml hat. Die Dichte ist wichtig für das Verständnis der physikalischen Eigenschaften von C2Cl4 und seines Verhaltens in verschiedenen Umgebungen.
Molekulargewicht von Tetrachlorethylen
Das Molekulargewicht von C2Cl4 beträgt 165,83 g/mol. Das bedeutet, dass das Gewicht eines C2Cl4-Moleküls 165,83 atomare Masseneinheiten beträgt. Das Molekulargewicht ist bei chemischen Berechnungen wichtig und kann dabei helfen, die Menge an C2Cl4 zu bestimmen, die für eine bestimmte Reaktion benötigt wird.
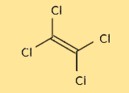
Struktur von Tetrachlorethylen
Die Struktur von C2Cl4 besteht aus zwei Kohlenstoffatomen und vier Chloratomen, die tetraedrisch angeordnet sind. Die Kohlenstoffatome sind durch eine Doppelbindung verbunden, während jedes Chloratom an eines der Kohlenstoffatome gebunden ist. Die Struktur ist wichtig für das Verständnis der chemischen und physikalischen Eigenschaften von C2Cl4.
Löslichkeit von Tetrachlorethylen
C2Cl4 ist in Wasser unlöslich, aber in organischen Lösungsmitteln wie Alkohol und Ether löslich. Das bedeutet, dass sich C2Cl4 nicht in Wasser löst, sich aber in anderen Stoffen lösen kann. Die Löslichkeit ist wichtig, um das Verhalten von C2Cl4 in verschiedenen Umgebungen zu verstehen, beispielsweise in industriellen Umgebungen oder im Labor.
| Aussehen | Farblose Flüssigkeit |
| Spezifisches Gewicht | 1,62 bei 20°C |
| Farbe | Farblos |
| Geruch | Süßer und ätherischer Geruch |
| Molmasse | 165,83 g/Mol |
| Dichte | 1,62 g/ml bei 20 °C |
| Fusionspunkt | -22,94°C |
| Siedepunkt | 121,1°C |
| Blitzpunkt | 55°C |
| Löslichkeit in Wasser | 0,015 g/100 ml bei 25 °C |
| Löslichkeit | Löslich in Alkohol und Ether |
| Dampfdruck | 10 mmHg bei 20°C |
| Wasserdampfdichte | 5.7 |
| pKa | 1.8 |
| pH-Wert | Nicht anwendbar (reine Substanz) |
Sicherheit und Gefahren von Tetrachlorethylen
C2Cl4 kann schädlich sein, wenn es eingeatmet oder eingenommen wird oder mit der Haut oder den Augen in Berührung kommt. Dies kann zu Schwindel, Kopfschmerzen, Verwirrtheit und Reizungen der Atemwege führen. Eine langfristige Exposition kann zu Leber- und Nierenschäden führen und das Risiko für bestimmte Krebsarten erhöhen. Es ist wichtig, vorsichtig mit C2Cl4 umzugehen und beim Umgang damit geeignete Schutzausrüstung zu verwenden. Der Stoff sollte in einem gut belüfteten Bereich gelagert und von Wärme- oder Zündquellen ferngehalten werden. Verschüttete Flüssigkeiten sollten sofort beseitigt und gemäß den örtlichen Vorschriften ordnungsgemäß entsorgt werden.
| Gefahrensymbole | Totenkopf, Flamme |
| Sicherheitsbeschreibung | Leicht entzündlich, giftig beim Einatmen oder Verschlucken, kann Krebs erzeugen, kann Organschäden verursachen |
| EINE ID | Ein 1897 |
| HS-Code | 290323 |
| Gefahrenklasse | 6.1 (Giftige Stoffe) |
| Verpackungsgruppe | III |
| Toxizität | Tetrachlorethylen wird von der Internationalen Agentur für Krebsforschung (IARC) als Karzinogen der Gruppe 2A (wahrscheinlich krebserregend für den Menschen) und von der Europäischen Union als Reproduktionstoxin der Kategorie 2 eingestuft. |
Methoden zur Synthese von Tetrachlorethylen
Um C2Cl4 zu synthetisieren, kann man verschiedene Methoden anwenden, wie zum Beispiel die direkte Chlorierung von Ethylen , die Chlorierung von Ethylendichlorid oder die Chlorierung von Tetrachlorkohlenstoff.
Bei der Direktchlorierung reagiert Ethylengas in einem Reaktor mit Chlorgas zu C2Cl4. Mit dieser Methode können hohe Ausbeuten an C2Cl4 erzielt werden, es ist jedoch eine sorgfältige Kontrolle der Reaktionsbedingungen erforderlich, um unerwünschte Nebenprodukte zu vermeiden.
Die zweite Methode beinhaltet die Chlorierung von Ethylendichlorid, einem Nebenprodukt der Vinylchloridproduktion. Auch diese Methode liefert hohe Ausbeuten an C2Cl4, kann jedoch zur Bildung toxischer Nebenprodukte wie Hexachlorbutadien führen.
Bei der dritten Methode handelt es sich um die Chlorierung von Tetrachlorkohlenstoff, wobei als Nebenprodukt C2Cl4 entstehen kann. Allerdings ist diese Methode weniger effizient und liefert geringere Erträge als die beiden anderen Methoden.
Neben diesen Methoden ist es auch möglich, C2Cl4 durch Reaktion von Trichlorethylen mit Chlorgas oder Hexachlorethan mit Phosgen herzustellen.
Im industriellen Maßstab verwenden Hersteller üblicherweise die direkte Ethylenchlorierung und die Ethylendichloridchlorierung als die am häufigsten verwendeten Methoden zur Herstellung von C2Cl4.
Verwendung von Tetrachlorethylen
C2Cl4 hat verschiedene industrielle und kommerzielle Anwendungen, darunter:
- Chemische Reinigung: Aufgrund seiner Fähigkeit, eine Vielzahl von Flecken und Verschmutzungen zu lösen, wird es häufig als Lösungsmittel für die chemische Reinigung von Kleidung verwendet.
- Metallentfettung: Ein wirksames Lösungsmittel zum Entfernen von Öl und Fett von Metalloberflächen, wodurch es in der metallverarbeitenden Industrie nützlich ist.
- Kleb- und Dichtstoffe: Wird als Lösungsmittel bei der Herstellung von Kleb- und Dichtstoffen verwendet, da es viele Arten von Polymeren und Harzen auflösen kann.
- Chemische Zwischenprodukte: Wird als Rohstoff bei der Herstellung anderer Chemikalien wie chlorierter Lösungsmittel und Fluorkohlenwasserstoffe verwendet.
- Textil- und Lederverarbeitung: Wird in der Textil- und Lederverarbeitung als Lösungsmittel und zur Entfernung von Verunreinigungen verwendet.
- Kältemittel: Einige Anwendungen verwenden C2Cl4 als Kältemittel, aber aus Umweltgründen wird diese Verwendung schrittweise eingestellt.
- Laborlösungsmittel: Wird auch als Laborlösungsmittel verwendet, insbesondere für Chromatographie- und Spektroskopieanwendungen.
Fragen:
F: Was ist Tetrachlorethylen?
A: C2Cl4, auch bekannt als Perchlorethylen oder PCE, ist eine farblose Flüssigkeit mit mildem Geruch, die häufig als Lösungsmittel in verschiedenen industriellen und kommerziellen Anwendungen verwendet wird.
F: Schwimmt Tetrachlorethylen auf dem Wasser?
A: Nein, C2Cl4 ist dichter als Wasser, daher sinkt es und bildet eine deutliche Schicht am Boden.
F: Wo kann man Tetrachlorethylen (Perchlorethylen) als Lösungsmittel für die chemische Reinigung kaufen?
A: C2Cl4 ist ein regulierter Stoff und kann nur von lizenzierten Fachleuten in der Textilreinigungsbranche erworben werden. Es wird normalerweise von Chemielieferanten oder Händlern bezogen, die auf industrielle Lösungsmittel spezialisiert sind.
F: Welche Beziehung besteht zwischen Tetrachlorethylen und Tetrachlorkohlenstoff?
A: C2Cl4 und Tetrachlorkohlenstoff sind beides halogenierte Kohlenwasserstoffe, die Chloratome enthalten, aber unterschiedliche Strukturen und molekulare Eigenschaften haben. Tetrachlorkohlenstoff ist ein unpolares Molekül, während C2Cl4 aufgrund der Anwesenheit einer Doppelbindung zwischen zwei Kohlenstoffatomen polar ist.
F: Tetrachlorethylen in Wasser?
A: C2Cl4 ist in Wasser nur wenig löslich und neigt dazu, sich im Boden und Sediment zu verteilen, was es zu einer häufigen Verunreinigung von Grundwasser und Boden macht.
F: Unternehmen, die Tetrachlorethylen testen?
A: Viele Umwelttestunternehmen bieten C2Cl4-Testdienste für Wasser-, Boden- und Luftproben an. Einige Beispiele sind ALS Global, Eurofins TestAmerica und Environmental Testing and Consulting, Inc.
F: Was ist die Hybridisierung von C-Atomen in C2Cl4?
A: Die C-Atome in C2Cl4 weisen eine sp2-Hybridisierung auf, was bedeutet, dass sie über drei Hybridorbitale verfügen, die an der Bindung mit anderen Atomen beteiligt sind.
F: Wie groß ist der ungefähre Winkel der Chlor-Kohlenstoff-Chlor-Bindung in C2Cl4?
A: Der ungefähre Winkel der Chlor-Kohlenstoff-Chlor-Bindung in C2Cl4 beträgt 120 Grad, was charakteristisch für Moleküle mit trigonaler planarer Geometrie ist.
F: Ist C2Cl4 polar oder unpolar?
A: C2Cl4 ist ein polares Molekül, da zwischen den Kohlenstoffatomen eine Doppelbindung vorhanden ist, die zu einer asymmetrischen Ladungsverteilung und einem Dipolmoment führt.
