Natriumbisulfit (NaHSO3) ist eine chemische Verbindung, die als Lebensmittelkonservierungsmittel und in verschiedenen industriellen Anwendungen verwendet wird. Es hemmt das Wachstum von Bakterien und verhindert die Oxidation.
| IUPAC-Name | Natriumhydrogensulfit |
| Molekularformel | NaHSO3 |
| CAS-Nummer | 7631-90-5 |
| Synonyme | Natriumbisulfit, saures Natriumsulfit, Natriumhydrogensulfit, Natriumhydrogensulfit, Natriumsulfit-Monohydrat |
| InChI | InChI=1S/Na.H2O3S/c;1-4(2)3/h;(H2,1,2,3)/q+1;/p-1 |
Eigenschaften von Natriumbisulfit
Natriumbisulfit-Formel
Die chemische Formel für Natriumbisulfit lautet NaHSO3. Diese Formel gibt die Anzahl und Art der Atome an, die in einem einzelnen Natriumbisulfitmolekül vorhanden sind. Die Formel ist entscheidend für die Bestimmung des Verhaltens von Natriumbisulfit unter verschiedenen chemischen Reaktionen und physikalischen Bedingungen.
Molmasse von Natriumbisulfit
NaHSO3 hat eine Molmasse von 104,06 g/mol. Dies ist die Summe der Atommassen der Bestandteile eines einzelnen NaHSO3-Moleküls. Die Molmasse ist eine wichtige physikalische Eigenschaft, die dabei hilft, die Menge einer Substanz in einer bestimmten Probe zu bestimmen.
Siedepunkt von Natriumbisulfit
Der Siedepunkt von NaHSO3 liegt bei 150°C. Dies ist die Temperatur, bei der die flüssige Form von NaHSO3 beginnt, sich in ein Gas zu verwandeln. Der Siedepunkt ist eine entscheidende physikalische Eigenschaft, die bestimmt, wie sich ein Stoff unter verschiedenen Temperaturbedingungen verhält.
Natriumbisulfit Schmelzpunkt
Der Schmelzpunkt von NaHSO3 liegt bei 150°C. Dies ist die Temperatur, bei der die feste Form von NaHSO3 beginnt, sich in eine Flüssigkeit umzuwandeln. Der Schmelzpunkt ist eine wesentliche physikalische Eigenschaft, die dabei hilft, das Verhalten eines Stoffes unter verschiedenen Temperaturbedingungen zu bestimmen.
Dichte von Natriumbisulfit g/ml
Die Dichte von NaHSO3 beträgt 1,48 g/ml. Dies bezieht sich auf die Massemenge, die in einem bestimmten Volumen NaHSO3 vorhanden ist. Die Dichte ist eine wichtige physikalische Eigenschaft, die dabei hilft, zu bestimmen, wie sich ein Stoff unter verschiedenen Druck- und Temperaturbedingungen verhält.
Molekulargewicht von Natriumbisulfit
Das Molekulargewicht von NaHSO3 beträgt 104,06 g/mol. Dies ist die Summe der Atomgewichte der Bestandteile eines einzelnen NaHSO3-Moleküls. Das Molekulargewicht ist eine wesentliche physikalische Eigenschaft, die dabei hilft, die Menge einer Substanz in einer bestimmten Probe zu bestimmen.
Struktur von Natriumbisulfit
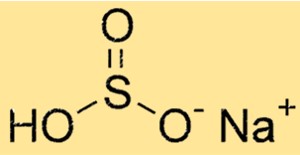
NaHSO3 hat eine Molekülstruktur, die aus einem Natriumkation (Na+) und einem HSO3–Anion besteht. Das Anion besteht aus einem Schwefelatom, drei Sauerstoffatomen und einem Wasserstoffatom. Die Struktur von NaHSO3 bestimmt seine chemischen und physikalischen Eigenschaften.
Löslichkeit von Natriumbisulfit
NaHSO3 ist in Wasser gut löslich, mit einer Löslichkeit von 62 g/100 ml bei 20 °C. Es ist auch in Glycerin löslich und in Alkohol schwer löslich. Seine Löslichkeit in Wasser macht es zu einem nützlichen Reagens bei verschiedenen chemischen Reaktionen.
| Aussehen | weißes kristallines Pulver |
| Spezifisches Gewicht | 1,48 |
| Farbe | Weiß bis leicht gelb |
| Geruch | Schwefeliger Geruch |
| Molmasse | 104,06 g/Mol |
| Dichte | 1,48 g/ml |
| Fusionspunkt | 150°C |
| Siedepunkt | 150°C |
| Blitzpunkt | Unzutreffend |
| Löslichkeit in Wasser | Sehr löslich |
| Löslichkeit | Löslich in Ethanol |
| Dampfdruck | Unzutreffend |
| Wasserdampfdichte | Unzutreffend |
| pKa | 6,97 |
| pH-Wert | 4,5–5,5 (5 %ige Lösung) |
Sicherheit und Gefahren von Natriumbisulfit
NaHSO3 kann schädlich sein, wenn es verschluckt, eingeatmet oder mit der Haut oder den Augen in Berührung kommt. Dies kann zu Hautreizungen, Augenschäden, Atemwegs- und Verdauungsproblemen führen. Eine längere Exposition kann zu schwerwiegenderen Gesundheitsproblemen führen. Es ist wichtig, NaHSO3 vorsichtig zu handhaben und zu lagern und persönliche Schutzausrüstung wie Handschuhe, Schutzbrillen und Atemschutzgeräte zu verwenden. Es muss von brennbaren Materialien und unverträglichen Substanzen ferngehalten werden. Im Falle eines versehentlichen Kontakts oder Verschluckens sollte sofort ein Arzt aufgesucht werden. Um potenzielle Gefahren zu vermeiden, müssen ordnungsgemäße Lagerungs- und Handhabungsverfahren befolgt werden.
| Gefahrensymbole | Totenkopf, ätzend |
| Sicherheitsbeschreibung | Kontakt mit Haut, Augen und Kleidung vermeiden. Nicht einnehmen oder einatmen. Verwenden Sie geeignete Schutzausrüstung. |
| UN-Identifikationsnummern | UN2693 |
| HS-Code | 28321000 |
| Gefahrenklasse | 8 |
| Verpackungsgruppe | III |
| Toxizität | Sehr giftig beim Verschlucken oder Einatmen. Kann Haut- und Augenreizungen sowie Atemwegs- und Verdauungsprobleme verursachen. Eine längere Exposition kann zu ernsthaften Gesundheitsproblemen führen. |
Methoden zur Synthese von Natriumbisulfit
Es gibt verschiedene Methoden zur Synthese von NaHSO3, die gebräuchlichste ist jedoch die Reaktion von Natriumcarbonat und Schwefeldioxid.
Um eine NaHSO3-Lösung herzustellen, mischen Sie eine Natriumcarbonatlösung mit Schwefeldioxidgas. Die Reaktion setzt Wärme frei und erfordert ein Reaktionsgefäß mit ausreichender Belüftung.
Eine andere Methode beinhaltet die Reaktion von Natriumhydroxid mit Schwefeldioxidgas, um eine Natriumsulfitlösung zu erzeugen, die dann angesäuert wird, um eine NaHSO3-Lösung zu erzeugen. Für große Mengen NaHSO3 erweist sich diese Methode als nützlich.
Um NaHSO3 zu synthetisieren, reagiert Schwefelsäure mit Natriumsulfit , wodurch eine NaHSO3-Lösung entsteht. Diese Methode ist vorteilhaft, wenn eine konzentriertere NaHSO3-Lösung erforderlich ist.
Verwendung von Natriumbisulfit
NaHSO3 hat ein breites Anwendungsspektrum in verschiedenen Branchen. Hier sind einige seiner häufigsten Verwendungszwecke:
- Lebensmittelindustrie – Wird als Lebensmittelkonservierungsmittel verwendet, um das Wachstum von Bakterien zu verhindern und die Haltbarkeit von Lebensmitteln wie Obst- und Gemüsekonserven, Säften und Wein zu verlängern.
- Wasseraufbereitung – Wird als Reduktionsmittel zur Entfernung von überschüssigem Chlor aus Trinkwasser- und Abwasseraufbereitungssystemen verwendet.
- Textilindustrie – Wird als Bleichmittel verwendet, um restliche Farbstoffe aus Textilien zu entfernen.
- Fotoindustrie – Wird als Entwicklungsmittel in der fotografischen Entwicklung verwendet.
- Ölbohren – Wird als Korrosionsinhibitor und in Rückgewinnungssystemen verwendet, um Sauerstoff zu entfernen und Korrosion bei Öl- und Gasbohrarbeiten zu verhindern.
- Pharmazeutika – Wird als Antioxidans und Reduktionsmittel bei der Herstellung bestimmter pharmazeutischer Produkte verwendet.
- Körperpflege – Wird als Haarglättungsmittel und bei der Herstellung einiger Körperpflegeprodukte wie Shampoos und Spülungen verwendet.
- Andere Verwendungen – Wird bei der Papier- und Zellstoffproduktion, als Laborreagenz und als Metallionen-Chelatbildner verwendet.
Fragen:
F: Was ist NaHSO3?
A: NaHSO3 ist die chemische Formel für Natriumbisulfit, ein Salz, das für verschiedene Zwecke in verschiedenen Industrien verwendet wird.
F: Wie hoch ist der ungefähre pH-Wert von 0,015 M NaHSO3?
A: Der ungefähre pH-Wert von 0,015 M NaHSO3 beträgt etwa 7. Diese Lösung ist neutral, da sie weder eine Säure noch eine Base ist.
F: Ist NaHSO3 sauer oder basisch?
A: NaHSO3 ist leicht sauer, da es Wasserstoffionen in Wasser abgeben kann, um HSO3- und H+-Ionen zu bilden.
F: Wie hoch ist die Oxidationszahl von Schwefel (S) in NaHSO3, einem der in diesem Experiment verwendeten Reaktanten?
A: Die Oxidationszahl von Schwefel (S) in NaHSO3 beträgt +4.
F: Was macht NaHSO3?
A: NaHSO3 wird als Reduktionsmittel und Schwefeldioxidquelle verwendet. Es kann auch als Antioxidans und Konservierungsmittel in Lebensmitteln und pharmazeutischen Produkten wirken.
F: Wenn Sie 1,00 kg I2 herstellen möchten, welche Massen an NaIO3 und NaHSO3 werden benötigt?
A: Die ausgewogene chemische Gleichung für die Reaktion zwischen NaIO3 und NaHSO3 unter Bildung von I2 lautet: 5NaIO3 + NaHSO3 + 3H2O → 3I2 + 5NaSO4 + 3H2SO4. Stöchiometrisch würden Sie 3,33 kg NaIO3 und 1,00 kg NaHSO3 benötigen, um 1,00 kg I2 herzustellen. .
F: Warum haben wir am Ende der Reaktion Natriumbisulfit hinzugefügt?
A: Am Ende einiger chemischer Reaktionen wird NaHSO3 hinzugefügt, um überschüssiges Brom zu entfernen, das schädlich sein oder spätere Schritte im Prozess beeinträchtigen kann.
F: Was ist Natriumbisulfit?
A: NaHSO3 ist ein Salz, das aufgrund seiner reduzierenden, antioxidativen und konservierenden Eigenschaften in verschiedenen Branchen, einschließlich der Lebensmittel-, Pharma- und Wasseraufbereitung, verwendet wird.
F: Wie entfernt Natriumbisulfit Brom?
A: NaHSO3 reagiert mit Brom unter Bildung von Natriumbromid und Schwefeldioxidgas, wodurch überschüssiges Brom effektiv aus einer Lösung entfernt wird.
F: Was ist Menadion-Natriumbisulfit-Komplex?
A: Menadion-Natriumbisulfit-Komplex ist eine synthetische Verbindung, die in einigen Nahrungsergänzungsmitteln und Tiernahrungsprodukten als Vitamin-K-Quelle verwendet wird.
F: Wofür wird Natriumbisulfit verwendet?
A: NaHSO3 wird als Reduktionsmittel, Antioxidans und Konservierungsmittel in verschiedenen Branchen eingesetzt, darunter in der Lebensmittel-, Pharma-, Wasseraufbereitungs- und Ölförderungsbranche. Es kann auch als Haarglättungsmittel und in der fotografischen Verarbeitung verwendet werden.
