1-Buten (C4H8) ist ein farbloses Gas mit leicht süßlichem Geruch. Es wird bei der Herstellung von Polyethylen und als Rohstoff für andere Chemikalien verwendet.
| IUPAC-Name | Mais-1-ène |
| Molekularformel | C4H8 |
| CAS-Nummer | 106-98-9 |
| Synonyme | Butylen, Ethylen, Vinylmethylen |
| InChI | 1S/C4H8/c1-3-4-2/h3-4H,1-2H3 |
Eigenschaften von 1-Buten
Formel 1-Buten
Die chemische Formel für 1-Buten lautet C4H8 und gibt die Anzahl und Art der im Molekül vorhandenen Atome an. Die Formel besagt, dass 1-Buten vier Kohlenstoffatome und acht Wasserstoffatome enthält. Die Formel für 1-Buten ist nützlich zur Bestimmung seines Molekulargewichts und zur Berechnung seiner Reaktivität bei chemischen Reaktionen.
Molmasse von 1-Buten
1-Buten, auch But-1-en genannt, hat eine Molmasse von 56,11 g/mol. Die Molmasse bezieht sich auf die Masse eines Mols einer Substanz und wird durch Addition der Atommassen jedes Atoms in einem Molekül berechnet. Im Fall von But-1-en enthält das Molekül vier Kohlenstoffatome und acht Wasserstoffatome, jedes mit seiner jeweiligen Atommasse.
Siedepunkt von 1-Buten
But-1-en hat einen Siedepunkt von -6,3 °C oder 20,7 °F. Der Siedepunkt bezeichnet die Temperatur, bei der eine Flüssigkeit bei einem festgelegten Druck in ein Gas übergeht. Da But-1-en bei Raumtemperatur ein Gas ist, benötigt es einen niedrigen Siedepunkt, um seinen gasförmigen Zustand beizubehalten. Der Siedepunkt von But-1-en wird durch Faktoren wie Druck und die Anwesenheit anderer Chemikalien beeinflusst.
1-Buten-Schmelzpunkt
But-1-en hat einen Schmelzpunkt von -185,4 °C oder -301,7 °F. Der Schmelzpunkt bezieht sich auf die Temperatur, bei der ein Feststoff bei einem festgelegten Druck in eine Flüssigkeit übergeht. Da But-1-en bei Raumtemperatur ein Gas ist, liegt es nicht in festem Zustand vor. Der Schmelzpunkt von But-1-en bleibt jedoch ein nützlicher Parameter zur Bestimmung seiner physikalischen und chemischen Eigenschaften.
Dichte von 1-Buten g/ml
But-1-en hat bei Raumtemperatur eine Dichte von 0,573 g/ml. Unter Dichte versteht man die Menge an Masse pro Volumeneinheit eines Stoffes. Die Dichte von But-1-en ist geringer als die von Wasser, das eine Dichte von 1 g/ml hat, was darauf hindeutet, dass But-1-en weniger dicht als Wasser ist. Die Dichte von But-1-en wird durch Faktoren wie Temperatur und Druck beeinflusst.
Molekulargewicht von 1-Buten
But-1-en hat ein Molekulargewicht von 56,11 g/mol. Das Molekulargewicht ist die Summe der Atomgewichte aller Atome in einem Molekül. Das Molekulargewicht von But-1-en ist ein wichtiger Faktor bei der Bestimmung seiner physikalischen und chemischen Eigenschaften sowie seines Verhaltens bei chemischen Reaktionen.
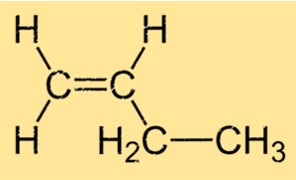
1-Buten-Struktur
But-1-en hat eine lineare Struktur mit vier Kohlenstoffatomen, die in einer geraden Kette aneinander gebunden sind, und jedem Kohlenstoffatom, das an zwei Wasserstoffatome gebunden ist. Die Summenformel für But-1-en lautet C4H8 und gehört zur Gruppe der Kohlenwasserstoffe, die Alkene genannt werden. Die Doppelbindung zwischen dem ersten und zweiten Kohlenstoffatom des Moleküls ist für seine Reaktivität bei chemischen Reaktionen verantwortlich.
| Aussehen | Farbloses Gas |
| Spezifisches Gewicht | 0,573 |
| Farbe | Farblos |
| Geruch | Leicht süßlicher Geruch |
| Molmasse | 56,11 g/Mol |
| Dichte | 0,573 g/ml bei Raumtemperatur |
| Fusionspunkt | -185,4°C oder -301,7°F |
| Siedepunkt | -6,3°C oder 20,7°F |
| Blitzpunkt | -70 °C (-94 °F) |
| Löslichkeit in Wasser | Unlöslich |
| Löslichkeit | Löslich in organischen Lösungsmitteln |
| Dampfdruck | 278,4 kPa bei 20 °C |
| Wasserdampfdichte | 2,98 (Luft = 1) |
| pKa | 45.1 |
| pH-Wert | Neutral |
Sicherheit und Gefahren von 1-Buten
But-1-en ist ein brennbares Gas und kann mit Luft explosive Gemische bilden. Außerdem reizt es die Augen, die Haut und die Atemwege. Die Exposition gegenüber hohen But-1-en-Konzentrationen kann Schwindel, Übelkeit und Kopfschmerzen verursachen. Daher sollten beim Umgang mit But-1-en geeignete Belüftungs- und Schutzausrüstungen verwendet werden. Es ist wichtig, But-1-en fern von Zündquellen und unverträglichen Materialien zu lagern und zu handhaben. Im Falle eines Lecks oder einer Verschüttung muss der Bereich sofort evakuiert und die Notfallmaßnahmen befolgt werden. Darüber hinaus sollten geeignete Entsorgungsmethoden angewendet werden, um eine Umweltverschmutzung zu vermeiden.
| Gefahrensymbole | F+ (leicht entzündlich) |
| Sicherheitsbeschreibung | Von Zündquellen fernhalten. Nur in gut belüfteten Bereichen verwenden. Schutzausrüstung tragen. |
| UN-Identifikationsnummern | UN 1012 |
| HS-Code | 290110 |
| Gefahrenklasse | 2.1 (Brennbares Gas) |
| Verpackungsgruppe | Gruppe II |
| Toxizität | Das Einatmen hoher Konzentrationen kann zu einer Depression des Zentralnervensystems führen. |
Methoden zur Synthese von 1-Buten
Zur Synthese von But-1-en gibt es verschiedene Methoden, darunter das katalytische Cracken von Rohölfraktionen oder die Dehydratisierung von Butanol.
Eine gängige Methode ist die katalytische Dehydrierung von Butenen, bei der Wasserstoffatome aus Butenen entfernt werden, um Buten-1 zu bilden. Verschiedene Katalysatoren wie Chrom-Aluminiumoxid, Kupferchromit oder Platin können diesen Prozess durchführen.
Eine andere Methode beinhaltet die selektive Dimerisierung von Ethylen und die anschließende Dehydratisierung der resultierenden Butene unter Bildung von But-1-en. Zeolithkatalysatoren wie ZSM-5 oder SAPO-11 können diesen Prozess umsetzen.
Ein Wolfram-Carben-Komplex kann die Metathesereaktion zwischen Propylen und Ethylen zur Herstellung von But-1-en katalysieren. Diese Methode ist interessant, weil sie die Herstellung von But-1-en aus erneuerbaren Ressourcen wie Ethylen biologischen Ursprungs ermöglicht.
Verwendungen von 1-Buten
But-1-en ist eine vielseitige chemische Verbindung, die vielfältige industrielle und kommerzielle Anwendungen findet. Zu den häufigsten Anwendungen von But-1-en gehören:
- Polyethylenproduktion: Wird als Comonomer bei der Herstellung von Polyethylen hoher Dichte und linearem Polyethylen niedriger Dichte verwendet. Der Zusatz von 1-Buten trägt zur Verbesserung der mechanischen und thermischen Eigenschaften des Polymers bei.
- Chemische Zwischenprodukte: Wird als chemisches Zwischenprodukt bei der Herstellung verschiedener Chemikalien wie Butadien, Butene, Butyraldehyd und Butanol verwendet.
- Kraftstoff und Kraftstoffzusätze: Wird aufgrund seiner hohen Oktanzahl und sauberen Verbrennungseigenschaften als Kraftstoff oder Kraftstoffzusatz verwendet.
- Kältemittel: Wird aufgrund seines niedrigen Siedepunkts und seiner nicht brennbaren Natur als Kältemittel verwendet.
- Klebstoffe: Wird bei der Herstellung von Schmelzklebstoffen verwendet. Diese werden häufig in der Verpackungsindustrie verwendet.
- Gummi und Kunststoffe: Wird als Rohstoff für die Herstellung von synthetischem Gummi und Kunststoffen wie Polybuten verwendet.
- Schmierstoffe: Wird als Schmierstoffzusatz zur Verbesserung der Schmier- und Verschleißschutzeigenschaften von Schmierstoffen verwendet.
- Pharmazeutische Industrie: Wird als Rohstoff bei der Synthese verschiedener pharmazeutischer Produkte verwendet.
Fragen:
F: Warum könnte es schwierig sein, die Trennung von cis- und trans-2-Buten durch TLC darzustellen?
A: Es kann schwierig sein, die Trennung von cis- und trans-2-Buten durch DC zu visualisieren, da diese Isomere sehr ähnliche physikalische und chemische Eigenschaften haben. Dies kann zu überlappenden Flecken auf der DC-Platte führen, was die Unterscheidung zwischen den beiden Isomeren erschwert.
F: Wie groß ist die Molmasse von 1-Buten, wenn 5,38 × 1016 Moleküle 1-Buten 5,00 μg wiegen?
A: Die Molmasse von But-1-en lässt sich aus der angegebenen Molekülzahl und dem Gewicht der Probe berechnen. Die Molmasse von But-1-en beträgt 56,11 g/mol.
F: Ihre Aufgabe besteht darin, 2-Brombutan mit der höchsten Ausbeute in 1-Buten umzuwandeln. Welche Reagenzien würden Sie verwenden?
A: Eine mögliche Methode zur Umwandlung von 2-Brombutan in But-1-en besteht darin, eine E2-Eliminierungsreaktion unter Verwendung einer starken Base wie Kalium-tert-butoxid (KOtBu) in einem polaren aprotischen Lösungsmittel wie Dimethylsulfoxid (DMSO) durchzuführen ). Goldtetrahydrofuran (THF).
F: Wie stellt man 1-Buten her?
A: But-1-en kann durch verschiedene Methoden hergestellt werden, beispielsweise durch katalytische Dehydrierung von Butenen, selektive Dimerisierung von Ethylen mit anschließender Dehydratisierung oder die Metathesereaktion zwischen Propylen und Ethylen. Diese Methoden erfordern unterschiedliche Katalysatoren und Reaktionsbedingungen, und es muss besonderes Augenmerk darauf gelegt werden, eine hohe Ausbeute und Reinheit des Endprodukts sicherzustellen.
