Diethylether oder Ethoxyethan ist eine farblose, leicht entzündliche und flüchtige Flüssigkeit, die üblicherweise als Lösungsmittel und als Ausgangsmaterial für die Synthese anderer organischer Verbindungen verwendet wird.
| IUPAC-Name | Ethoxyethan |
| Molekularformel | C4H10O |
| CAS-Nummer | 60-29-7 |
| Synonyme | Ether, Ethylether, Ethyloxid, Diethyloxid, 1,1′-Oxybisethan, Ether, Anästhesieether, Schwefelsäureether, Ethylether |
| InChI | InChI=1S/C4H10O/c1-3-5-4-2/h3-4H2.1-2H3 |
Eigenschaften von Diethylether
Dichte von Diethylether g/ml
Die Dichte von Diethylether beträgt 0,713 g/ml. Die Dichte ist definiert als die Masse eines Stoffes pro Volumeneinheit. Im Fall von Diethylether ist seine Dichte geringer als die von Wasser, das eine Dichte von 1 g/ml hat. Das bedeutet, dass Diethylether auf der Wasseroberfläche schwimmt.
Molmasse von Diethylether
Diethylether hat eine Molmasse von 74,12 g/mol. Die Molmasse ist die Masse eines Mols einer Substanz, ausgedrückt in Gramm. Im Fall von Ethoxyethan enthält ein Mol der Verbindung 74,12 Gramm. Dieser Wert ergibt sich aus den Atommassen von Kohlenstoff, Wasserstoff und Sauerstoff, aus denen das Molekül besteht. Die Molmasse einer Substanz ist ein wichtiger Parameter in chemischen Berechnungen, da sie zur Bestimmung der in einer bestimmten Probe vorhandenen Substanzmenge verwendet wird.
Struktur von Diethylether
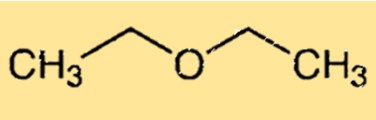
Diethylether hat eine einfache chemische Struktur, die aus zwei an ein Sauerstoffatom gebundenen Ethylgruppen besteht. Aufgrund des freien Elektronenpaars am Sauerstoffatom weist das Molekül eine gebogene Form auf, was dazu führt, dass das Molekül von der idealen tetraedrischen Geometrie abweicht. Die gekrümmte Struktur von Ethoxyethan ist für seine Fähigkeit verantwortlich, Wasserstoffbrückenbindungen mit anderen Molekülen zu bilden, was es zu einem nützlichen Lösungsmittel macht.
Siedepunkt von Diethylether
Der Siedepunkt von Diethylether beträgt 34,6 °C (94,3 °F). Der Siedepunkt ist die Temperatur, bei der ein Stoff bei Atmosphärendruck vom flüssigen in den gasförmigen Zustand übergeht. Diethylether hat einen relativ niedrigen Siedepunkt und ist daher eine flüchtige Flüssigkeit, die bei Raumtemperatur leicht verdunstet. Diese Eigenschaft macht es als Lösungsmittel und Anästhetikum in der Medizin nützlich.
Schmelzpunkt von Diethylether
Der Schmelzpunkt von Ethoxyethan beträgt -116,3 °C (-177,3 °F). Der Schmelzpunkt ist die Temperatur, bei der ein fester Stoff bei Atmosphärendruck in den flüssigen Zustand übergeht. Ethoxyethan ist bei Raumtemperatur eine farblose Flüssigkeit und aufgrund seines niedrigen Schmelzpunkts kommt es selten vor, dass es in festem Zustand vorliegt.
Molekulargewicht von Diethylether
Ethoxyethan hat ein Molekulargewicht von 74,12 g/mol. Das Molekulargewicht ist die Summe der Atomgewichte aller Atome in einem Molekül. Es ist ein wichtiger Parameter bei chemischen Reaktionen und der Stöchiometrie, da er die Menge des Reaktanten bestimmt, die zur Bildung einer bestimmten Produktmenge erforderlich ist.
Diethylether-Formel
Die chemische Formel für Ethoxyethan lautet C4H10O. Es besteht aus vier Kohlenstoffatomen, zehn Wasserstoffatomen und einem Sauerstoffatom. Die Formel gibt die genaue Anzahl jeder Atomart in einem Molekül an und wird zur Bestimmung des Molekulargewichts der Substanz verwendet. Die chemische Formel einer Substanz ist in chemischen Gleichungen von wesentlicher Bedeutung, da sie dazu dient, Reaktionen auszugleichen und die Menge an Reaktanten und Produkten zu bestimmen.
| Aussehen | Farblose Flüssigkeit |
| Spezifisches Gewicht | 0,713 |
| Farbe | Farblos |
| Geruch | Weich, wie Äther |
| Molmasse | 74,12 g/Mol |
| Dichte | 0,713 g/ml |
| Fusionspunkt | -116,3°C (-177,3°F) |
| Siedepunkt | 34,6°C (94,3°F) |
| Blitzpunkt | -45°C (-49°F) |
| Löslichkeit in Wasser | 6,9 g/L bei 25°C |
| Löslichkeit | Mit den meisten organischen Lösungsmitteln mischbar |
| Dampfdruck | 440 mmHg bei 25°C |
| Wasserdampfdichte | 2.5 |
| pKa | 15.9 |
| pH-Wert | 7 (neutral) |
Diethylether Sicherheit und Gefahren
Bei der Handhabung von Ethoxyethan müssen verschiedene Sicherheits- und Gefahrenaspekte berücksichtigt werden. Es ist leicht entzündlich und kann explosionsfähige Dampf-Luft-Gemische bilden. Daher muss es von Zündquellen und Funken ferngehalten werden. Es kann außerdem zu Reizungen der Haut, der Augen und der Atemwege führen und bei längerer Exposition zu Schwindel und Kopfschmerzen führen. Bei der Verwendung von Ethoxyethan ist eine ausreichende Belüftung erforderlich und es sollte Schutzausrüstung wie Handschuhe und Schutzbrille getragen werden. Es sollte außerdem an einem kühlen, trockenen Ort, entfernt von Oxidationsmitteln und inkompatiblen Materialien, gelagert werden.
| Gefahrensymbole | F, Xi |
| Sicherheitsbeschreibung | S9, S16, S29, S33, S60, S61 |
| UN-Identifikationsnummern | UN 1155 |
| HS-Code | 2909.19.00 |
| Gefahrenklasse | 3 |
| Verpackungsgruppe | II |
| Toxizität | LD50 (oral, Ratte): 3.500 mg/kg |
Methoden zur Synthese von Diethylether
Es gibt verschiedene Methoden zur Synthese von Diethylether, einschließlich der Reaktion von Ethanol mit Schwefelsäure und der Dehydratisierung des Ethanols mithilfe eines Dehydratisierungsmittels wie Schwefelsäure oder Aluminiumoxid.
Um Ethoxyethan über die Dehydratisierungsmethode zu synthetisieren, erhitzen Sie Ethanol mit einem Dehydratisierungsmittel wie Schwefelsäure oder Aluminiumoxid, um ein Wassermolekül zu entfernen und Ethoxyethan zu bilden. Um die Reaktionsausbeute zu verbessern, kann ein Katalysator wie Kaliumhydroxid oder Natriumhydroxid verwendet werden.
Eine weitere Methode zur Synthese von Ethoxyethan ist die Synthese von Williamson-Ether, bei der Ethanol mit einem Alkoxidion wie Natriumethoxid unter Bildung von Ethoxyethan reagiert. Diese Reaktion erfordert die Verwendung einer starken Base und eines geeigneten Lösungsmittels, beispielsweise wasserfreies Ethanol.
Eine andere Methode zur Herstellung von Ethoxyethan ist die Verwendung der Tischtschenko-Reaktion. Bei diesem Verfahren reagieren Essigsäure und Ethanol in Gegenwart eines Katalysators wie Schwefelsäure oder Aluminiumoxid, was zu einer hohen Ausbeute an Ethoxyethan führt.
Um Ethoxyethan als Endprodukt herzustellen, kann Natriumborhydrid oder Natriumamalgam zur Reduzierung von Acetaldehyd verwendet werden. Dies ist eine weitere Methode zur Synthese von Ethoxyethan. Diese Reaktion führt zur Bildung von Ethanol , das dann der oben beschriebenen Dehydratisierungsmethode unterzogen werden kann, um Ethoxyethan zu bilden.
Verwendung von Diethylether
Einige Anwendungen von Diethylether umfassen:
- Lösungsmittel: Ein sehr wirksames Lösungsmittel für eine Reihe organischer Verbindungen, darunter Öle, Fette, Harze und Wachse. Wird zur Herstellung von Lacken, Firnissen und anderen Beschichtungen verwendet.
- Anästhetikum: Wird als Anästhetikum bei chirurgischen Eingriffen verwendet, obwohl es in der modernen Medizin weitgehend durch sicherere Alternativen ersetzt wurde.
- Extraktion: Wird als Extraktionslösungsmittel bei der Herstellung von Arzneimitteln, Naturprodukten und ätherischen Ölen verwendet.
- Kraftstoffzusatz: Wird als Kraftstoffzusatz zur Verbesserung der Leistung von Dieselmotoren verwendet, da er die Cetanzahl des Kraftstoffs erhöhen kann.
- Chemisches Zwischenprodukt: Ein wichtiges Zwischenprodukt bei der Herstellung einer Reihe organischer Verbindungen, darunter Ethanol, Acetaldehyd und Essigsäure.
- Aromastoff: Wird als Aromastoff bei der Herstellung bestimmter Lebensmittel und Getränke wie Süßigkeiten und Liköre verwendet.
- Laborreagenz: Wird als Reagenz in Laborexperimenten verwendet, insbesondere in der organischen Chemie.
- Aerosol-Treibmittel: Wird als Treibmittel in Aerosolprodukten verwendet. Sicherheitsbedenken führten dazu, dass diese Nutzung schrittweise aufgegeben wurde.
Fragen:
F: Ist Diethylether polar?
A: Ja, Ethoxyethan ist aufgrund des Vorhandenseins des Sauerstoffatoms ein polares Molekül, das an einem Ende des Moleküls eine teilweise negative Ladung und am anderen Ende eine teilweise positive Ladung erzeugt.
F: Ist Diethylether mit Wasser mischbar?
A: Ethoxyethan ist in Wasser nicht sehr löslich. Allerdings gilt es als teilweise wassermischbar, d. h. es kann sich zwar teilweise, aber nicht vollständig mit Wasser vermischen.
F: Ist Diethylether brennbar?
A: Ja, Ethoxyethan ist leicht entzündlich und kann mit Luft explosive Gemische bilden.
F: Ist Diethylether polar oder unpolar?
A: Ethoxyethan ist aufgrund der Anwesenheit des Sauerstoffatoms ein polares Molekül.
F: Ist Diethylether polar aprotisch?
A: Ja, Ethoxyethan gilt als polares aprotisches Lösungsmittel, was bedeutet, dass es polare Moleküle auflösen kann, aber kein Wasserstoffatom besitzt, das als Donor für Wasserstoffbrücken fungieren kann.
