1-Brombutan ist eine farblose flüssige organische Verbindung mit der Summenformel C4H9Br. Es wird als Alkylierungsmittel in der organischen Synthese und als Lösungsmittel in der Industrie verwendet.
| IUPAC-Name | Butylbromid |
| Molekularformel | C4H9Br |
| CAS-Nummer | 109-65-9 |
| Synonyme | 1-Brombutan, n-Butylbromid, Butylbromid, Brombutan, Butan, 1-Brom-, 109-65-9, 1-Brombutan, 1-Brombutan, n-C4H9Br |
| InChI | InChI=1S/C4H9Br/c1-2-3-4-5/h2-4H2.1H3 |
Molmasse von 1-Brombutan
Die Molmasse von 1-Brombutan beträgt 137,03 g/mol. Um die Molmasse von 1-Brombutan zu erhalten, addieren wir die Atommassen von Kohlenstoff, Wasserstoff und Brom in einem einzelnen Molekül. Chemische Berechnungen erfordern oft die Umrechnung der Masse eines Stoffes in seine Molzahl, und für diese Umrechnung ist die Molmasse entscheidend.
Dichte von 1-Brombutan g/ml
Die Dichte von 1-Brombutan beträgt 1,27 g/ml bei 25 °C (77 °F). Dies ist die Masse pro Volumeneinheit des Stoffes. Die Dichte von 1-Brombutan ist größer als die von Wasser, sodass es sich leicht aus wässrigen Lösungen abtrennen lässt.
Siedepunkt von 1-Brombutan
Der Siedepunkt von 1-Brombutan beträgt 101 °C (214 °F). Es handelt sich um die Temperatur, bei der der Dampfdruck der Flüssigkeit dem Außendruck entspricht. Sie ist ein Maß für die Stärke zwischenmolekularer Kräfte in der Flüssigkeit. Der Siedepunkt von 1-Brombutan macht es zu einem nützlichen Lösungsmittel und Reagens in der organischen Chemie.
Schmelzpunkt von C4H9Br
Der Schmelzpunkt von C4H9Br beträgt -112 °C (-170 °F). Dabei handelt es sich um die Temperatur, bei der die feste und flüssige Phase eines Stoffes im Gleichgewicht sind. Der Schmelzpunkt hängt von der Stärke der im Feststoff vorhandenen zwischenmolekularen Kräfte ab. Der niedrige Schmelzpunkt von C4H9Br macht es bei Raumtemperatur flüssig und ermöglicht eine einfache Handhabung.
Molekulargewicht C4H9Br
Das Molekulargewicht von C4H9Br beträgt 137,03 g/mol. Es ist die Summe der Atomgewichte aller Atome im Molekül. Das Molekulargewicht wird verwendet, um die Menge einer Substanz zu berechnen, die für eine Reaktion benötigt wird, oder um die Menge des erhaltenen Produkts zu bestimmen.
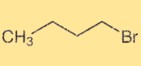
1-Brombutan-Struktur
1-Brombutan hat eine geradkettige Alkylstruktur mit einem Bromatom am vierten Kohlenstoffatom. Es ist eine organische Verbindung mit der chemischen Formel C4H9Br. Die Struktur von 1-Brombutan bestimmt seine physikalischen und chemischen Eigenschaften sowie seine Reaktivität bei organischen Reaktionen.
Formel 1-Brombutan
Die Formel für 1-Brombutan lautet C4H9Br. Dies zeigt die Anzahl und Art der im Molekül vorhandenen Atome. Die Formel von 1-Brombutan ist wichtig für die Bestimmung seiner Reaktivität und seines Verhaltens bei chemischen Reaktionen.
| Aussehen | Farblose Flüssigkeit |
| Spezifisches Gewicht | 1,27 bei 25°C |
| Farbe | Farblos |
| Geruch | Charakteristischer und süßer Geruch |
| Molmasse | 137,03 g/Mol |
| Dichte | 1,27 g/ml bei 25 °C |
| Fusionspunkt | -112°C |
| Siedepunkt | 101°C |
| Blitzpunkt | 25°C |
| Löslichkeit in Wasser | Schwach löslich |
| Löslichkeit | Löslich in Ethanol, Ether, Chloroform |
| Dampfdruck | 10 mmHg bei 25°C |
| Wasserdampfdichte | 4.6 |
| pKa | 16.5 |
| pH-Wert | Neutral |
1-Brombutan Sicherheit und Gefahren
1-Brombutan ist eine gefährliche Chemikalie, die mit Vorsicht gehandhabt werden sollte. Es ist giftig, wenn es eingenommen oder eingeatmet wird, und kann bei Kontakt Haut- und Augenreizungen verursachen. Die Chemikalie ist außerdem brennbar und kann eine Brandgefahr darstellen, wenn sie Hitze, Funken oder Flammen ausgesetzt wird. Beim Umgang mit 1-Brombutan ist das Tragen geeigneter Schutzausrüstung wie Handschuhe, Schutzbrille und Laborkittel wichtig. Die Chemikalie sollte an einem kühlen, trockenen und gut belüfteten Ort gelagert und von Zündquellen ferngehalten werden. Im Falle einer versehentlichen Exposition die betroffene Stelle sofort mit Wasser ausspülen und einen Arzt aufsuchen.
| Gefahrensymbole | T,F |
| Sicherheitsbeschreibung | Von Hitze, Funken und Flammen fernhalten. Schutzhandschuhe/Augenschutz/Gesichtsschutz tragen. BEI EINATMEN: Das Opfer an die frische Luft bringen und in einer Position ruhigstellen, die das Atmen erleichtert. BEI VERSCHLUCKEN: Bei Unwohlsein GIFTINFORMATIONSZENTRUM oder Arzt anrufen. Spülen Sie Ihren Mund aus. An einem gut belüfteten Ort aufbewahren. Ruhig halten. Inhalt/Behälter gemäß den lokalen/regionalen/nationalen/internationalen Vorschriften entsorgen. |
| AN-Kennungen | UN1126 |
| HS-Code | 290339 |
| Gefahrenklasse | 3 |
| Verpackungsgruppe | II |
| Toxizität | Giftig bei Verschlucken oder Einatmen. Kann Haut- und Augenreizungen verursachen. |
Methoden zur Synthese von 1-Brombutan
C4H9Br kann durch die Reaktion von 1-Butanol und Bromwasserstoffsäure (HBr) in Gegenwart von Schwefelsäure (H2SO4) als Katalysator synthetisiert werden. Dies wird als säurekatalysierte Halogenierungsreaktion bezeichnet. Die Reaktion läuft wie folgt ab:
- HBr wird in Gegenwart von Schwefelsäure zu 1-Butanol gegeben.
- HBr protoniert die Hydroxylgruppe von 1-Butanol und erzeugt so eine gute Abgangsgruppe (Wasser).
- Die Abgangsgruppe (Wasser) wird durch das Bromidion (Br-) von HBr ersetzt, wodurch C4H9Br entsteht.
- Die Reaktionsmischung wird dann erhitzt, um das C4H9Br zu destillieren.
Eine andere Methode zur Synthese von C4H9Br beinhaltet die Reaktion von Buten mit Bromwasserstoff in Gegenwart eines Peroxidinitiators wie Benzoylperoxid oder t-Butylperoxid. Dies wird als radikalische Halogenierungsreaktion bezeichnet. Die Reaktion läuft wie folgt ab:
- Buten wird einer Mischung aus Bromwasserstoff und einem Peroxidinitiator zugesetzt.
- Der Peroxidinitiator wird homolytisch gespalten, wodurch zwei reaktive Radikale entstehen.
- Die Radikale greifen die Doppelbindung von Buten an und bilden ein Bromidradikal und ein kohlenstoffzentriertes Radikal.
- Das Bromidradikal reagiert dann mit dem kohlenstoffzentrierten Radikal und bildet C4H9Br.
Beide Methoden werden häufig für die Synthese von C4H9Br eingesetzt und können optimiert werden, um hohe Produktausbeuten zu erzielen. Bei der Arbeit mit gefährlichen Chemikalien wie HBr und Peroxiden ist es jedoch wichtig, die entsprechenden Sicherheitsvorkehrungen zu beachten.
Verwendung von 1-Brombutan
C4H9Br ist eine vielseitige Chemikalie, die in verschiedenen Industrie- und Laboranwendungen eingesetzt wird.
- Organische Chemiker nutzen C4H9Br als Rohstoff zur Synthese anderer organischer Verbindungen, insbesondere für die Herstellung von Pharmazeutika und Agrochemikalien.
- Chemische Reaktionen erfordern C4H9Br als Lösungsmittel und dienen als Reagens in der organischen Synthese.
- Hersteller integrieren C4H9Br in Aromen, Duftstoffe und andere aromatische Verbindungen. Darüber hinaus ist es Bestandteil der Tensidproduktion und wird häufig in Reinigungsmitteln wie Waschmitteln und Seifen verwendet.
- C4H9Br fungiert als Oktanverstärker in Benzinadditiven und wird bei der Herstellung von Kältemitteln und Polymeren verwendet.
- Analysetechniken wie die Gaschromatographie erfordern C4H9Br als Standard-Laborreferenzmaterial. Lehr- und Forschungslabore für organische Chemie verwenden es als Rohstoff für verschiedene Experimente.
Insgesamt machen die vielseitigen Eigenschaften von C4H9Br es zu einer wichtigen Chemikalie in chemischen, pharmazeutischen und industriellen Bereichen mit einem breiten Anwendungsspektrum in der organischen Synthese, Produktion und Forschung.
Fragen:
Ihre Aufgabe ist es, 2-Brombutan mit höchster Ausbeute in 1-Buten umzuwandeln. Welche Reagenzien würden Sie verwenden?
Um 2-Brombutan mit der höchsten Ausbeute in 1-Buten umzuwandeln, würde ich eine starke Base wie Natriumethoxid (NaOEt) in Ethanol als Reagenz verwenden. Die Reaktion würde als Eliminierungsreaktion ablaufen, die als Dehydrohalogenierungsreaktion bekannt ist.
Die Reaktion würde wie folgt ablaufen:
- 2-Brombutan wird zu einer Lösung von Natriumethoxid in Ethanol gegeben.
- Die starke Base extrahiert ein Proton aus dem Beta-Kohlenstoff neben dem Brom und bildet ein intermediäres Alkoxidion.
- Das intermediäre Alkoxidion eliminiert die Abgangsgruppe (Brom), was zur Bildung des Alkens (1-Buten) und Natriumbromid führt.
- Die Reaktionsmischung wird dann destilliert, um das 1-Buten-Produkt zu entfernen.
Durch die Verwendung einer starken Base wie NaOEt kann die Reaktion in Richtung der Bildung von 1-Buten vorangetrieben werden, und durch die Verwendung von Ethanol als Lösungsmittel kann die Reaktion relativ sicher und kostengünstig durchgeführt werden. Darüber hinaus kann die Verwendung einer starken Base und Ethanol als Lösungsmittel zu hohen Ausbeuten an 1-Buten führen.
Warum sollten Sie im Aceton-Test mit 1-Brombutan für Ihren Nai beginnen?
Der Beginn mit C4H9Br für den NAI im Acetontest ist eine nützliche Methode, um festzustellen, ob eine bestimmte organische Verbindung ein Halogenatom enthält oder nicht. Der Test beinhaltet die Zugabe von Natriumiodid (NaI) zu der in Aceton gelösten organischen Verbindung, gefolgt von der Zugabe einer kleinen Menge Chlor oder Jod.
Die Reaktion läuft nach folgendem Mechanismus ab:
- Der in Aceton gelösten organischen Verbindung wird NaI zugesetzt, was zur Bildung des Natriumhalogenidsalzes und des entsprechenden organischen Halogenids führt.
- Die Zugabe einer kleinen Menge Chlor oder Jod führt zur Bildung einer kleinen Menge Halogengas, das mit dem Natriumhalogenid unter Bildung des entsprechenden Halogengases reagiert.
- Das Halogengas reagiert dann mit dem organischen Halogenid und bildet einen farbigen Niederschlag, der auf das Vorhandensein des Halogens in der ursprünglichen organischen Verbindung hinweist.
C4H9Br ist eine häufig verwendete Verbindung für diesen Test, da es sich um eine einfache, leicht zugängliche organische Verbindung handelt, die ein Halogenatom (Brom) enthält. Es reagiert auch leicht mit Natriumiodid und Halogengas und bildet einen farbigen Niederschlag, was es zu einer nützlichen Testverbindung zum Nachweis des Vorhandenseins eines Halogens in anderen organischen Verbindungen macht.
