Toluol ist eine farblose Flüssigkeit mit einem süßen, stechenden Geruch. Es wird häufig als Lösungsmittel sowie bei der Herstellung von Chemikalien, Farbstoffen und Pharmazeutika verwendet. Es kann schädlich sein, wenn es in großen Mengen eingenommen oder eingeatmet wird.
| IUPAC-Name | Methylbenzol |
| Molekularformel | C7H8 |
| CAS-Nummer | 108-88-3 |
| Synonyme | Toluol, Phenylmethan, Methylbenzol, Tolusol, Toluol, Methylbenzol, Toluolöl, Anisen, Antisal 1A, Benzol, Methyl, Monomethylbenzol |
| InChI | InChI=1S/C7H8/c1-7-5-3-2-4-6-7/h2-6H,1H3 |
Eigenschaften von Toluol
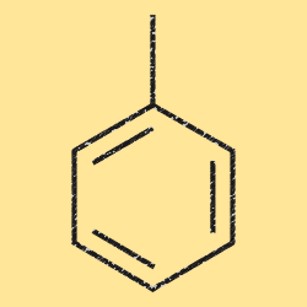
Struktur von Toluol
Toluol hat eine einfache chemische Struktur und besteht aus einem Benzolring mit einer einzelnen daran gebundenen Methylgruppe. Das Molekül ist planar und weist eine delokalisierte elektronische Pi-Bindung auf. Diese einzigartige Struktur macht Toluol zu einem nützlichen Rohstoff bei der Herstellung verschiedener Chemikalien wie Benzol und Xylol sowie bei der Synthese von Pharmazeutika, Farbstoffen und Polymeren.
Toluol-Formel
Die chemische Formel für Toluol lautet C7H8 und gibt die Anzahl und Art der im Molekül vorhandenen Atome an. Diese Formel ist in verschiedenen industriellen Anwendungen wichtig, da sie dabei helfen kann, die physikalischen und chemischen Eigenschaften der Verbindung vorherzusagen, wie z. B. ihren Schmelzpunkt, Siedepunkt und ihre Reaktivität bei verschiedenen chemischen Reaktionen.
Dichte von Toluol g/ml
Die Dichte von Toluol beträgt bei Standardtemperatur und -druck etwa 0,87 Gramm pro Milliliter. Diese relativ geringe Dichte ist auf die geringe Molmasse und kleine Molekülgröße von Toluol zurückzuführen. Die Dichte von Toluol ist in vielen industriellen Prozessen wichtig, da sie die Löslichkeit und Reaktivität der Verbindung bei verschiedenen chemischen Reaktionen beeinflussen kann.
Molmasse von Toluol
Toluol mit der Summenformel C7H8 hat eine Molmasse von etwa 92,14 Gramm pro Mol. Dieser Wert kann durch Addition der Atommassen der Atome, aus denen das Molekül besteht, erhalten werden. Die relativ geringe Molmasse von Toluol macht es zu einer flüchtigen und sehr mobilen Verbindung, was zu seiner Verwendung als Lösungsmittel in verschiedenen industriellen Prozessen beiträgt.
Siedepunkt von Toluol
Toluol hat bei normalem Atmosphärendruck einen Siedepunkt von etwa 110,6 Grad Celsius. Aufgrund seines relativ niedrigen Siedepunkts lässt es sich leicht verdampfen und als Lösungsmittel in einer Vielzahl industrieller Anwendungen verwenden, unter anderem als Verdünnungsmittel in Farben und Beschichtungen sowie bei der Herstellung von synthetischen Fasern und Gummi.
Schmelzpunkt von Toluol
Der Schmelzpunkt von Toluol liegt bei etwa -95 Grad Celsius. Dies macht es bei normaler Temperatur und normalem Druck zu einer Flüssigkeit, kann aber durch Abkühlen unter seinen Schmelzpunkt leicht verfestigt werden. Der niedrige Schmelzpunkt von Toluol ist auf die schwachen intermolekularen Anziehungskräfte zwischen seinen Molekülen zurückzuführen, bei denen es sich hauptsächlich um Van-der-Waals-Kräfte handelt.
Molekulargewicht von Toluol
Das Molekulargewicht von Toluol beträgt 92,14 Gramm pro Mol und wird durch Addition der Atommassen der Atome im Molekül berechnet. Dieser Wert ist in verschiedenen industriellen Anwendungen wichtig, da er die physikalischen und chemischen Eigenschaften der Verbindung beeinflussen kann, einschließlich ihres Siedepunkts, Schmelzpunkts und ihrer Löslichkeit in verschiedenen Lösungsmitteln.
| Aussehen | Farblose Flüssigkeit |
| Spezifisches Gewicht | 0,866 |
| Farbe | Farblos |
| Geruch | Süß, würzig |
| Molmasse | 92,14 g/Mol |
| Dichte | 0,87 g/ml bei 25 °C |
| Fusionspunkt | -95°C |
| Siedepunkt | 110,6°C |
| Blitzpunkt | 4,4°C |
| Löslichkeit in Wasser | 0,052 g/100 ml bei 25 °C |
| Löslichkeit | Löslich in organischen Lösungsmitteln |
| Dampfdruck | 22 mmHg bei 25°C |
| Wasserdampfdichte | 3,1 (Luft = 1) |
| pKa | 44 |
| pH-Wert | Unzutreffend |
Hinweis: Einige Werte können je nach Quelle und Messbedingungen variieren.
Sicherheit und Gefahren von Toluol
Methylbenzol kann bei unsachgemäßer Handhabung mehrere Sicherheitsrisiken bergen. Es ist brennbar und kann mit Luft explosive Gemische bilden. Daher sollte es von Hitze, Funken und Flammen ferngehalten werden. Das Einatmen von Methylbenzoldampf kann zu Reizungen der Atemwege, Kopfschmerzen, Schwindel und Schläfrigkeit führen, und eine chronische Exposition kann zu neurologischen und Verhaltensänderungen führen. Längerer oder wiederholter Hautkontakt kann Dermatitis verursachen. Methylbenzol hat außerdem nachweislich Auswirkungen auf die Fortpflanzung und Entwicklung von Tieren und wird als Karzinogen der Kategorie 2 eingestuft. Beim Umgang mit Methylbenzol sollten geeignete Schutzausrüstung und Belüftung verwendet werden, um Schäden zu minimieren. Exposition gegenüber seinen gefährlichen Auswirkungen.
| Gefahrensymbole | Xn,F |
| Sicherheitsbeschreibung | Von Hitze/Funken/offener Flamme/heißen Oberflächen fernhalten. Explosionsgeschützte Elektro-/Lüftungs-/Beleuchtungsgeräte verwenden. Halten Sie den Behälter fest verschlossen. Dämpfe nicht einatmen. Handschuhe/Schutzkleidung/Augenschutz/Gesichtsschutz tragen. |
| UN-Identifikationsnummern | UN 1294 |
| HS-Code | 2902.2 |
| Gefahrenklasse | 3 |
| Verpackungsgruppe | II |
| Toxizität | Methylbenzol kann Augen-, Nasen- und Rachenreizungen sowie Kopfschmerzen, Schwindel und Schläfrigkeit verursachen. Chronische Exposition kann zu neurologischen und Verhaltensänderungen führen. Längerer oder wiederholter Hautkontakt kann zu Trockenheit, Rissbildung und Dermatitis führen. Methylbenzol hat nachweislich Auswirkungen auf die Fortpflanzung und Entwicklung von Tieren. Es wird von der Internationalen Agentur für Krebsforschung (IARC) als Karzinogen der Kategorie 2 eingestuft. Beim Umgang mit Methylbenzol sollten geeignete Schutzausrüstung und Belüftung verwendet werden, um die Exposition zu minimieren. |
Methoden der Toluol-Synthese
Die chemische Industrie produziert Methylbenzol typischerweise durch eine Reihe von Synthesemethoden, darunter katalytische Reformierung von Naphtha, katalytisches Cracken von Rohölfraktionen und Disproportionierung von Methylbenzol.
Die katalytische Reformierung von Naphtha ist eine der am häufigsten verwendeten Methoden zur Herstellung von Methylbenzol, da dabei ein Gemisch aromatischer Kohlenwasserstoffe entsteht, das abgetrennt und gereinigt werden kann. Bei dem Verfahren wird Naphtha mit einem Katalysator in Gegenwart von Wasserstoff umgesetzt, wodurch eine Mischung aus Aromaten, einschließlich Methylbenzol, entsteht.
Beim katalytischen Cracken von Rohölfraktionen können auch Methylbenzol sowie andere aromatische und nichtaromatische Kohlenwasserstoffe entstehen. Bei diesem Verfahren werden hochsiedende Rohölfraktionen mit einem Katalysator bei hoher Temperatur und hohem Druck umgesetzt. Dadurch werden Moleküle in kleinere Fragmente zerlegt, die getrennt und gereinigt werden können.
Die Disproportionierung von Methylbenzol ist ein Prozess, der Methylbenzol in eine Mischung aus Benzol und Xylolen umwandelt. Die Reaktion wird typischerweise bei erhöhter Temperatur und erhöhtem Druck in Gegenwart eines Katalysators durchgeführt und kann zur Herstellung von hochreinem Benzol und Xylolen für den Einsatz in verschiedenen industriellen Anwendungen verwendet werden.
Verwendung von Toluol
Aufgrund seiner einzigartigen Eigenschaften als flüchtige, farblose Flüssigkeit mit ausgeprägtem Geruch findet Methylbenzol vielfältige industrielle und kommerzielle Verwendungsmöglichkeiten. Zu den Hauptanwendungen gehören:
- Lösungsmittelhersteller verwenden Toluol häufig als Lösungsmittel bei der Herstellung von Farben, Beschichtungen, Klebstoffen und anderen Produkten. Es wird wegen seiner Fähigkeit, ein breites Spektrum organischer Verbindungen aufzulösen, sowie seiner relativ geringen Toxizität und hohen Verdunstungsrate geschätzt.
- Toluol verbessert die Leistung und Effizienz von Verbrennungsmotoren, weshalb es als hochoktaniger Bestandteil in Benzin verwendet wird.
- Hersteller verwenden Toluol als wichtiges Zwischenprodukt bei der Herstellung verschiedener Chemikalien, darunter Benzol, Xylol und verschiedene andere aromatische Verbindungen. Diese Chemikalien werden bei der Herstellung von Kunststoffen, synthetischen Fasern, Gummi und anderen Materialien verwendet.
- In einigen medizinischen und pharmazeutischen Anwendungen wird Toluol verwendet, unter anderem als Bestandteil bestimmter topischer Medikamente und als Lösungsmittel für bestimmte medizinische Verbindungen.
- Aufgrund seiner Fähigkeit, eine Vielzahl organischer Verbindungen aufzulösen und mit ihnen zu reagieren, verwenden Forscher Toluol als Lösungsmittel und Reagenz in verschiedenen Laborforschungsanwendungen.
Fragen:
Toluol zu Benzylalkohol
Durch einen mehrstufigen Prozess wird Methylbenzol in Benzylalkohol umgewandelt. Ein gängiger Ansatz umfasst die folgenden Schritte:
- Oxidation von Methylbenzol zu Benzylchlorid: Methylbenzol kann mit Chlorgas und einem Katalysator wie Eisen- oder Aluminiumchlorid zu Benzylchlorid oxidiert werden. Bei dieser Reaktion wird ein Wasserstoffatom an der Methylgruppe von Methylbenzol durch ein Chloratom ersetzt.
- Hydrolyse von Benzylchlorid zu Benzylalkohol: Benzylchlorid kann mit einer wässrigen Lösung von Natriumhydroxid zu Benzylalkohol hydrolysiert werden. Bei dieser Reaktion wird die Chloridgruppe von Benzylchlorid durch eine Hydroxylgruppe ersetzt.
- Reinigung von Benzylalkohol: Der resultierende Benzylalkohol kann durch Destillation oder andere Methoden gereinigt werden, um alle Verunreinigungen zu entfernen.
Toluol zu Benzaldehyd
Die Umwandlung von Methylbenzol in Benzaldehyd kann durch einen mehrstufigen Prozess erfolgen. Ein gängiger Ansatz umfasst die folgenden Schritte:
- Oxidation von Methylbenzol zu Benzylalkohol: Methylbenzol kann mit einem Oxidationsmittel wie Kaliumpermanganat oder Chromsäure zu Benzylalkohol oxidiert werden. Bei dieser Reaktion wird ein Wasserstoffatom an der Methylgruppe von Methylbenzol durch eine Hydroxylgruppe ersetzt, um Benzylalkohol zu bilden.
- Oxidation von Benzylalkohol zu Benzaldehyd: Benzylalkohol kann mit einem Oxidationsmittel wie Kaliumpermanganat oder Natriumchlorit weiter zu Benzaldehyd oxidiert werden. Bei dieser Reaktion wird die Hydroxylgruppe am Benzylalkohol entfernt, um eine Carbonylgruppe am Benzaldehyd zu bilden.
- Reinigung von Benzaldehyd: Der resultierende Benzaldehyd kann durch Destillation oder andere Methoden gereinigt werden, um alle Verunreinigungen zu entfernen.
