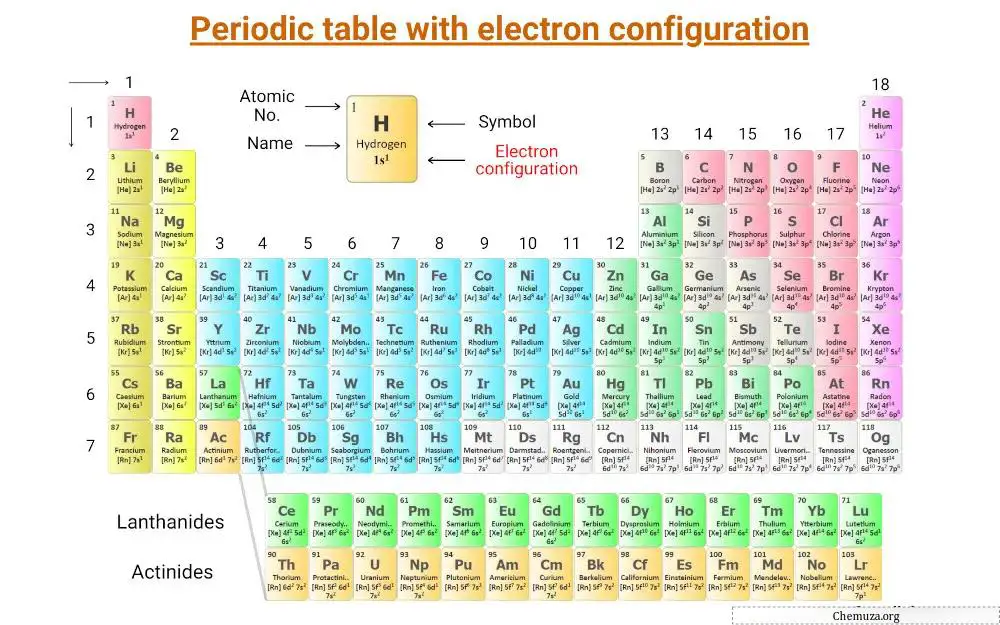
Es handelt sich um ein Periodensystem , in dem die elektronische Konfiguration der Elemente angegeben ist.
Sie können hier auch HD-Bilder herunterladen.
Lassen Sie uns die elektronischen Konfigurationen der Elemente weiter untersuchen.
Was ist eine elektronische Konfiguration?
Unter elektronischer Konfiguration versteht man die Anordnung der Elektronen in einem Atom .
Elektronen sind winzige negativ geladene Teilchen, die den positiv geladenen Kern eines Atoms umkreisen.
Die elektronische Konfiguration eines Atoms bestimmt seine chemischen und physikalischen Eigenschaften wie seine Reaktivität, Leitfähigkeit und seinen Schmelzpunkt.
Die Anordnung der Elektronen in einem Atom wird durch seine Energieniveaus (auch Schalen genannt) und die spezifischen Unterschalen innerhalb dieser Schalen bestimmt.
Die elektronische Konfiguration wird normalerweise mithilfe einer Notation dargestellt, die die Anzahl der Elektronen in jeder Schale und Unterschale angibt und bestimmten Regeln folgt, die auf den Prinzipien der Quantenmechanik basieren.
Was sind Schalen (n) und Unterschalen (s, p, d, f)?
Hülle: Die Hülle ist die Umlaufbahn, in der Elektronen um den Kern eines Atoms kreisen.
Jeder Schale wird eine Nummer (n) zugewiesen, beginnend mit eins für die erste Schale und zunehmend mit jeder weiteren Schale.
Die erste Schale kann nur maximal 2 Elektronen aufnehmen, während die zweite Schale bis zu 8 Elektronen aufnehmen kann und die nachfolgenden Schalen noch mehr aufnehmen können.
Unterschale (oder Orbitale): Innerhalb jeder Schale gibt es verschiedene Unterschalen, die mit Buchstaben wie s, p, d und f gekennzeichnet sind.
Die s-Unterschale kann maximal 2 Elektronen aufnehmen, die p-Unterschale kann bis zu 6 Elektronen aufnehmen, die d-Unterschale kann bis zu 10 Elektronen aufnehmen und die f-Unterschale kann bis zu 14 Elektronen aufnehmen. [1]
Die Schichten und Unterschichten eines Atoms bestimmen seine elektronische Konfiguration, die wiederum seine chemischen und physikalischen Eigenschaften bestimmt.
Elektronische Konfiguration von Elementen (Liste)
Hier ist die Liste der elektronischen Konfigurationen der ersten 20 Elemente des Periodensystems.
| Ordnungszahl | Element | Elektronische Konfiguration |
| 1 | Wasserstoff (H) | 1s 1 |
| 2 | Helium (He) | 1s 2 |
| 3 | Lithium (Li) | [Es] 2s 1 |
| 4 | Beryllium (Be) | [Er] 2s 2 |
| 5 | Bor (B) | [Es] 2s 2 2p 1 |
| 6 | Kohlenstoff (C) | [Er] 2s 2 2p 2 |
| 7 | Stickstoff (N) | [Er] 2s 2 2p 3 |
| 8 | Sauerstoff (O) | [Er] 2s 2 2p 4 |
| 9 | Fluorit (F) | [Es] 2s 2 2p 5 |
| zehn | Neon (Ne) | [Er] 2s 2 2p 6 |
| 11 | Natrium (Na) | [Do] 3s 1 |
| 12 | Magnesium (Mg) | [Do] 3s 2 |
| 13 | Aluminium (Al) | [Do] 3s 2 3p 1 |
| 14 | Silizium (Si) | [Nicht] 3s 2 3p 2 |
| 15 | Phosphor (P) | [Nicht] 3s 2 3p 3 |
| 16 | Schwefel (S) | [Do] 3s 2 3p 4 |
| 17 | Chlor (Cl) | [Nicht] 3s 2 3p 5 |
| 18 | Argon (Ar) | [Do] 3s 2 3p 6 |
| 19 | Kalium (K) | [Ar] 4s 1 |
| 20 | Kalzium (Ca) | [Ar] 4s 2 |
