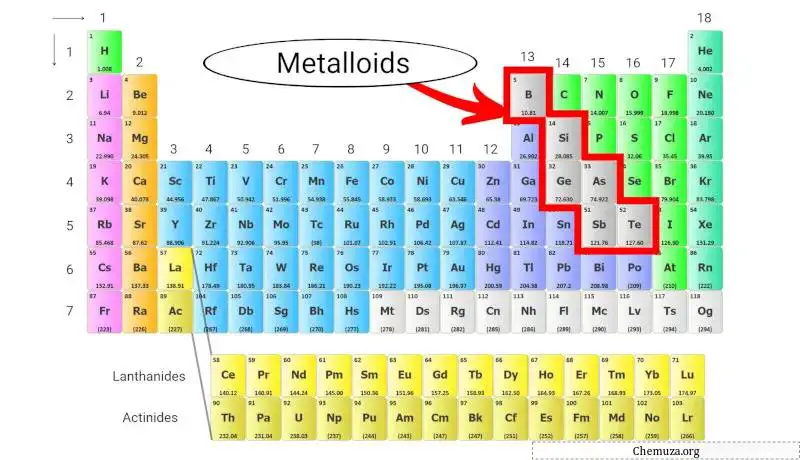
Metalloide sind eine Gruppe von Elementen im Periodensystem , die sowohl metallische als auch nichtmetallische Eigenschaften besitzen. Sie werden auch Halbmetalle genannt.
Sie haben einige Eigenschaften von Metallen, wie zum Beispiel die Fähigkeit, Strom und Wärme zu leiten, haben aber auch Eigenschaften von Nichtmetallen, wie zum Beispiel, dass sie spröde und nicht glänzend sind.
Lassen Sie uns Metalloide weiter erforschen.
Was sind Metalloide?
Metalloide sind eine Gruppe von Elementen im Periodensystem, deren Eigenschaften zwischen Metallen und Nichtmetallen liegen. Sie werden manchmal auch „Halbmetalle“ genannt.

Zu den Metalloiden gehören Bor , Silizium , Germanium , Arsen , Antimon und Tellur .
Metalloide haben sowohl metallische als auch nichtmetallische Eigenschaften. Beispielsweise können sie wie Metalle bis zu einem gewissen Grad Elektrizität leiten, sind aber nicht so gute Leiter wie Metalle.
Sie haben auch einen gewissen metallischen Glanz und können duktil und formbar sein, wenn auch nicht so stark wie reine Metalle. Darüber hinaus können sie wie Nichtmetalle kovalente Bindungen eingehen, aber auch ionische Bindungen mit Metallen eingehen.
Diese Elemente sind in verschiedenen Branchen wichtig, darunter auch in der Elektronikbranche, wo sie zur Herstellung von Halbleitern und anderen elektronischen Bauteilen verwendet werden. [1]
Wie viele Metalloide gibt es im Periodensystem?
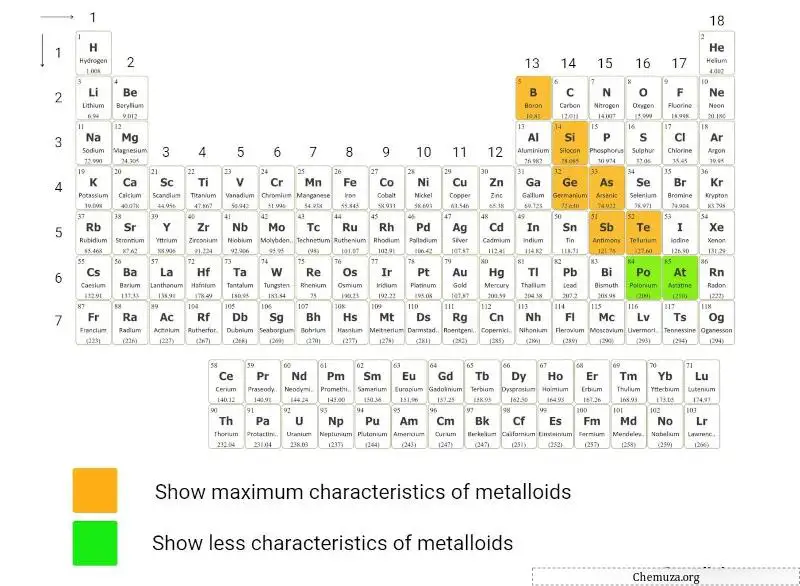
Es gibt 6 allgemein bekannte Metalloide im Periodensystem.
Sie sind;
- Bor
- Silizium
- Germanium
- Arsen
- Antimon und
- Tellur
Aber das stimmt nicht ganz. Denn auch Polonium und Astat weisen einige Eigenschaften von Metalloiden auf.
Werden Polonium und Astat als Metalloide betrachtet?
Die Einstufung von Polonium und Astat als Metalloide ist unter Forschern umstritten.
Einige Forscher behaupten, dass Polonium eher metallische Eigenschaften aufweist, während Astatin eher nichtmetallische Eigenschaften aufweist, ähnlich wie Halogene . [2]
Daher gibt es keine allgemein akzeptierte Definition von Metalloiden. Verschiedene Forscher können sie anhand verschiedener Kriterien definieren, darunter Dichte, physikalische oder chemische Eigenschaften.
Darüber hinaus ist die Klassifizierung von Polonium und Astat aufgrund ihrer synthetischen Natur und extrem kurzen Halbwertszeiten noch komplizierter.
Derzeit umfasst die weithin akzeptierte Liste der Metalloide oder Halbmetalle im Periodensystem sechs Elemente.
Laufende Forschung und ein sich weiterentwickelndes Verständnis der Eigenschaften der Elemente könnten jedoch in Zukunft zu Änderungen in der Klassifizierung von Polonium und Astat führen.
Halbleitereigenschaften von Metalloiden
Metalloide sind Elemente mit Halbleitereigenschaften. Dies bedeutet, dass sie eine mittlere Leitfähigkeit zwischen Metallen und Nichtmetallen aufweisen.
Metalloide sind keine guten Leiter wie Metalle, aber ihre Leitfähigkeit ist höher als die von Nichtmetallen.
Metalloide werden Halbleiter genannt, weil ihre Energiebandlücke zwischen der von Leitern und Isolatoren liegt.
Lassen Sie uns dies anhand einfacher Bilder verstehen.
Treiber:
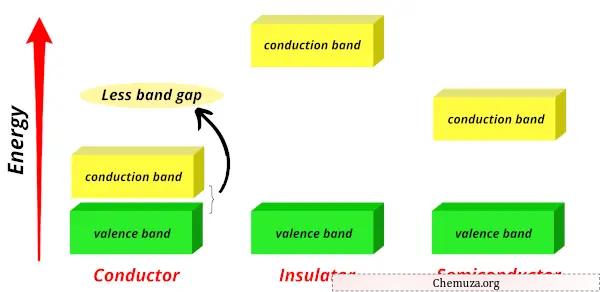
In Leitern liegen das Valenzband und das Leitungsband sehr nahe beieinander, sodass freie Elektronen problemlos vom Valenzband in das Leitungsband gelangen können.
Isolatoren:
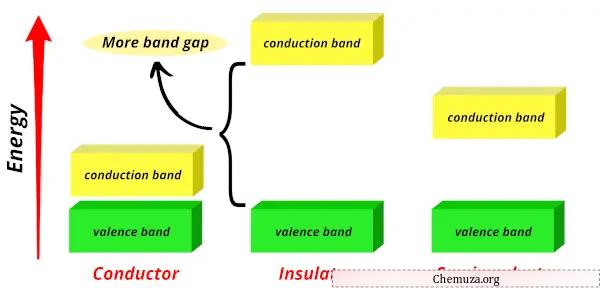
In Isolatoren ist die Bandlücke sehr groß, sodass die Elektronen viel Energie benötigen, um vom Valenzband in das Leitungsband zu gelangen.
Halbleiter:
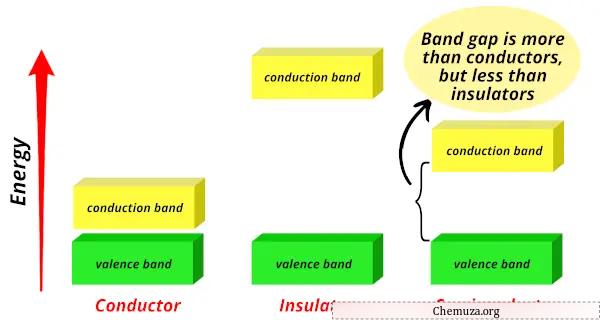
Im Gegensatz dazu liegt die Bandlücke von Halbleitern dazwischen, was bedeutet, dass Elektronen weniger Energie als die von Isolatoren, aber mehr Energie als die von Leitern benötigen, um vom Valenzband zur Bandlücke zu gelangen. der Leitung.
Daher werden Elemente, deren Energiebandlücke zwischen der von Leitern und Isolatoren liegt, als Halbleiter klassifiziert.
Verwendung von Metalloiden
Metalloide finden vielfältige Einsatzmöglichkeiten in einer Vielzahl von Branchen, von der Elektronik über die Medizin bis hin zur Fertigung. Hier sind einige Verwendungsmöglichkeiten von Metalloiden.
- Bor wird zur Herstellung von hitzebeständigem Glas für Gegenstände wie Küchenutensilien und Laborgeräte verwendet. [3]
- Silizium ist eines der am häufigsten verwendeten Metalloide in der Elektronik. Es wird zur Herstellung von Computerchips, Mobiltelefonen und anderen elektronischen Geräten verwendet.
- Antimon wird zur Herstellung bestimmter Arten von Batterien und Geschossen verwendet. [4]
- Aus Germanium werden Speziallinsen für Infrarotkameras hergestellt, die in Nachtsichtbrillen zum Einsatz kommen. [5]
- Tellur wird zur Herstellung bestimmter Arten von Solarmodulen verwendet, die Sonnenlicht in Strom umwandeln können. [6]
- Metalloide werden auch bei der Herstellung von Legierungen verwendet, bei denen es sich um Metallmischungen handelt. Beispielsweise wird Blei Arsen zugesetzt, um es härter zu machen, und Bor wird Stahl zugesetzt, um es fester zu machen.
- Einige Metalloide wie Silizium und Germanium können zur Herstellung von Halbleitern für elektronische Geräte wie Computer und Mobiltelefone verwendet werden.
Zusammenfassung
Metalloide sind eine Gruppe von Elementen mit sowohl metallischen als auch nichtmetallischen Eigenschaften. Dazu gehören Bor, Silizium, Germanium, Arsen, Antimon und Tellur, wobei auch Polonium und Astat einige Eigenschaften von Metalloiden aufweisen.
Metalloide haben halbleitende Eigenschaften, was bedeutet, dass sie eine Leitfähigkeit haben, die zwischen Metallen und Nichtmetallen liegt.
Sie werden in verschiedenen Branchen eingesetzt, darunter in der Elektronik, Medizin und Fertigung. Bor wird für hitzebeständiges Glas, Silizium für Computerchips, Arsen für einige Medikamente, Antimon für Batterien und Kugeln, Germanium für Infrarotkameraobjektive und Tellur für Sonnenkollektoren verwendet. Einige Metalloide können auch zur Herstellung von Halbleitern für elektronische Geräte verwendet werden.
