Zinkcitrat (C12H10O14Zn3) ist eine Verbindung mit drei Zinkionen, die an Citratmoleküle gebunden sind. Aufgrund seiner potenziellen gesundheitlichen Vorteile, wie der Unterstützung des Immunsystems und der Verdauung, wird es häufig in Nahrungsergänzungsmitteln verwendet.
| IUPAC-Name | Trizink-Dicitrat |
| Molekularformel | C12H10O14Zn3 |
| CAS-Nummer | 546-46-3 |
| Synonyme | Zitronensäure, Zinksalz; Trizinkcitrat; Zinktricitrat; Trizinksalz der Zitronensäure |
| InChI | InChI=1S/2C6H8O7.3Zn/c2 7-3(8)1-6(13.5(11)12)2-4(9)10;;;/h2 13H,1-2H2,(H,7, 8) (H,9,10)(H,11,12);;;/q;;3*+2/p-6 |
Eigenschaften von Zinkcitrat
Zinkcitrat-Formel
Die chemische Formel von Trizinkcitrat lautet C12H10O14Zn3. Damit ist die Anordnung von 12 Kohlenstoffatomen, 10 Wasserstoffatomen, 14 Sauerstoffatomen und 3 Zinkatomen in der Verbindung gemeint.
Molmasse von Zinkcitrat
Die Molmasse von Trizinkcitrat wird durch Addition der Atommassen seiner Bestandteile berechnet. Es wiegt etwa 574,38 g/mol.
Siedepunkt von Zinkcitrat
Der Siedepunkt von Trizinkcitrat bezeichnet die Temperatur, bei der es vom flüssigen in den gasförmigen Zustand übergeht. Aufgrund seiner komplexen Natur zersetzt sich Trizinkcitrat jedoch typischerweise, bevor es einen bestimmten Siedepunkt erreicht.
Schmelzpunkt von Zinkcitrat
Der Schmelzpunkt von Trizinkcitrat, die Temperatur, bei der es vom festen in den flüssigen Zustand übergeht, liegt im Allgemeinen zwischen 190 °C und 200 °C. Dieser Temperaturbereich kann je nach Faktoren wie Verunreinigungen und Kristallstruktur leicht variieren.
Dichte von Zinkcitrat g/ml
Die Dichte von Trizinkcitrat, die seine Masse pro Volumeneinheit misst, beträgt etwa 1,98 g/ml. Diese Dichte weist darauf hin, dass Trizinccitrat relativ dicht und kompakt ist.
Molekulargewicht von Zinkcitrat
Das Molekulargewicht von Trizinkcitrat wird durch Addition der Atomgewichte seiner Bestandteile bestimmt. Mit der Summenformel C12H10O14Zn3 hat es ein Molekulargewicht von etwa 574,38 g/mol.
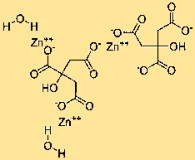
Struktur von Zinkcitrat
Trizinkcitrat hat eine komplexe Struktur, in der drei Zinkionen mit Citratmolekülen koordiniert sind. Diese Anordnung bildet ein dreidimensionales Netzwerk, das durch chemische Bindungen zusammengehalten wird. Die genaue Anordnung der Atome innerhalb der Struktur trägt zu ihren Eigenschaften und ihrem Verhalten bei.
Löslichkeit von Zinkcitrat
Die Löslichkeit von Trizinkcitrat, die seine Fähigkeit definiert, sich in einem Lösungsmittel wie Wasser aufzulösen, wird von verschiedenen Faktoren beeinflusst, darunter Temperatur und pH-Wert. Im Allgemeinen ist Trizinkcitrat wasserlöslich und seine Löslichkeit nimmt mit zunehmendem Säuregehalt zu.
| Aussehen | weißes kristallines Pulver |
| Spezifisches Gewicht | 1,98 g/ml |
| Farbe | Weiß |
| Geruch | Geruchlos |
| Molmasse | 574,38 g/Mol |
| Dichte | 1,98 g/ml |
| Fusionspunkt | 190°C – 200°C |
| Siedepunkt | Zersetzt sich, bevor ein deutlicher Siedepunkt erreicht wird |
| Blitzpunkt | Unzutreffend |
| Löslichkeit in Wasser | Löslich |
| Löslichkeit | In Wasser löslich |
| Dampfdruck | Nicht verfügbar |
| Wasserdampfdichte | Nicht verfügbar |
| pKa | Nicht verfügbar |
| pH-Wert | Es kommt auf die Lösung an |
Sicherheit und Gefahren von Zinkcitrat
Trizincitrat gilt im Allgemeinen als sicher, wenn es in empfohlenen Dosierungen in Nahrungsergänzungsmitteln verwendet wird. Allerdings kann ein übermäßiger Verzehr zu Nebenwirkungen wie Magenbeschwerden oder Magen-Darm-Problemen führen. Außerhalb der Reichweite von Kindern aufbewahren und Kontakt mit Augen oder Haut vermeiden. Im Falle einer versehentlichen Einnahme oder einer unerwünschten Reaktion suchen Sie umgehend einen Arzt auf. Obwohl Trizinkcitrat nicht sehr giftig ist, ist es wichtig, es verantwortungsvoll zu verwenden und die empfohlenen Richtlinien zu befolgen, um potenzielle Gefahren zu vermeiden.
| Gefahrensymbole | Unzutreffend |
| Sicherheitsbeschreibung | Gilt allgemein als sicher, wenn es in empfohlenen Dosierungen in Nahrungsergänzungsmitteln verwendet wird. Übermäßiger Verzehr kann zu Magenbeschwerden oder Magen-Darm-Problemen führen. |
| UN-Identifikationsnummern | Unzutreffend |
| HS-Code | Unzutreffend |
| Gefahrenklasse | Nicht als gefährlich eingestuft |
| Verpackungsgruppe | Unzutreffend |
| Toxizität | Nicht sehr giftig; Befolgen Sie die empfohlenen Richtlinien für die Verwendung und Dosierung. |
Bitte beachten Sie, dass bestimmte Eigenschaften wie Gefahrensymbole, UN-Kennzeichnungen, HS-Code und Verpackungsgruppe möglicherweise nicht für Trizinkcitrat gelten, da es bei seinen üblichen Verwendungszwecken im Allgemeinen nicht als gefährlich eingestuft wird.
Schreiben Sie Methoden zur Synthese von Zinkcitrat
Trizinkcitrat kann auf verschiedene Weise synthetisiert werden. Ein gängiger Ansatz besteht darin, Zitronensäure mit Zinkoxid oder Zinkcarbonat in einer wässrigen Lösung umzusetzen. Bei der Reaktion entstehen als Nebenprodukte Trizinkcitrat und Wasser. Eine andere Methode verwendet Zitronensäure und Zinkacetat als Rohstoffe und liefert mit Essigsäure die gewünschte Verbindung. Diese Reaktionen finden im Allgemeinen unter kontrollierten Temperatur- und pH-Bedingungen statt, um eine optimale Produktbildung sicherzustellen.
Eine andere Methode ist die Neutralisationsreaktion, bei der Zitronensäure mit Zinkhydroxid oder Zinkcarbonat neutralisiert wird, was zur Bildung von Trizinkcitrat und Wasser führt. Diese Methode erfordert eine sorgfältige Kontrolle der Reaktantenverhältnisse, um das gewünschte Produkt zu erhalten.
Bei Fällungsmethoden wird eine Lösung eines Zinksalzes (z. B. Zinksulfat) mit einer Citrationen enthaltenden Lösung gemischt. Dabei entsteht unlösliches Trizinkcitrat, das anschließend abgetrennt und gereinigt werden kann.
Insgesamt unterstreichen diese Synthesemethoden die Bedeutung präziser Reagenzienverhältnisse und Reaktionsbedingungen, um effizient hochwertiges Trizinkcitrat zu erhalten.
Verwendung von Zinkcitrat
Trizinkcitrat findet aufgrund seiner wohltuenden Eigenschaften vielseitige Anwendungsmöglichkeiten. Einige häufige Verwendungszwecke sind:
- Nahrungsergänzungsmittel: Nahrungsergänzungsmittel verwenden Trizinkcitrat, da es die Immunfunktion unterstützen, die Wundheilung unterstützen und eine gesunde Haut fördern kann.
- Mundgesundheitsprodukte: Zahnpasta- und Mundwasserformulierungen enthalten Trizinkcitrat als Bestandteil. Seine antimikrobiellen Eigenschaften helfen, Plaquebildung zu verhindern und die Mundhygiene aufrechtzuerhalten.
- Körperpflegeprodukte: Kosmetika und Hautpflegeprodukte enthalten Trizinccitrat, um die Talgproduktion zu regulieren und Hautunreinheiten zu minimieren.
- Pharmazeutische Formulierungen: Einige Medikamente enthalten Trizinkcitrat wegen seiner Rolle bei der Nährstoffaufnahme und der Unterstützung der allgemeinen Gesundheit.
- Lebensmittel und Getränke: Lebensmittelzusatzstoffe werden in verschiedenen Produkten als Nährstoffverstärker und Säureregulatoren eingesetzt.
- Metalloberflächenbehandlung: Industrielle Anwendungen verwenden Trizinkcitrat zur Behandlung von Metalloberflächen und verbessern so die Korrosionsbeständigkeit.
- Verzinkung: Trizinkcitrat trägt zum Verzinkungsprozess bei, verhindert Korrosion und verlängert die Lebensdauer von Metallgegenständen.
- Zinkionenquelle: Verschiedene chemische und biologische Forschungsstudien nutzen es als Quelle für Zinkionen.
- Textilindustrie: Bei der Textilveredelung wird Trizinkcitrat verwendet, da es Stoffen antimikrobielle Eigenschaften verleiht.
- Wasseraufbereitung: Bei der Wasseraufbereitung hilft es, Verunreinigungen wie Schwermetalle auszufällen und zu entfernen.
- Landwirtschaftliche Verwendung: Trizinccitrat kann als Blattspray verwendet werden, um Pflanzen mit Zn zu ergänzen.
Diese Anwendungen unterstreichen den breiten Nutzen von Trizinkcitrat in verschiedenen Branchen aufgrund seiner vielfältigen Eigenschaften und potenziellen gesundheitlichen Vorteile.
Fragen:
F: Wofür werden Calciumcitrat, Magnesium und Zink verwendet?
A: Diese Kombination unterstützt die Knochengesundheit, die Muskelfunktion und das Immunsystem, wobei jedes Element zu verschiedenen physiologischen Prozessen beiträgt.
F: Was ist Zinkcitrat?
A: Trizinkcitrat ist eine Verbindung aus Zink und Zitronensäure, die aufgrund ihrer potenziellen gesundheitlichen Vorteile, wie z. B. der Unterstützung des Immunsystems, häufig in Nahrungsergänzungsmitteln verwendet wird.
F: Was ist der Unterschied zwischen Zinkcitrat und Zinkchelat?
A: Trizinkcitrat entsteht durch Bindung von Zn an Zitronensäure, während bei Zn-Chelat das Zn an einen Chelatbildner gebunden wird, was die Absorption erleichtert.
F: Wie verwende ich Zinkcitratpulver?
A: Mischen Sie im Allgemeinen die empfohlene Dosis Trizinkcitratpulver mit Wasser oder einem Getränk und befolgen Sie dabei die Anweisungen auf dem Produktetikett.
F: Werden die Kalzium-, Magnesium- und Zinkpräparate von Nature Made mit Kalziumcitrat hergestellt?
A: Nahrungsergänzungsmittel von Nature Made können Calciumcitrat enthalten, es wird jedoch empfohlen, zur Bestätigung das Etikett oder die Produktinformationen zu überprüfen.
F: Ist Zinkcitrat synthetisch?
A: Trizinkcitrat kann synthetisiert werden, es kommt aber auch natürlicherweise in bestimmten Lebensmitteln vor und kann aus diesen gewonnen werden.
F: Woher kommt Zinkcitrat?
A: Trizinkcitrat kann aus natürlichen Quellen gewonnen oder durch chemische Reaktionen unter Beteiligung von Zn-Verbindungen und Zitronensäure synthetisiert werden.
F: Ist Zinkcitrat-Trihydrat biologisch?
A: Trizinkcitrat-Trihydrat kann entweder synthetisiert oder aus natürlichen Quellen gewonnen werden, wird jedoch nicht als „biologisch“ im Sinne der ökologischen Landwirtschaftspraxis eingestuft.
F: Ist Zinkcitrat gut?
A: Trizinccitrat gilt bei bestimmungsgemäßer Anwendung als vorteilhaft für verschiedene Aspekte der Gesundheit, einschließlich der Unterstützung des Immunsystems, der Hautgesundheit und des allgemeinen Wohlbefindens.
