Boroxid (B2O3) ist eine Verbindung, die durch die chemische Bindung von Bor und Sauerstoff entsteht. Aufgrund seines hohen Schmelzpunktes wird es bei der Herstellung von Glas und Keramik verwendet.
| IUPAC-Name | Boroxid |
| Molekularformel | B2O3 |
| CAS-Nummer | 1303-86-2 |
| Synonyme | Tribortrioxid, Boroxid, Bor(III)-oxid |
| InChI | InChI=1S/B2O3/c3-1-5-2(4)6-1 |
Eigenschaften von Boroxid
Boroxid-Formel
Die chemische Formel für Boroxid lautet B2O3. Es gibt das Verhältnis von Boratomen zu Sauerstoffatomen in der Verbindung an. Die Indexzahlen geben an, dass in jedem Boroxidmolekül zwei Boratome und drei Sauerstoffatome vorhanden sind.
Molmasse von Boroxid
Die Molmasse von Boroxid kann durch Addition der Atommassen seiner Bestandteile berechnet werden. Bor hat eine Atommasse von 10,81 g/mol, während Sauerstoff eine Atommasse von 16,00 g/mol hat. Durch Multiplikation der Atommassen mit der jeweiligen Atomzahl und deren Addition ergibt sich die Molmasse von Boroxid zu 69,62 g/mol.
Siedepunkt von Boroxid
Boroxid hat einen hohen Siedepunkt von etwa 1.860 Grad Celsius. Das bedeutet, dass bei normalem Atmosphärendruck erhebliche Energie benötigt wird, um Boroxid vom flüssigen in den gasförmigen Zustand umzuwandeln.
Schmelzpunkt von Boroxid
Der Schmelzpunkt von Boroxid liegt bei etwa 450 Grad Celsius. Bei dieser Temperatur geht festes Boroxid in einen flüssigen Zustand über. Aufgrund seines relativ niedrigen Schmelzpunkts eignet es sich für verschiedene industrielle Anwendungen.
Dichte von Boroxid g/ml
Boroxid hat eine Dichte von etwa 2,46 g/ml. Unter Dichte versteht man die Masse pro Volumeneinheit eines Stoffes. Die Dichte von Boroxid weist darauf hin, dass es relativ dicht ist und in den meisten Flüssigkeiten fließen kann.
Molekulargewicht von Boroxid
Das Molekulargewicht von Boroxid, auch Molmasse genannt, beträgt 69,62 g/mol. Dieser Wert stellt die Masse eines Mols der Verbindung dar und ist nützlich für die Berechnung der Menge an Boroxid in einer bestimmten Probe.
Struktur von Boroxid
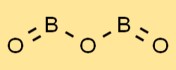
Boroxid hat eine einzigartige Struktur mit einer Reihe trigonaler planarer BO3-Einheiten. Die Boratome sind von drei dreieckig angeordneten Sauerstoffatomen umgeben. Diese Anordnung verleiht Boroxid seine charakteristischen Eigenschaften und Stabilität.
Löslichkeit von Boroxid
Boroxid ist in Wasser und den meisten organischen Lösungsmitteln unlöslich. Seine Löslichkeit ist in Säuren wie Schwefelsäure und Salzsäure begrenzt. Diese geringe Löslichkeit trägt zu seiner Stabilität und Nützlichkeit in verschiedenen Anwendungen bei, beispielsweise in der Glas- und Keramikproduktion.
| Aussehen | Weißer Feststoff |
| Spezifisches Gewicht | 2,46 g/ml |
| Farbe | Weiß |
| Geruch | Geruchlos |
| Molmasse | 69,62 g/Mol |
| Dichte | 2,46 g/ml |
| Fusionspunkt | 450°C |
| Siedepunkt | 1860°C |
| Blitzpunkt | Unzutreffend |
| Löslichkeit in Wasser | Unlöslich |
| Löslichkeit | Begrenzte Löslichkeit in Säuren wie Schwefelsäure und Salzsäure |
| Dampfdruck | Unzutreffend |
| Wasserdampfdichte | Unzutreffend |
| pKa | Unzutreffend |
| pH-Wert | Unzutreffend |
Bitte beachten Sie, dass einige Eigenschaften wie Flammpunkt, Dampfdruck, Dampfdichte, pKa und pH-Wert nicht anwendbar sind oder für Boroxid nicht angegeben wurden.
Sicherheit und Gefahren von Boroxid
Boroxid wirft bestimmte Sicherheits- und Gefahrenaspekte auf. Direkter Kontakt mit Boroxidpulver oder -staub kann zu Reizungen der Haut, Augen und Atemwege führen. Es ist wichtig, vorsichtig damit umzugehen und geeignete persönliche Schutzausrüstung wie Handschuhe und Schutzbrillen zu verwenden. Das Einatmen von Boroxidpartikeln kann zu Reizungen der Atemwege führen. Daher ist es ratsam, in gut belüfteten Bereichen zu arbeiten. Im Falle einer versehentlichen Einnahme sollte sofort ein Arzt aufgesucht werden. Boroxid ist nicht brennbar und hat keinen Flammpunkt. Wie bei jeder chemischen Substanz wird empfohlen, die Richtlinien zur ordnungsgemäßen Handhabung und Lagerung zu befolgen, um eine sichere Verwendung zu gewährleisten.
| Gefahrensymbole | Nicht klassifiziert |
| Sicherheitsbeschreibung | Kontakt mit Haut und Augen vermeiden. In einem gut belüfteten Bereich verwenden. Schutzausrüstung tragen. |
| UN-Identifikationsnummern | Unzutreffend |
| HS-Code | 2810.00.2000 |
| Gefahrenklasse | Nicht klassifiziert |
| Verpackungsgruppe | Unzutreffend |
| Toxizität | Geringe bis mäßige Toxizität. Kann bei Kontakt oder Einatmen Reizungen verursachen. |
Bitte beachten Sie, dass Boroxid keine Gefahrensymbole, UN-Kennzeichnung, Gefahrenklasse oder Verpackungsgruppe trägt. Es ist wichtig, bei der Handhabung und Verwendung von Boroxid die allgemeinen Sicherheitsrichtlinien und -praktiken zu befolgen, um das Risiko einer Exposition zu minimieren und eine sichere Verwendung zu gewährleisten.
Methoden zur Synthese von Boroxid
Verschiedene Methoden ermöglichen die Synthese von Boroxid. Ein weit verbreiteter Ansatz besteht darin, elementares Bor in Gegenwart von Sauerstoff oder Luft zu erhitzen, um Boroxid zu erzeugen. Eine andere Methode besteht darin, Borhalogenide wie Bortrichlorid (BCl3) oder Bortribromid (BBr3) mit Wasser zur Reaktion zu bringen, was zur Bildung von Boroxid führt.
Darüber hinaus können borhaltige Verbindungen wie Bornitrid oder Bortrisulfid mit Wasser hydrolysiert werden, um Boroxid zu erzeugen. Bei der thermischen Zersetzung von Boraten wie Natriumborat oder Borax entsteht unter Hitzeeinwirkung ebenfalls Boroxid.
Es ist wichtig zu beachten, dass die Wahl einer bestimmten Synthesemethode von der gewünschten Reinheit, Menge und Anwendung des Boroxids abhängt. Jede Methode hat Vorteile und kann für unterschiedliche Situationen geeignet sein.
Verwendung von Boroxid
Boroxid findet vielfältige Anwendungen in verschiedenen Branchen. Hier sind einige seiner Verwendungsmöglichkeiten:
- Glas- und Keramikherstellung: Boroxid ist ein wichtiger Bestandteil bei der Herstellung von Glas und Keramik. Es verleiht Glasprodukten wünschenswerte Eigenschaften wie Hitzebeständigkeit, Transparenz und Haltbarkeit.
- Flammschutzmittel: Hersteller verwenden Boroxid als Flammschutzmittel in Materialien wie Textilien, Kunststoffen und Holzprodukten. Boroxid verringert die Entflammbarkeit dieser Materialien und sorgt so für mehr Sicherheit.
- Borosilikatglas: Boroxid spielt eine wichtige Rolle als Bestandteil von Borosilikatglas, das für seine geringe Wärmeausdehnung und hohe Hitzebeständigkeit bekannt ist. Die Industrie verwendet diese Art von Glas in Laborgeräten, Küchenutensilien und hochwertigen optischen Geräten.
- Spezialfasern: Bei der Herstellung von Spezialfasern, einschließlich Borfasern und Bornitridfasern, wird Boroxid verwendet. Diese Fasern verfügen über außergewöhnliche mechanische und thermische Eigenschaften und eignen sich daher für die Luft- und Raumfahrt-, Automobil- und High-Tech-Industrie.
- Borchemikalien: Boroxid dient als Vorstufe für die Synthese verschiedener Borchemikalien wie Borate und Borhydride. Diese Chemikalien finden Anwendung in der Landwirtschaft, Pharmazie und Energiespeichersystemen.
- Flussmittel und Lötmittel: Boroxid senkt den Schmelzpunkt von Materialien und verbessert deren Fließfähigkeit, was es zu einem wirksamen Flussmittel in metallurgischen Prozessen macht. Als Lötmittel verbessert es die Verbindung von Metalloberflächen.
- Katalysatoren: Chemische Reaktionen profitieren von Boroxidkatalysatoren, da sie gewünschte Reaktionen fördern und die Reaktionsgeschwindigkeit erhöhen.
- Halbleiterindustrie: Boroxid spielt eine entscheidende Rolle bei der Herstellung von Halbleitern. Es fungiert als Dotierungsmaterial und verändert aktiv die elektrischen Eigenschaften von Silizium.
Das breite Anwendungsspektrum von Boroxid unterstreicht seine Vielseitigkeit und Bedeutung in verschiedenen Branchen und trägt zu Fortschritten in Technologie, Sicherheit und Materialwissenschaft bei.
Fragen:
F: Welche Oxidationsstufe hat Bor in B2O3?
A: Die Oxidationsstufe von Bor in B2O3 beträgt +3.
F: Wie lautet die empirische Formel für Boroxid?
A: Die empirische Formel für Boroxid lautet B2O3.
F: Wann beeinflusst die Oberflächenkonzentration von Bor die Wachstumsrate des Oxids?
A: Die Oberflächenkonzentration von Bor beeinflusst die Wachstumsrate des Oxids, wenn es als Dotierstoff oder Katalysator im Oxidationsprozess fungiert.
F: Was ist Boria-Boroxid?
A: Boroxid, auch Boroxid genannt, ist eine Verbindung mit der chemischen Formel B2O3.
F: Wie hoch ist die Oxidationszahl von Bor?
A: Bor hat im Allgemeinen eine Oxidationszahl von +3.
F: Verlangsamt Bor die Oxidation in sauerstoffarmen Materialien?
A: Bor verlangsamt die Oxidation in sauerstoffarmen Materialien nicht, da es Sauerstoff zur Bildung von Boroxid benötigt.
F: Welche Oxidationsstufe hat Bor in HBO2 in CuO?
A: Die Oxidationsstufe von Bor in HBO2 beträgt +3.
F: Wie viele Mol B2O3 können gebildet werden?
A: Die Anzahl der gebildeten Mol B2O3 hängt von der Menge der in der Reaktion verwendeten Reaktanten ab.
F: Ist B2O3 ionisch oder molekular?
A: B2O3 ist eine ionische Verbindung.
F: Welches Paar ist in der Reihenfolge zunehmender Basizität aufgeführt? PBO < SiO2 B2O3 < Li2O
A: Das in der Reihenfolge zunehmender Basizität aufgeführte Paar ist B2O3 < Li2O < PBO < SiO2.
F: B2H6 + O2 → B2O3 + H2O, ist diese Gleichung ausgeglichen?
A: Nein, die Gleichung ist nicht ausgeglichen. Dies erfordert Anpassungen, um eine ausgewogene Gleichung zu erreichen.
F: Wie viel Bor kann man aus 210,0 Pfund B2O3 gewinnen?
A: Die aus 210,0 Pfund B2O3 gewonnene Bormenge hängt von der Molmasse und der Stöchiometrie der Reaktion ab.
