Natriumcyanid ist eine hochgiftige Verbindung, die in verschiedenen Industriezweigen verwendet wird. Es setzt Zyanidionen frei, die die Zellatmung beeinträchtigen und zu ernsthaften Gesundheitsrisiken und sogar zum Tod führen können.
| IUPAC-Name | Natriumcyanid |
| Molekularformel | NaCN |
| CAS-Nummer | 143-33-9 |
| Synonyme | Cyanogran, Natriumcyanid, Cyanidsalz, Natriumcyanidsalz |
| InChI | InChI=1S/CN.Na/c1-2;/h1H;/q-1;+1 |
Eigenschaften von Natriumcyanid
Natriumcyanid-Formel
Die Formel für Natriumcyanid lautet NaCN. Es besteht aus einem Na+-Kation und einem CN-Anion. Diese chemische Verbindung wird häufig in verschiedenen industriellen Prozessen verwendet.
Molmasse von Natriumcyanid
Die Molmasse von NaCN wird durch Addition der Atommassen seiner Bestandteile Natrium (Na) und Kohlenstoff (C) plus Stickstoff (N) berechnet. Die Molmasse von NaCN beträgt etwa 49,01 Gramm pro Mol.
Siedepunkt von Natriumcyanid
NaCN hat einen Siedepunkt von etwa 1.496 Grad Celsius. Bei dieser Temperatur vollzieht die Verbindung einen Phasenwechsel von flüssig zu gasförmig. Aufgrund seiner toxischen Natur ist es wichtig, mit NaCN vorsichtig umzugehen.
Natriumcyanid Schmelzpunkt
Der Schmelzpunkt von NaCN liegt bei etwa 564 Grad Celsius. Bei dieser Temperatur geht die feste Verbindung in den flüssigen Zustand über. Beim Umgang mit NaCN ist Vorsicht geboten, da es ernsthafte Gesundheitsrisiken birgt.
Dichte von Natriumcyanid g/ml
Die Dichte von NaCN beträgt etwa 1,6 Gramm pro Milliliter. Dieser Dichtewert gibt die Masse des Stoffes pro Volumeneinheit an. Die hohe Dichte von NaCN trägt zu seiner Stabilität bei und erleichtert seinen Einsatz in verschiedenen Anwendungen.
Molekulargewicht von Natriumcyanid
Das Molekulargewicht von NaCN beträgt etwa 49,01 Gramm pro Mol. Dieser Wert stellt die Summe der Atomgewichte seiner Bestandteile dar. Das Molekulargewicht von NaCN ist entscheidend für die Bestimmung der Menge der Verbindung, die für chemische Reaktionen benötigt wird.
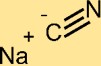
Struktur von Natriumcyanid
NaCN hat eine Kristallstruktur, die aus Na+-Kationen und CN–Anionen besteht. Das Cyanid-Ion besteht aus einem Kohlenstoffatom, das an ein Stickstoffatom gebunden ist. Die Struktur von NaCN spielt eine wichtige Rolle für seine Reaktivität und sein chemisches Verhalten.
Löslichkeit von Natriumcyanid
NaCN ist in Wasser gut löslich, mit einer Löslichkeit von etwa 46 Gramm pro 100 Milliliter bei Raumtemperatur. Diese hohe Löslichkeit ermöglicht eine effiziente Auflösung und Nutzung von NaCN in verschiedenen Prozessen.
| Aussehen | Weißer kristalliner Feststoff |
| Spezifisches Gewicht | 1,6 g/ml |
| Farbe | Weiß |
| Geruch | Geruchlos |
| Molmasse | 49,01 g/Mol |
| Dichte | 1,6 g/ml |
| Fusionspunkt | 564°C |
| Siedepunkt | 1496°C |
| Blitzpunkt | Unzutreffend |
| Löslichkeit in Wasser | Löslich |
| Löslichkeit | Löslich in Wasser, Ammoniak, Methanol, Ethanol |
| Dampfdruck | Nicht verfügbar |
| Wasserdampfdichte | Nicht verfügbar |
| pKa | Nicht verfügbar |
| pH-Wert | Alkalisch |
Sicherheit und Gefahren von Natriumcyanid
NaCN birgt aufgrund seiner toxischen Natur erhebliche Sicherheitsrisiken und Gefahren. Der Kontakt mit dieser Verbindung kann schwerwiegende gesundheitliche Folgen haben. Es stört die Zellatmung und verhindert so die Sauerstoffversorgung lebenswichtiger Organe, was zu Atemnot, Herzstillstand und sogar zum Tod führen kann. Das Einatmen oder Verschlucken von NaCN kann schnelle und möglicherweise tödliche Symptome hervorrufen. Der Umgang mit NaCN erfordert äußerste Vorsicht, einschließlich der Verwendung geeigneter persönlicher Schutzausrüstung (PSA) und der Einhaltung von Sicherheitsprotokollen. Es ist von entscheidender Bedeutung, NaCN ordnungsgemäß zu lagern, zu transportieren und zu entsorgen, um eine versehentliche Freisetzung oder Kontamination zu vermeiden. Um die mit NaCN verbundenen Risiken zu minimieren, sind regelmäßige Schulungen und Sensibilisierung unerlässlich.
| Gefahrensymbole | Totenkopf |
| Sicherheitsbeschreibung | Sehr giftig |
| UN-Identifikationsnummern | Ein 1689 |
| HS-Code | 2837.11.00 |
| Gefahrenklasse | 6.1 |
| Verpackungsgruppe | ICH |
| Toxizität | Tödlich für den Menschen. Es setzt Blausäure frei, ein hochgiftiges chemisches Erstickungsmittel, das die Fähigkeit des Körpers, Sauerstoff zu nutzen, beeinträchtigt. |
Methoden zur Synthese von Natriumcyanid
Es gibt mehrere Methoden zur Synthese von NaCN, die jeweils die Reaktion geeigneter Reagenzien beinhalten. Eine gängige Methode ist das Castner-Verfahren. Bei diesem Prozess erzeugt die geschmolzene Mischung aus Natriumcarbonat , Kohlenstoff und Stickstoffgas einen elektrischen Strom, wodurch NaCN entsteht. Sammeln Sie dann das verfestigte NaCN.
Bei einer anderen Methode reagiert Natriumhydroxid mit HCN-Gas. Mischen Sie Wasser mit Natriumhydroxid, um eine Lösung zu erzeugen, und setzen Sie die Lösung HCN-Gas aus. Daher bilden NaCN und Wasser Nebenprodukte.
Darüber hinaus beinhaltet die Synthese von NaCN die Reaktion zwischen dem Metall Na und Cyanwasserstoffgas. Leiten Sie das Gas in das Natriummetall ein, was zu einer heftigen Reaktion führt, bei der NaCN und Wasserstoffgas entstehen.
Es ist wichtig zu beachten, dass die Synthese von NaCN nur von geschultem Fachpersonal in gut ausgestatteten Einrichtungen durchgeführt werden sollte. Aufgrund der hochtoxischen Natur der Verbindung erfordert der Prozess die strikte Einhaltung von Sicherheitsprotokollen.
Verwendung von Natriumcyanid
Aufgrund seiner einzigartigen Eigenschaften findet NaCN vielfältige Anwendungsmöglichkeiten in verschiedenen Branchen. Hier sind einige häufige Verwendungszwecke:
- Goldbergbau: Der Goldbergbau nutzt häufig NaCN, um Edelmetalle aus Erzen zu gewinnen. Es bildet mit Gold einen Komplex, der die Abtrennung und Reinigung des Metalls erleichtert.
- Metallbeschichtung: Bei der Galvanisierung wird NaCN verwendet, um eine Metallschicht auf Oberflächen abzuscheiden. Es ermöglicht die Bildung einer schützenden und dekorativen Beschichtung, die die Haltbarkeit und das Aussehen verbessert.
- Chemische Synthese: NaCN dient als Vorstufe für die Synthese verschiedener organischer Verbindungen bei der Herstellung von Arzneimitteln, Kunststoffen, Farbstoffen und anderen Chemikalien.
- Schädlingsbekämpfung: NaCN wirkt als Begasungsmittel zur Schädlingsbekämpfung in bestimmten landwirtschaftlichen Kontexten. Es beseitigt Nagetiere und Schädlinge, die Schäden an Ernten und gelagerten Produkten verursachen können.
- Aufkohlen: NaCN trägt zum Aufkohlen bei, einem Prozess, der die Oberflächenhärte von Stahlgegenständen verbessert. Es bildet eine harte Außenschicht, die die Verschleiß- und Korrosionsbeständigkeit verbessert.
- Schmuckherstellung: Bei der Schmuckherstellung wird NaCN zum Reinigen, Polieren und Ätzen von Metallen verwendet. Es trägt dazu bei, die gewünschte Oberflächengüte zu erzielen und Verunreinigungen zu entfernen.
- Laborforschung: NaCN findet Anwendung in verschiedenen Laborexperimenten und in der Forschung, insbesondere in den Bereichen Chemie, Biochemie und Metallurgie.
Fragen:
F: Wofür wird Natriumcyanid verwendet?
A: NaCN wird im Goldbergbau, in der Metallbeschichtung, in der chemischen Synthese, zur Schädlingsbekämpfung, beim Aufkohlen, in der Schmuckherstellung und in der Laborforschung verwendet.
F: Wie stellt man Natriumcyanid her?
A: NaCN kann durch Methoden wie das Castner-Verfahren, die Reaktion mit Natriumhydroxid und HCN-Gas oder die Reaktion von Natriummetall mit HCN-Gas synthetisiert werden.
F: Wie viele Atome sind insgesamt in 9,203 e-22 Mol Natriumcyanid enthalten?
A: In 9,203 e-22 mol NaCN kann die Gesamtzahl der Atome basierend auf der Avogadro-Zahl berechnet werden, die ungefähr 6,022 x 10^23 Atome/mol beträgt.
F: Ist Natriumcyanid wasserlöslich?
A: Ja, NaCN ist in Wasser gut löslich.
F: Macht Natriumcyanid Sn2?
A: NaCN kann an SN2-Reaktionen (bimolekulare nukleophile Substitution) teilnehmen.
F: Ist Natriumcyanid tödlich?
A: Ja, NaCN ist hochgiftig und kann bei unsachgemäßer Handhabung tödlich sein.
F: Wie wird Natriumcyanid im Bergbau verwendet?
A: NaCN wird im Bergbau zur Goldgewinnung verwendet, wo es mit Gold einen Komplex bildet und sich so leichter von den Erzen trennen lässt.
F: Wie lösche ich Natriumcyanid?
A: NaCN kann durch Zugabe eines geeigneten Desaktivierungsmittels wie Wasserstoffperoxid oder Natriumhypochlorit deaktiviert werden, um es in weniger toxische Substanzen umzuwandeln.
F: Was ist das Hauptprodukt, das bei der Behandlung von (R)1-Brom-4-methylhexan mit Natriumcyanid entsteht?
A: Das Hauptprodukt, das bei der Behandlung von (R)1-Brom-4-methylhexan mit NaCN entsteht, ist (R)4-Methylhexannitril.
F: Welche der folgenden Substanzen reagiert am langsamsten mit NaCN?
A: Die Reaktivität mit NaCN kann variieren, aber primäre Alkylhalogenide reagieren im Allgemeinen langsamer als sekundäre oder tertiäre Alkylhalogenide.
F: Hemmt Cyanid die Na-K-Pumpe?
A: Ja, CN hemmt die Natrium-Kalium-Pumpe, die für die Aufrechterhaltung der ordnungsgemäßen Zellfunktion von entscheidender Bedeutung ist.
