Piperidin ist ein zyklisches Amin, das aus einem Sechsring mit einem Stickstoffatom besteht. Es wird in Arzneimitteln, Pestiziden und als Lösungsmittel für organische Reaktionen verwendet.
| IUPAC-Name | Piperidin |
| Molekularformel | C₅H₁₁N |
| CAS-Nummer | 110-89-4 |
| Synonyme | Hexahydropyridin, Azacyclohexan, Cyclopentimin |
| InChI | InChI=1S/C5H11N/c1-2-4-6-5-3-1/h6H,1-5H2 |
Eigenschaften von Piperidin
Piperidin-Formel
Die chemische Formel für Hexahydropyridin lautet C₅H₁₁N. Es besteht aus fünf Kohlenstoffatomen, elf Wasserstoffatomen und einem Stickstoffatom. Die Formel stellt die genaue Zusammensetzung der Elemente in einem Hexahydropyridin-Molekül dar.
Molmasse von Piperidin
Die Molmasse von Hexahydropyridin wird durch Addition der Atommassen seiner Bestandteile berechnet. Für Hexahydropyridin (C₅H₁₁N) beträgt die Molmasse etwa 85,15 Gramm pro Mol. Dieser Wert ist nützlich, um die Menge an Hexahydropyridin in einer bestimmten Probe zu bestimmen.
Siedepunkt von Piperidin
Hexahydropyridin hat einen Siedepunkt von etwa 106 Grad Celsius. Diese Temperatur stellt den Punkt dar, an dem die flüssige Form von Hexahydropyridin in ein Gas übergeht. Der Siedepunkt ist in verschiedenen industriellen Prozessen wichtig, bei denen Hexahydropyridin verwendet wird.
Schmelzpunkt von Piperidin
Der Schmelzpunkt von Hexahydropyridin liegt bei etwa -7 Grad Celsius. Sie gibt die Temperatur an, bei der festes Hexahydropyridin in den flüssigen Zustand übergeht. Der Schmelzpunkt ist ein entscheidendes Merkmal für die Handhabung und Lagerung von Hexahydropyridin in verschiedenen Anwendungen.
Piperidindichte g/ml
Die Dichte von Hexahydropyridin beträgt etwa 0,86 Gramm pro Milliliter (g/ml). Unter Dichte versteht man die Masse eines Stoffes pro Volumeneinheit. Diese Eigenschaft ist wertvoll bei der Bestimmung der Menge an Hexahydropyridin, die für bestimmte Anwendungen erforderlich ist.
Molekulargewicht von Piperidin
Das Molekulargewicht von Hexahydropyridin beträgt etwa 85,15 Gramm pro Mol. Es stellt die Summe der Atomgewichte aller in einem Hexahydropyridinmolekül vorhandenen Atome dar. Das Molekulargewicht ist ein wesentlicher Parameter, der bei verschiedenen chemischen Berechnungen und Reaktionen mit Hexahydropyridin verwendet wird.
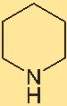
Struktur von Piperidin
Hexahydropyridin hat eine Ringstruktur, die aus einem sechsgliedrigen Ring mit einem Stickstoffatom und fünf Kohlenstoffatomen besteht. Die Anordnung der Atome in dieser Struktur beeinflusst die chemischen Eigenschaften und das Verhalten von Hexahydropyridin. Das Verständnis der Struktur ermöglicht es uns, ihre Reaktivität und Wechselwirkungen zu untersuchen.
Löslichkeit von Piperidin
Hexahydropyridin ist in Wasser und organischen Lösungsmitteln löslich. Aufgrund der Anwesenheit eines Stickstoffatoms bildet es Wasserstoffbrückenbindungen mit Wassermolekülen. Die Löslichkeit von Hexahydropyridin ermöglicht die Verwendung als Lösungsmittel in verschiedenen chemischen Prozessen und als Reagenz in der organischen Synthese.
| Aussehen | Klare Flüssigkeit |
| Spezifisches Gewicht | 0,862 g/ml |
| Farbe | Farblos |
| Geruch | Stark, ammoniakhaltig |
| Molmasse | 85,15 g/Mol |
| Dichte | 0,862 g/ml |
| Fusionspunkt | -7°C |
| Siedepunkt | 106°C |
| Blitzpunkt | 9°C |
| Löslichkeit in Wasser | Mischbar |
| Löslichkeit | Löslich in polaren Lösungsmitteln wie Wasser und organischen Lösungsmitteln |
| Dampfdruck | 7,4 mmHg bei 25°C |
| Wasserdampfdichte | 2,95 (Luft=1) |
| pKa | 11.24 |
| pH-Wert | Basic |
Sicherheit und Gefahren von Piperidin
Hexahydropyridin birgt mehrere Sicherheitsrisiken und sollte mit Vorsicht gehandhabt werden. Es reizt Haut, Augen und Atemwege. Direkter Kontakt kann zu Verbrennungen oder Reizungen führen. Das Einatmen von Hexahydropyridindämpfen kann zu Atembeschwerden und Lungenschäden führen. Es ist brennbar und kann mit Luft explosionsfähige Gemische bilden. Beim Erhitzen können giftige Dämpfe, einschließlich Stickoxide, freigesetzt werden. Bei der Arbeit mit Hexahydropyridin sind ausreichende Belüftung und persönliche Schutzausrüstung wie Handschuhe und Schutzbrille erforderlich. Darüber hinaus sollte es an einem kühlen, gut belüfteten Ort fern von Zündquellen gelagert werden. Um potenzielle Risiken zu minimieren, sind beim Umgang mit Hexahydropyridin eine angemessene Schulung und Kenntnisse der Sicherheitsprotokolle unerlässlich.
| Gefahrensymbole | Totenkopf, Flamme, ätzend |
| Sicherheitsbeschreibung | Kontakt mit Haut und Augen vermeiden. In einem gut belüfteten Bereich verwenden. Von Zündquellen fernhalten. |
| UN-Identifikationsnummern | UN-Nr. 2879 (für Piperidin) |
| HS-Code | 2933.99.80 |
| Gefahrenklasse | Klasse 6.1 (Giftige Stoffe) |
| Verpackungsgruppe | Verpackungsgruppe II |
| Toxizität | Piperidin ist giftig und kann schwerwiegende gesundheitliche Auswirkungen haben. Einatmen, Verschlucken oder Hautabsorption sollten vermieden werden. Eine längere oder wiederholte Exposition kann zu Organschäden oder Atemproblemen führen. Bei der Handhabung und Lagerung sind entsprechende Schutzmaßnahmen zu treffen. |
Piperidin-Synthesemethoden
Es gibt verschiedene Methoden zur Synthese von Hexahydropyridin.
Eine häufig verwendete Methode ist die Reaktion von 1,5-Dihalogenpentan mit Ammoniak . Bei diesem Prozess ersetzt die Aminogruppe (-NH2) die Halogenatome durch eine nukleophile Substitution. Eine andere Methode beinhaltet die Reduktion von Pyridin mit Wasserstoffgas über einem Katalysator wie Palladium oder Platin. Diese Reduktionsreaktion wandelt Pyridin in Hexahydropyridin um, indem zwei Wasserstoffatome an das Stickstoffatom addiert werden.
Darüber hinaus ergibt die Hydrierung von Pyridiniumsalzen oder Pyridinderivaten Hexahydropyridin. Dieser Hydrierungsprozess erfolgt unter hohem Druck und hoher Temperatur unter Verwendung eines geeigneten Katalysators. Ein anderer Ansatz beinhaltet die Reaktion von 2,5-Dimethylpyrrol mit Acetylen und die anschließende Hydrierung, die Hexahydropyridin ergibt.
Darüber hinaus kann auch die reduktive Aminierung von Cyclopentanon oder seinen Derivaten mit Ammoniak oder primären Aminen zur Bildung von Hexahydropyridin führen. Bei dieser Reaktion wird der Ketongruppe eine Aminogruppe hinzugefügt und anschließend reduziert, um den Hexahydropyridinring zu bilden.
Insgesamt ermöglichen diese Synthesemethoden die Gewinnung von Hexahydropyridin aus verschiedenen Rohstoffen und ermöglichen so seine Produktion in verschiedenen Industrie- und Forschungsumgebungen. Die Wahl der Methode hängt von Faktoren wie der Verfügbarkeit der Rohstoffe, der gewünschten Ausbeute und den spezifischen Anwendungsanforderungen ab.
Verwendungsmöglichkeiten von Piperidin
Hexahydropyridin findet aufgrund seiner vielseitigen Eigenschaften zahlreiche Anwendungen in verschiedenen Branchen. Einige häufige Anwendungen von Hexahydropyridin sind:
- Pharmazeutische Industrie: Die pharmazeutische Industrie verwendet Hexahydropyridin als Baustein zur Synthese vieler pharmazeutischer Verbindungen. Es spielt eine entscheidende Rolle bei der Herstellung von Arzneimitteln wie Antihistaminika, Antipsychotika, Analgetika und antiviralen Wirkstoffen.
- Agrochemikalien: Hexahydropyridin verbessert die Wirksamkeit von Pestiziden und Insektiziden, da Hersteller es in ihrer Produktion verwenden. Es verbessert die Schädlingsbekämpfung und steigert die Ernteerträge.
- Organische Synthese: Hexahydropyridin fungiert als Katalysator oder Lösungsmittel bei organischen Reaktionen und erleichtert Kondensations-, Zyklisierungs- und Oxidationsprozesse. Es ermöglicht die Synthese verschiedener chemischer Verbindungen.
- Gummiindustrie: In der Gummiindustrie fungiert Hexahydropyridin als Vulkanisationsbeschleuniger. Es verbessert die mechanische Festigkeit, Elastizität und Haltbarkeit von Gummiprodukten, indem es die Vernetzung von Gummipolymeren verbessert.
- Lösungsmittel: Hexahydropyridin dient als Lösungsmittel für verschiedene organische Verbindungen und eignet sich daher für Extraktionsprozesse, chemische Reaktionen und als Medium für die pharmazeutische Formulierung. Es löst ein breites Spektrum an Stoffen.
- Korrosionsinhibitor: Hexahydropyridin fungiert als Korrosionsinhibitor und schützt Metalloberflächen vor Zersetzung. Es bildet einen Schutzfilm auf dem Metall und verlangsamt oder verhindert Korrosionsreaktionen.
- Laborreagenz: Forscher verwenden Hexahydropyridin als Reagenz in Laborexperimenten, insbesondere in der organischen Chemie. Es nimmt aktiv an Reaktionen wie N-Alkylierungen und Ringöffnungsreaktionen teil und erleichtert so die Synthese gewünschter Verbindungen.
- Chemische Zwischenprodukte: Hexahydropyridin-Derivate dienen als Zwischenprodukte bei der Herstellung verschiedener Chemikalien, darunter Farbstoffe, Duftstoffe und Tenside.
Diese Anwendungen verdeutlichen die vielfältige und wertvolle Rolle, die Hexahydropyridin in zahlreichen Branchen spielt und zur Entwicklung von Pharmazeutika, Agrochemikalien, Gummiprodukten und mehr beiträgt.
Fragen:
F: Wie hoch ist der pKa von Piperidin?
A: Der pKa von Hexahydropyridin beträgt ungefähr 11,24.
F: Wie hoch ist der pKa-Wert von Diethylmalonat?
A: Der pKa von Diethylmalonat beträgt etwa 12,5.
F: Warum ist die konjugierte Säure von Morpholin saurer als die konjugierte Säure von Piperidin?
A: Morpholinkonjugatsäure ist saurer, da im Morpholinring ein elektronenziehendes Sauerstoffatom vorhanden ist, das die positive Ladung der Konjugatsäure stabilisiert.
F: Wie entferne ich das Dibenzofulven-Piperidin-Addukt?
A: Das Dibenzofulven-Piperidin-Addukt kann je nach den spezifischen Bedingungen und der gewünschten Reinheit durch geeignete Reinigungstechniken wie Lösungsmittelextraktion, Chromatographie oder Umkristallisation entfernt werden.
F: Welche Rolle spielt Piperidin bei der von Ihnen durchgeführten Reaktion?
A: Hexahydropyridin kann je nach den spezifischen Reaktionsbedingungen und Anforderungen als Katalysator, Base oder Reagenz fungieren.
F: Ist Piperidin mit THF mischbar?
A: Ja, Hexahydropyridin ist mit THF (Tetrahydrofuran) mischbar.
F: Was passiert, wenn Piperidin und DMF kombiniert werden?
A: Wenn Hexahydropyridin und DMF (Dimethylformamid) kombiniert werden, können sie abhängig von den Reaktionsbedingungen und der Anwesenheit anderer Reaktanten oder Katalysatoren möglicherweise verschiedene Reaktionen eingehen.
F: Wie hoch ist der pH-Wert einer Lösung mit 0,120 M Piperidin und 0,079 M Chloridsalz?
A: Der pH-Wert der Lösung würde vom pKa des Hexahydropyridins und der Dissoziation seines Chloridsalzes abhängen und würde zusätzliche Berechnungen erfordern, um den genauen pH-Wert zu bestimmen.
F: Wie kann man den Piperidinring brechen?
A: Das Aufbrechen des Hexahydropyridinrings kann durch verschiedene Methoden wie Oxidation, Reduktion oder Ringöffnungsreaktionen unter Verwendung geeigneter Reagenzien und Reaktionsbedingungen erreicht werden.
F: Basizität von Pyridin oder Piperidin?
A: Hexahydropyridin ist im Allgemeinen basischer als Pyridin, da in seinem Ring ein nukleophileres Stickstoffatom vorhanden ist, wodurch es leichter ein Proton abgeben kann.
