Acetaldehyd ist eine flüchtige organische Verbindung, die beim Stoffwechsel von Alkohol entsteht und Katersymptome verursacht. Es wird auch als chemisches Zwischenprodukt in verschiedenen Industrien verwendet.
| IUPAC-Name | Ethanal |
| Molekularformel | C₂H₄O |
| CAS-Nummer | 75-07-0 |
| Synonyme | Ethylaldehyd, Essigsäurealdehyd, Ethanal, 1-Oxapropylen |
| InChI | InChI=1S/C2H4O/c1-2-3/h2H,1H3 |
Eigenschaften von Acetaldehyd
Acetaldehyd-Formel
Die Formel für Ethanal lautet C₂H₄O. Es besteht aus zwei Kohlenstoffatomen, vier Wasserstoffatomen und einem Sauerstoffatom. Die Formel gibt das Verhältnis der in einem Ethanalmolekül vorhandenen Atome an.
Acetaldehyd-Molmasse
Die Molmasse von Ethanol beträgt etwa 44,05 g/mol. Sie wird durch Addition der Atommassen aller Atome im Molekül gemäß der Formel C₂H₄O berechnet.
Siedepunkt von Acetaldehyd
Ethanal hat einen Siedepunkt von etwa 20,2 Grad Celsius (68,4 Grad Fahrenheit). Dies ist die Temperatur, bei der Ethanol unter normalem Atmosphärendruck von flüssig in gasförmig übergeht.
Schmelzpunkt von Acetaldehyd
Der Schmelzpunkt von Ethanol liegt bei etwa -123,5 Grad Celsius (-190,3 Grad Fahrenheit). Dies ist die Temperatur, bei der Ethanol vom festen in den flüssigen Zustand übergeht.
Acetaldehyddichte g/ml
Die Dichte von Ethanol beträgt etwa 0,78 g/ml. Dieser Wert gibt die Masse an Ethanol pro Volumeneinheit an. Sie gibt an, wie dicht Moleküle in einem bestimmten Volumen der Substanz gepackt sind.
Molekulargewicht von Acetaldehyd
Das Molekulargewicht von Ethanol beträgt etwa 44,05 g/mol. Es ist die Summe der Atomgewichte aller Atome im Molekül und wird in Gramm pro Mol ausgedrückt.
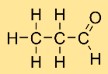
Struktur von Acetaldehyd
Ethanal hat eine lineare Struktur mit aneinander und an das Sauerstoffatom gebundenen Kohlenstoffatomen. Das Molekül besteht aus einem zentralen Kohlenstoffatom, zwei daran gebundenen Wasserstoffatomen und einem an das Kohlenstoffatom gebundenen Sauerstoffatom.
Löslichkeit von Acetaldehyd
Ethanal ist in Wasser und organischen Lösungsmitteln löslich. Aufgrund der Anwesenheit polarer funktioneller Gruppen löst es sich leicht in Wasser. Die Löslichkeit von Ethanal in Wasser nimmt mit steigender Temperatur ab.
| Aussehen | Farblose Flüssigkeit |
| Spezifisches Gewicht | 0,780 g/ml |
| Farbe | Farblos |
| Geruch | Würzig, fruchtig |
| Molmasse | 44,05 g/Mol |
| Dichte | 0,78 g/ml |
| Fusionspunkt | -123,5°C |
| Siedepunkt | 20,2°C |
| Blitzpunkt | -36°C |
| Löslichkeit in Wasser | Mischbar |
| Löslichkeit | Löslich in organischen Lösungsmitteln wie Ether, Alkohol, Essigsäure |
| Dampfdruck | 97,2 mmHg bei 25°C |
| Wasserdampfdichte | 1,52 (Luft = 1) |
| pKa | 13:55 Uhr |
| pH-Wert | 3,5-4,5 |
Sicherheit und Gefahren von Acetaldehyd
Ethanal wirft mehrere Sicherheits- und Gefahrenprobleme auf. Da es leicht entflammbar ist, sollten Vorkehrungen getroffen werden, um Zündquellen zu vermeiden. Das Einatmen von Ethanoldämpfen kann zu Reizungen der Atemwege, der Augen und der Haut führen. Eine längere Exposition kann schwerwiegendere gesundheitliche Auswirkungen haben. Ethanal ist außerdem potenziell krebserregend und mit einem erhöhten Krebsrisiko verbunden. Beim Umgang mit Ethanol sollten ausreichende Belüftung und persönliche Schutzausrüstung verwendet werden. Darüber hinaus ist es wichtig, Ethanal in einem gut belüfteten Bereich, entfernt von inkompatiblen Substanzen, zu lagern und zu handhaben. Die Einhaltung von Sicherheitsrichtlinien und -protokollen ist entscheidend für die Minimierung der mit Ethanol verbundenen Risiken.
| Gefahrensymbole | Entzündlich, gesundheitsschädlich, krebserregend |
| Sicherheitsbeschreibung | Von Hitze, Funken und offenen Flammen fernhalten. Einatmen und Kontakt mit Augen und Haut vermeiden. Für ausreichende Belüftung und persönliche Schutzausrüstung sorgen. An einem kühlen, gut belüfteten Ort, entfernt von unverträglichen Substanzen, lagern. Befolgen Sie die Sicherheitsanweisungen und Protokolle. |
| UN-Identifikationsnummern | UN1089 |
| HS-Code | 29121900 |
| Gefahrenklasse | 3 (Brennbare Flüssigkeiten) |
| Verpackungsgruppe | II |
| Toxizität | Akute Toxizität: Gesundheitsschädlich bei Verschlucken, Einatmen oder Aufnahme durch die Haut. Eine langfristige Exposition kann das Krebsrisiko erhöhen. |
Methoden zur Synthese von Acetaldehyd
Es gibt verschiedene Methoden zur Synthese von Ethanol. Ein gängiger Ansatz besteht darin, Ethanol mit Oxidationsmitteln wie Kaliumdichromat oder Kupferoxid unter sauren Bedingungen zu oxidieren. Bei dieser Reaktion entsteht als Hauptprodukt Ethanol.
Eine andere Methode besteht darin, Ethylen zu dehydrieren, indem man es bei hoher Temperatur über einen Katalysator wie Silber oder Kupfer leitet. Bei diesem Prozess werden Wasserstoffatome aus Ethylen entfernt, was zur Bildung von Ethanal führt.
Bei der Hydratisierung von Acetylen kann Ethanal gewonnen werden. Wenn Acetylengas in Gegenwart von Katalysatoren wie Quecksilbersulfat oder Phosphorsäure mit Wasser reagiert, entsteht Ethanal.
Zur Herstellung von Ethanal durch Oxidation von Ethylenglykol können geeignete Oxidationsmittel wie Salpetersäure oder Kaliumpermanganat eingesetzt werden. Durch diese Oxidation wird Ethylenglykol in Ethanal umgewandelt.
Diese Beispiele veranschaulichen verschiedene Methoden zur Synthese von Ethanol, von denen jede ihre eigenen Vorteile hat. Die Wahl der Methode kann von Faktoren wie der Verfügbarkeit der Rohstoffe, der gewünschten Ausbeute und den Reaktionsbedingungen abhängen.
Verwendung von Acetaldehyd
Ethanal wird in unterschiedlichen Branchen vielfältig eingesetzt. Hier sind einige seiner Hauptanwendungen:
- Chemisches Zwischenprodukt: Ethanal dient als wichtiges chemisches Zwischenprodukt bei der Herstellung vieler organischer Verbindungen, darunter Essigsäure, Pyridin und Pentaerythrit.
- Lebensmittel- und Getränkeindustrie: In der Lebensmittel- und Getränkeindustrie wird Ethanol als Aromastoff und Konservierungsmittel verwendet. Ethanal verleiht verschiedenen Produkten wie Fruchtsäften, Süßigkeiten und Backwaren fruchtige oder nussige Aromen.
- Kunststoff- und Harzproduktion: Hersteller verwenden Ethanol zur Herstellung von Kunststoffen und Harzen, darunter Polyvinylacetat (PVA) und Polyacetal.
Diese Materialien finden Anwendung in Klebstoffen, Beschichtungen und synthetischen Fasern. - Pharmazeutika: Ethanal ist eine Vorstufe bei der Synthese vieler pharmazeutischer Verbindungen. Ethanal spielt eine Rolle bei der Herstellung von Vitaminen, Malariamitteln und Beruhigungsmitteln.
- Kautschukindustrie: Bei der Herstellung von synthetischem Kautschuk wird Ethanol verwendet. Es erleichtert die Vernetzung von Gummipolymeren und verbessert dadurch deren Haltbarkeit und Elastizität.
- Textilindustrie: Ethanal findet Anwendung als Färbe- und Veredelungsmittel in der Textilindustrie. Es trägt dazu bei, die Farbechtheit und Gesamtqualität von Textilmaterialien zu verbessern.
- Kraftstoff und Energie: Ethanal ist aufgrund seines hohen Energiegehalts ein potenzieller Kandidat für Biokraftstoffe. Ethanal vergärt aktiv zu Ethanol oder dient aktiv als Kraftstoffzusatz.
Dies sind nur einige Beispiele für die vielseitigen Einsatzmöglichkeiten von Ethanol. Seine vielfältigen Eigenschaften machen es zu einem wertvollen Bestandteil verschiedener industrieller Prozesse und tragen zur Entwicklung einer breiten Produktpalette in zahlreichen Branchen bei.
Fragen:
F: Wie kann man Acetaldehyd aus dem Körper entfernen?
A: Ethanal wird auf natürliche Weise durch Leberenzyme abgebaut, aber die Aufrechterhaltung eines gesunden Lebensstils, einschließlich ausreichender Flüssigkeitszufuhr und einer ausgewogenen Ernährung, kann die Entgiftungsprozesse des Körpers unterstützen.
F: Was ist Acetaldehyd?
A: Ethanal ist eine flüchtige organische Verbindung, die auf natürliche Weise im Körper beim Stoffwechsel von Alkohol entsteht und auch in verschiedenen industriellen Prozessen und Lebensmitteln vorkommt.
F: Welche Atom- oder Hybridorbitale bilden die Bindung zwischen C2 und O in Acetaldehyd, CH3CHO?
A: Die Bindung zwischen C2 und O in Acetaldehyd wird durch die Überlappung des sp²-Hybridorbitals von Kohlenstoff und des sp²-Hybridorbitals von Sauerstoff gebildet.
F: Wie wirkt sich Acetaldehyd auf die Leber aus?
A: Ethanal kann Leberschäden verursachen, indem es ihre normalen Funktionen beeinträchtigt und zu Entzündungen, oxidativem Stress und Fettansammlung in der Leber führt.
F: Wie riecht Acetaldehyd?
A: Ethanal hat einen stechenden, fruchtigen Geruch, der oft als ähnlich wie frisch geschnittene Äpfel oder Nagellackentferner beschrieben wird.
F: Ist Acetaldehyd wasserlöslich?
A: Ja, Ethanal ist wasserlöslich. Aufgrund der Anwesenheit polarer funktioneller Gruppen löst es sich leicht auf.
F: Sollte ich den Verzehr von Lebensmitteln vermeiden, die Acetaldehyd enthalten?
A: Ethanal kommt natürlicherweise in vielen Lebensmitteln vor, darunter Obst, Gemüse und fermentierte Produkte. Ein mäßiger Verzehr dieser Lebensmittel ist für die meisten Menschen im Allgemeinen unbedenklich.
F: Worin ist Acetaldehyd enthalten?
A: Ethanal ist in alkoholischen Getränken, Obst, Gemüse, Kaffee, Brot und verschiedenen fermentierten Lebensmitteln enthalten.
F: Wie schmeckt Acetaldehyd?
A: Ethanal hat einen scharfen, bitteren Geschmack.
F: Wie lagere ich Acetaldehyd?
A: Ethanal sollte an einem kühlen, gut belüfteten Ort gelagert werden, entfernt von Zündquellen, unverträglichen Substanzen und direkter Sonneneinstrahlung. Die Lagerung erfolgt üblicherweise in verschlossenen Behältern.
F: Wie wirkt sich Acetaldehyd auf den Körper aus?
A: Ethanal kann toxische Wirkungen auf den Körper haben und Symptome wie Kopfschmerzen, Übelkeit und Hitzewallungen hervorrufen, insbesondere wenn es in großen Mengen bei der Verstoffwechselung von Alkohol entsteht.
F: Wofür wird Acetaldehyd verwendet?
A: Ethanal wird als chemisches Zwischenprodukt in verschiedenen Branchen verwendet, darunter Lebensmittel und Getränke, Pharmazeutika, Kunststoffe und Textilien.
F: Wie spricht man Acetaldehyd aus?
A: Uh-see-tuhl-deh-hahyd.
