Ethyl-4-aminobenzoat, auch bekannt als Benzocain, ist ein Lokalanästhetikum, das häufig bei zahnärztlichen Eingriffen und zur topischen Schmerzlinderung eingesetzt wird. Es funktioniert, indem es Nervensignale blockiert.
| IUPAC-Name | Ethyl-4-aminobenzoat |
| Molekularformel | C9H11NO2 |
| CAS-Nummer | 94-09-7 |
| Synonyme | Benzocain, p-Aminobenzoesäureethylester, Ethylaminobenzoat, Ethyl-p-aminobenzoat, 4-(Ethoxycarbonyl)aniliniumbenzoat |
| InChI | InChI=1S/C9H11NO2/c1-2-12-9(11)7-3-5-8(10)6-4-7/h3-6H,2,10H2,1H3 |
Molmasse von Ethyl-4-aminobenzoat:
Die Molmasse von Ethyl-4-aminobenzoat beträgt 165,19 g/mol. Die Molmasse ist die Masse eines Mols einer Substanz und wird durch Addition der Atommassen aller Atome in einem Molekül berechnet. Die Molmasse ist ein wichtiger Parameter bei chemischen Reaktionen und wird zur Bestimmung der in einer Probe vorhandenen Substanzmenge verwendet.
Siedepunkt von Ethyl-4-aminobenzoat:
Der Siedepunkt von Ethyl-4-aminobenzoat beträgt 310,7°C. Der Siedepunkt ist die Temperatur, bei der der Dampfdruck einer Flüssigkeit dem Außendruck entspricht. Beim Siedepunkt vollzieht ein Stoff einen Phasenübergang von flüssig zu gasförmig. Der hohe Siedepunkt von Ethyl-4-aminobenzoat macht es zu einer geeigneten Verbindung für den Einsatz bei zahnärztlichen und medizinischen Eingriffen, bei denen hohe Temperaturen erforderlich sind.
Schmelzpunkt von Ethyl-4-aminobenzoat:
Der Schmelzpunkt von Ethyl-4-aminobenzoat liegt bei 89–92 °C. Der Schmelzpunkt ist die Temperatur, bei der ein fester Stoff in den flüssigen Zustand übergeht. Der Schmelzpunkt einer Verbindung hängt von ihrer chemischen Struktur, Reinheit und ihrem Druck ab. Ethyl-4-aminobenzoat hat einen niedrigen Schmelzpunkt, wodurch es leicht zu handhaben und bei der Herstellung von topischen Anästhetika und Analgetika zu verwenden ist.
Dichte von Ethyl-4-aminobenzoat g/ml:
Die Dichte von Ethyl-4-aminobenzoat beträgt 1,17 g/ml. Die Dichte ist die Menge an Masse pro Volumeneinheit eines Stoffes. Die Dichte einer Verbindung hängt von ihrem Molekulargewicht, ihrer Temperatur und ihrem Druck ab. Die hohe Dichte von Ethyl-4-aminobenzoat macht es zu einer schweren Verbindung, die leicht gemessen und in präzisen Mengen in chemischen Reaktionen eingesetzt werden kann.
Molekulargewicht von Benzocain:
Das Molekulargewicht von Benzocain beträgt 165,19 g/mol. Das Molekulargewicht ist die Summe der Atomgewichte aller Atome in einem Molekül. Das Molekulargewicht einer Verbindung ist wichtig für die Bestimmung ihrer physikalischen und chemischen Eigenschaften.
Struktur von Benzocain:
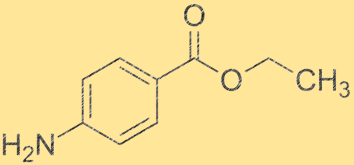
Die Struktur von Benzocain ist ein weißes kristallines Pulver mit der chemischen Formel C9H11NO2. Es besitzt einen Benzolring, an den eine Carboxylgruppe und eine Aminogruppe gebunden sind. Die Ethylgruppe ist an die Aminogruppe gebunden, wodurch es sich um ein Derivat der Benzoesäure handelt. Die Struktur von Benzocain ist wichtig für das Verständnis seiner physikalischen und chemischen Eigenschaften.
Benzocain-Formel:
Die chemische Formel für Benzocain lautet C9H11NO2. Es ist ein Derivat der Benzoesäure und hat eine Ethylgruppe an der Aminogruppe. Die Formel für Benzocain wird verwendet, um die Zusammensetzung der Verbindung darzustellen und ist wichtig für das Verständnis ihrer physikalischen und chemischen Eigenschaften.
| Aussehen | weißes kristallines Pulver |
| Spezifisches Gewicht | 1,17 g/ml |
| Farbe | Farblos bis weiß |
| Geruch | Geruchlos |
| Molmasse | 165,19 g/Mol |
| Dichte | 1,17 g/ml |
| Fusionspunkt | 89-92°C |
| Siedepunkt | 310,7°C |
| Blitzpunkt | 164,2°C |
| Löslichkeit in Wasser | Schwach löslich |
| Löslichkeit | Löslich in Ethanol, Chloroform, Ether |
| Dampfdruck | 1,07E-07 mmHg bei 25°C |
| Wasserdampfdichte | 5,7 (gegen Luft) |
| pKa | 2.5 |
| pH-Wert | 6,5 – 7,5 |
Sicherheit und Gefahren von Ethyl-4-aminobenzoat
Benzocain kann bei Kontakt Haut- und Augenreizungen verursachen. Das Verschlucken oder Einatmen der Verbindung kann zu Reizungen des Verdauungs- oder Atmungssystems führen. Eine längere oder wiederholte Einwirkung von Benzocain kann zu Leber- oder Nierenschäden führen. Die Verbindung gilt nicht als krebserregend oder mutagen, beim Umgang ist jedoch Vorsicht geboten. Beim Umgang mit Benzocain sollte geeignete persönliche Schutzausrüstung wie Handschuhe und Schutzbrille getragen werden. Bei Verschlucken oder versehentlicher Exposition sofort einen Arzt aufsuchen. Benzocain sollte an einem kühlen, trockenen Ort und fern von Zünd- oder Wärmequellen gelagert werden.
| Gefahrensymbole | XI |
| Sicherheitsbeschreibung | S22-S24/25-S36-S37 |
| UN-Identifikationsnummern | Nicht reguliert |
| HS-Code | 29224990 |
| Gefahrenklasse | Reizend |
| Verpackungsgruppe | Nicht reguliert |
| Toxizität | LD50 (Ratte, oral) = 940 mg/kg; LD50 (Ratte, dermal) > 2 g/kg |
Methoden zur Synthese von Ethyl-4-aminobenzoat
Benzocain, auch Benzocain genannt, kann auf verschiedene Weise synthetisiert werden. Eine übliche Methode beinhaltet die Reaktion von p-Aminobenzoesäure mit Ethanol in Gegenwart eines starken Säurekatalysators wie Schwefelsäure oder Salzsäure. Der resultierende Ethylester der p-Aminobenzoesäure wird dann mit Natriumnitrit und Salzsäure behandelt, um das Diazoniumsalz zu bilden. Dieses Salz reagiert dann mit Natriumacetat und Essigsäureanhydrid zu Ethyl-4-acetoxy-3-nitrobenzoat, das dann mit Zinn und Salzsäure zu Benzocain reduziert wird.
Eine andere Methode beinhaltet die Reaktion von p-Nitroanilin mit Ethylchlorformiat in Gegenwart von Natriumhydroxid unter Bildung von Ethyl-p-Nitrophenylcarbamat. Diese Verbindung wird dann mit Wasserstoffgas und einem Palladiumkatalysator reduziert, um Benzocain zu ergeben.
Bei einer dritten Methode wird Ethyl-4-nitrobenzoat mit Zinkstaub und Salzsäure reduziert, um Benzocain herzustellen.
Unabhängig von der verwendeten Synthesemethode muss die resultierende Verbindung durch Umkristallisation oder andere Methoden gereinigt werden, um ein reines Produkt zu erhalten. Benzocain ist ein häufig verwendetes Lokalanästhetikum und wird auch bei der Herstellung verschiedener Arzneimittel und Kosmetika verwendet.
Verwendung von Ethyl-4-aminobenzoat
Benzocain, ein übliches Lokalanästhetikum, betäubt den betroffenen Bereich und lindert vorübergehend Schmerzen und Juckreiz, die durch leichte Hautreizungen, Halsschmerzen, Zahnschmerzen und Zahnen verursacht werden. Es ist in verschiedenen Formen wie Cremes, Gels, Sprays und Lutschtabletten erhältlich und wird häufig in Arzneimitteln und Kosmetika eingesetzt. Es ist ein häufiger Bestandteil von Hustenbonbons, Halssprays, Mundschmerzgelen, Sonnenschutzlotionen und Lippenbalsam zur Linderung von Schmerzen durch Sonnenbrand und rissige Lippen.
Die Lebensmittelindustrie verwendet Benzocain auch als Aromastoff in Süßigkeiten, Kaugummi und anderen Süßwarenprodukten, um eine kühlende und betäubende Wirkung zu erzielen. Die US-amerikanische Food and Drug Administration (FDA) genehmigt die Verwendung in Lebensmitteln.
Benzocain sollte jedoch nur nach Anweisung eines Arztes oder gemäß den Angaben auf dem Produktetikett verwendet werden, um unerwünschte Nebenwirkungen wie Hautreizungen und allergische Reaktionen zu vermeiden. Es ist daher wichtig, es mit Vorsicht zu verwenden.
Fragen:
Ist Ethyl-4-aminobenzoat polar?
Ja, Ethyl-4-aminobenzoat ist polar. Es verfügt über eine polare funktionelle Gruppe (die Aminogruppe) und eine polare Estergruppe, was ihm ein Nettodipolmoment verleiht. Das bedeutet, dass es an einem Ende des Moleküls teilweise positiv und am anderen Ende teilweise negativ geladen ist, was es polar macht. Diese Eigenschaft von Benzocain macht es in polaren Lösungsmitteln wie Wasser und Ethanol löslich und in unpolaren Lösungsmitteln wie Hexan und Benzol weniger löslich. Die Polarität von Ethyl-4-aminobenzoat beeinflusst auch seine physikalischen und chemischen Eigenschaften, wie seinen Schmelzpunkt, Siedepunkt und seine Löslichkeit.
Ist Ethyl-4-aminobenzoat wasserlöslich?
Ja, Ethyl-4-aminobenzoat ist teilweise wasserlöslich. Es verfügt über eine polare funktionelle Gruppe und eine Estergruppe, wodurch es in der Lage ist, Wasserstoffbrückenbindungen mit Wassermolekülen zu bilden. Seine Wasserlöslichkeit ist jedoch aufgrund der in seiner Struktur vorhandenen unpolaren Ethylgruppe begrenzt. Dies bedeutet, dass Ethyl-4-aminobenzoat in organischen Lösungsmitteln wie Ethanol und Aceton besser löslich ist als in Wasser. Die Löslichkeit von Ethyl-4-aminobenzoat in Wasser hängt außerdem von verschiedenen Faktoren wie Temperatur, pH-Wert und der Anwesenheit anderer Substanzen ab. Unter normalen Bedingungen beträgt die Löslichkeit von Ethyl-4-aminobenzoat in Wasser etwa 0,3 g/L bei 25 °C.
