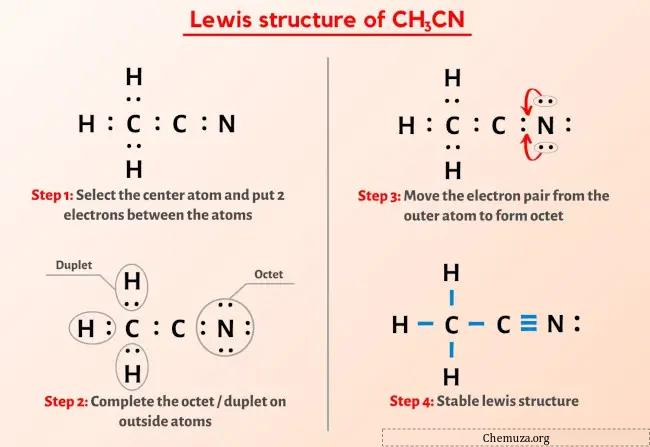
所以你已经看过上面的图片了,对吧?
让我简单解释一下上图。
CH3CN路易斯结构中心有2个碳(C)原子,周围环绕着3个氢(H)原子和1个氮(N)原子。碳原子(C)和氮原子(N)之间存在三键。氮 (N) 原子上有 1 个游离双峰。
如果您对上面的 CH3CN 路易斯结构图像没有理解任何内容,那么请跟着我,您将获得有关绘制CH3CN分子路易斯结构的详细逐步解释。
那么让我们继续绘制 CH3CN 的路易斯结构的步骤。
绘制 CH3CN 路易斯结构的步骤
步骤 1:求 CH3CN 中的价电子总数
为了找到CH3CN分子中的价电子总数,您首先需要知道碳原子、氢原子以及氮原子中存在的价电子。
(价电子是存在于任何原子最外层轨道的电子。)
在这里我将告诉您如何使用元素周期表轻松找到碳、氢和氮的价电子。
CH3CN 分子中的总价电子
→ 碳原子给出的价电子:
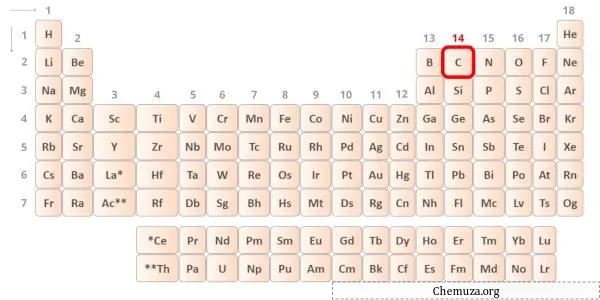
碳是元素周期表第 14 族的元素。 [1]因此,碳中存在的价电子为4 。
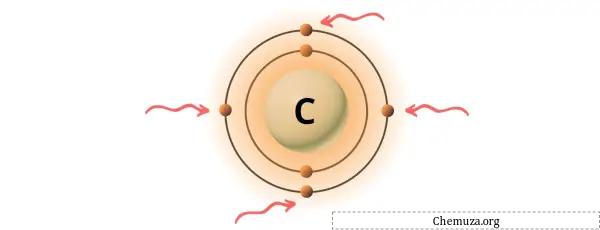
您可以看到碳原子中存在 4 个价电子,如上图所示。
→ 氢原子给出的价电子:
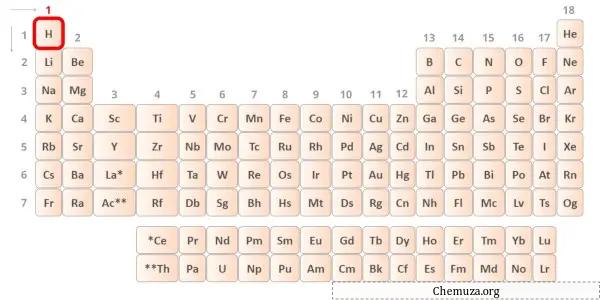
氢是元素周期表中的第 1 族元素。 [2]因此,氢中存在的价电子为1 。

您可以看到氢原子中只存在一个价电子,如上图所示。
→ 氮原子给出的价电子:
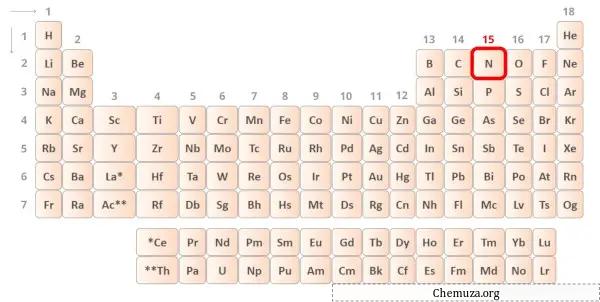
氮是元素周期表第 15 族的元素。[3]因此,氮中存在的价电子为5 。

您可以看到氮原子中存在 5 个价电子,如上图所示。
所以,
CH3CN分子中的总价电子= 2个碳原子贡献的价电子 + 3个氢原子贡献的价电子 + 1个氮原子贡献的价电子 = 4(2) + 1(3) + 5 = 16 。
第二步:选择中心原子
为了选择中心原子,我们必须记住电负性最小的原子保留在中心。
(记住:如果给定分子中存在氢,则始终将氢放在外面。)
现在这里给定的分子是 CH3CN,它包含碳 (C) 原子、氢 (H) 原子和氮 (N) 原子。
所以根据规则我们必须将氢气排除在外。
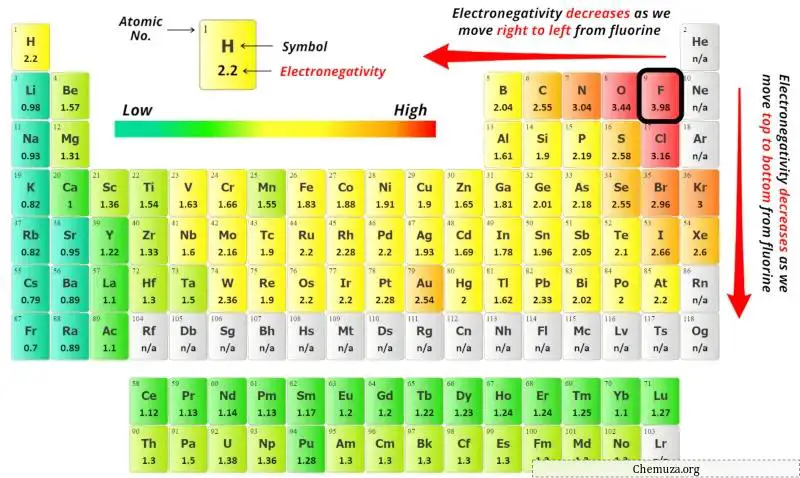
现在您可以看到上面元素周期表中碳原子(C)和氮原子(N)的电负性值。
如果我们比较碳(C)和氮(N)的电负性值,那么碳原子的电负性较小。
这里,碳(C)原子是中心原子,氮(N)原子是外部原子。
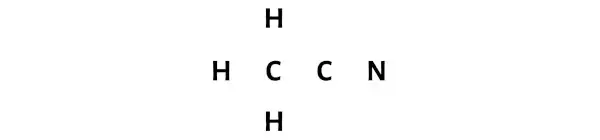
第三步:通过在原子之间放置一对电子来连接每个原子
现在,在 CH3CN 分子中,您需要将电子对放置在碳 (C)、氮 (N) 和氢 (H) 原子之间。
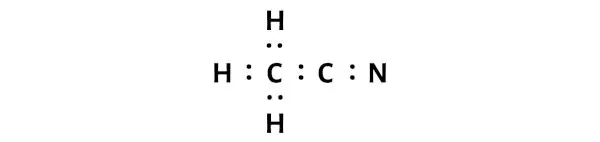
这表明这些原子在 CH3CN 分子中彼此化学键合。
第四步:使外部原子稳定
在此步骤中,您需要检查外部原子的稳定性。
在 CH3CN 分子的示意图中,您可以看到外部原子是氢原子和氮原子。
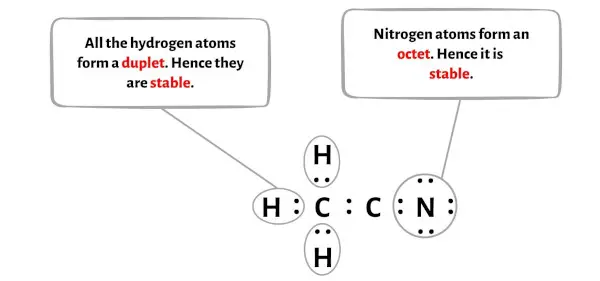
此外,在步骤 1 中,我们计算了 CH3CN 分子中存在的价电子总数。
CH3CN 分子共有16 个价电子,所有这些价电子都用于上图中。
因此,中心原子上不再有电子对。
现在让我们继续下一步。
步骤5:检查中心原子上的八位字节。如果它没有八位组,则移动孤对以形成双键或三键。
在此步骤中,您需要检查中心碳原子(C)是否稳定。
为了检查中心碳(C)原子的稳定性,我们需要检查它是否形成八位组。
不幸的是,碳原子在这里不形成八位组。碳只有4个电子,不稳定。
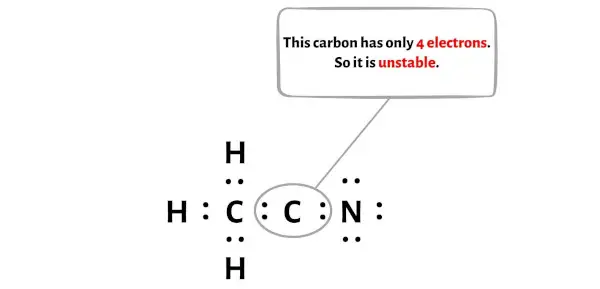
现在,为了使这个碳原子稳定,您需要移动外部氮原子的电子对,以便碳原子可以有8个电子(即1个八位组)。
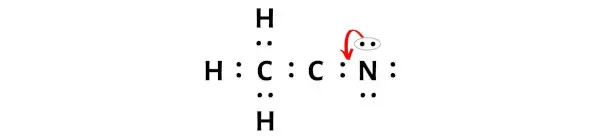
但在移动一对电子后,碳原子仍然没有形成八位组,因为它只有 6 个电子。
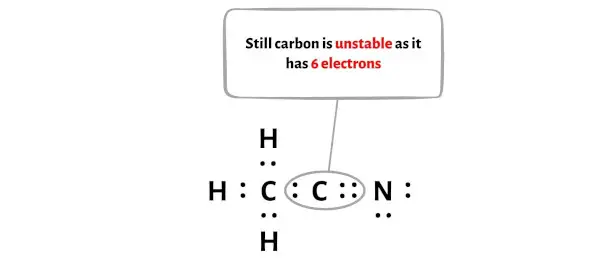
同样,我们只需要从氮原子上移动一对额外的电子。
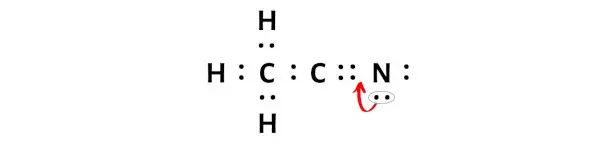
移动这对电子后,中心碳原子将多获得2个电子,其总电子数将变为8。
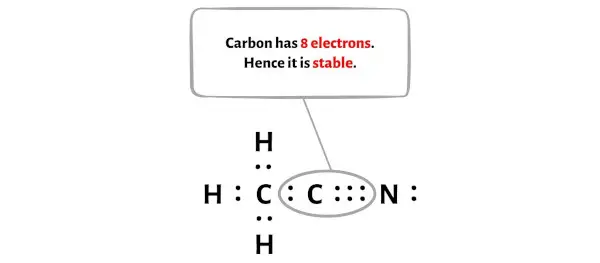
您可以在上图中看到碳原子形成一个八位组。
因此碳原子是稳定的。
现在让我们进行最后一步,检查 CH3CN 的路易斯结构是否稳定。
第6步:检查路易斯结构的稳定性
现在您已完成最后一步,您需要检查 CH3CN 的路易斯结构的稳定性。
路易斯结构的稳定性可以使用形式电荷概念来验证。
简而言之,我们现在必须找到 CH3CN 分子中氢 (H)、碳 (C) 和氮 (N) 原子的形式电荷。
要计算正式税,您必须使用以下公式:
形式电荷 = 价电子 – (键合电子)/2 – 非键合电子
您可以在下图中看到 CH3CN 分子每个原子的键合电子和非键合电子数量。
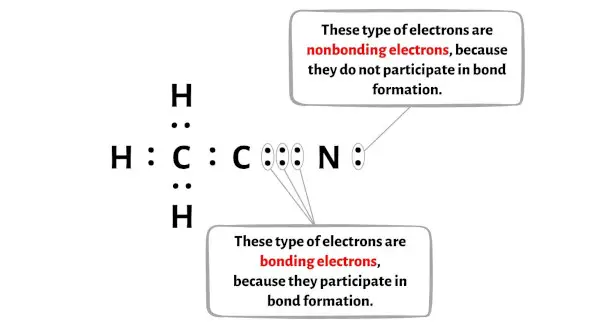
对于氢原子 (H):
价电子 = 1(因为氢属于第 1 族)
键合电子 = 2
非键合电子 = 0
对于碳原子 (C):
价电子 = 4(因为碳属于第 14 族)
键合电子 = 8
非键合电子 = 0
对于氮原子 (N):
价电子 = 5(因为氮属于第 15 族)
键合电子 = 6
非键合电子 = 2
| 正式指控 | = | 价电子 | – | (结合电子)/2 | – | 非键合电子 | ||
| H | = | 1 | – | 2/2 | – | 0 | = | 0 |
| VS | = | 4 | – | 8/2 | – | 0 | = | 0 |
| 不是 | = | 5 | – | 6/2 | – | 2 | = | 0 |
从上面的形式电荷计算中,您可以看到氢原子(H)、碳原子(C)以及氮原子(N)的形式电荷“为零” 。
这表明CH3CN的上述Lewis结构是稳定的,CH3CN的上述结构没有发生进一步的变化。
在上述 CH3CN 的路易斯点结构中,您还可以将每对成键电子 (:) 表示为单键(|)。这样做将产生以下 CH3CN 的路易斯结构。
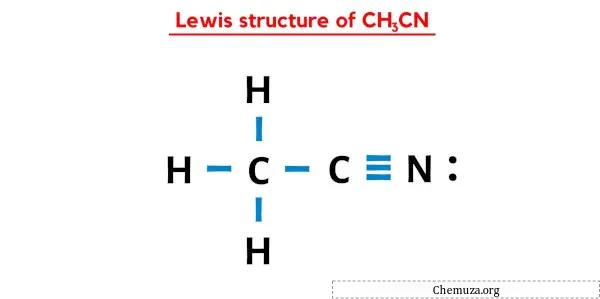
我希望您已经完全理解上述所有步骤。
为了进行更多练习和更好地理解,您可以尝试下面列出的其他路易斯结构。
尝试(或至少查看)这些路易斯结构以更好地理解:
