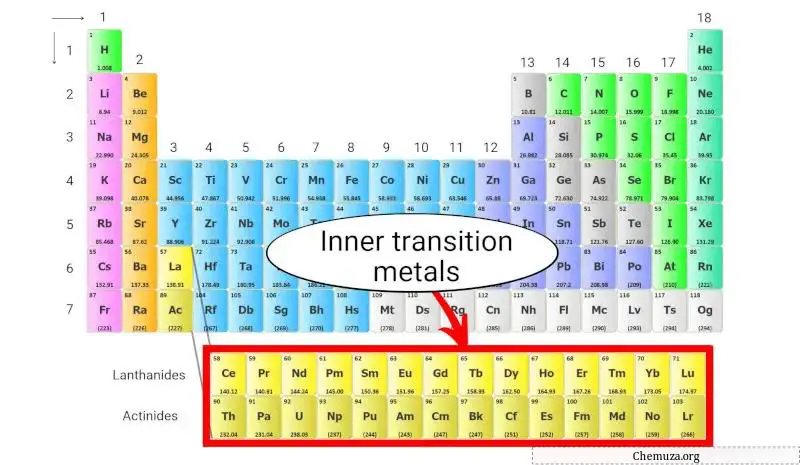
内部过渡金属是一组化学元素,位于元素周期表的底部两行,就在主要过渡金属块的下方。
内部过渡金属分为两类:
- 镧系元素,其原子序数范围为 57 至 71,以及
- 锕系元素,原子序数为 89 至 103。
让我们探索更多元素周期表的内部过渡元素。
什么是内部过渡金属?为什么它们被放置在底部?
内部过渡金属构成了元素周期表底部的元素组。
这些内部过渡金属只是过渡金属的一部分,也具有与过渡金属相似的性质。但它们被放置在内部部分作为第 3 组的扩展。
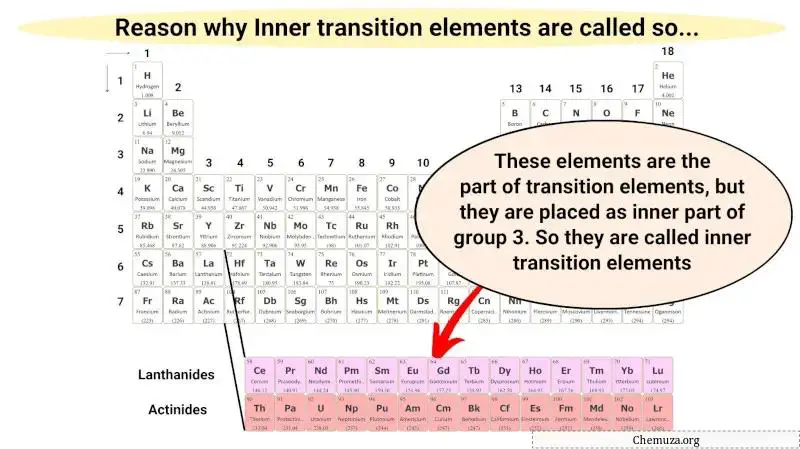
因此,这些金属元素被称为内部过渡金属。
为什么它们位于元素周期表的底部?
如果将内部过渡金属作为第3族的延伸,那么元素周期表就会显得很长(如下所示)。

因此,为了适合 A4 格式的纸张,将 2 排内部过渡金属放置在底部。
此外,这些内部过渡元素的价电子位于f 轨道中,因此这些元素表现出相似的化学性质。
正是由于这些原因,内部过渡金属被置于元素周期表的底部。
内部过渡金属列表
下面给出了内部过渡金属的列表。
| 原子数 | 象征 | 元素名称及符号 |
| 57 | 那里 | 镧 |
| 58 | 这 | 铈 |
| 59 | 普罗 | 镨 |
| 60 | 标准差 | 钕 |
| 61 | 下午 | 钷 |
| 62 | 小的 | 钐 |
| 63 | 我们 | 铕 |
| 64 | 上帝 | 钆 |
| 65 | 结核 | 铽 |
| 66 | 镝 | 镝 |
| 67 | 何 | 钬 |
| 68 | 呃 | 铒 |
| 69 | TM值 | 铥 |
| 70 | 镱 | 镱 |
| 71 | 读 | 镏 |
| 89 | 乙酰胆碱 | 锕 |
| 90 | 钍 | 钍 |
| 91 | 宾夕法尼亚州 | 镤 |
| 92 | 你 | 铀 |
| 93 | 氮磷 | 镎 |
| 94 | 可以 | 钚 |
| 95 | 是 | 镅 |
| 96 | 厘米 | 锔 |
| 97 | B.K. | 锫 |
| 98 | 看 | 加利福尼亚州 |
| 99 | 是 | 锿 |
| 100 | 调频 | 镄 |
| 101 | 马里兰州 | 钔 |
| 102 | 不 | 诺贝尔 |
| 103 | 左/右 | 劳伦斯 |
关于内部过渡金属的事实
以下是有关内部过渡金属的一些有趣事实:
- 内部过渡金属有两种类型:镧系元素和锕系元素。镧系元素是原子序数范围从 57(镧)到 71(镥)的 15 种元素,而锕系元素是原子序数范围从 89(锕)到 103(铍)的 15 种元素。
- 由于 f 轨道的存在,内部过渡金属具有独特的电子构型。这导致了不寻常的化学和物理特性,例如高熔点和沸点、复杂离子形成和顺磁性。
- 大多数内部过渡金属具有放射性,有些已用于核反应堆和武器。
- 内部过渡金属在技术和工业中很重要。例如,钕和钐用于制造强力磁铁[1] ,而铈用于催化转化器以减少车辆排放。 [2]
- 镧系元素也被称为“稀土元素”,因为它们在地壳中相对稀有。然而,它们实际上并不稀有,并且存在于许多矿物中。
- 锕系元素都具有放射性,其中一些元素,如铀和钚,对于核能和武器很重要。然而,由于其放射性,它们也造成环境和健康风险。
- 内部过渡金属自古以来就已为人所知,并用于珠宝和装饰。然而,直到20世纪,它们才被广泛研究或理解。
内部过渡金属的性质
以下是内部过渡金属的一些性质:
- 电子构型:内部过渡金属部分填充了 f 轨道,赋予它们独特的电子构型和不寻常的化学和物理性质。
- 高熔点和沸点:由于 f 轨道中存在不成对电子而产生牢固的金属键,因此内部过渡金属具有高熔点和沸点。
- 顺磁性:内部过渡金属是顺磁性的,这意味着它们由于 f 轨道中存在不成对电子而被磁场吸引。
- 络合离子的形成:由于存在空的 f 轨道,内部过渡金属可以形成络合离子,该空轨道可以容纳来自其他原子或分子的电子。
- 放射性:许多内部过渡金属由于其原子核中存在不稳定同位素而具有放射性。
- 氧化态:由于 f 轨道中存在多个价电子,内部过渡金属表现出一系列氧化态,包括高氧化态。
- 相似的化学性质:镧系元素和锕系元素具有相似的化学性质,这使得它们很难彼此分离。
- 金属光泽:内部过渡金属一般有光泽,由于其光反射率高而具有金属光泽。
内部过渡金属的用途
内过渡金属由于其独特的性质而具有广泛的用途。内部过渡金属的一些用途是:
- 核能:许多内部过渡金属,特别是铀等锕系元素,被用作核反应堆和武器的燃料。
- 磁铁:钕、钐和钆等稀土元素可用于制造用于各种应用的强力磁铁,包括计算机硬盘驱动器、风力涡轮机和核磁共振成像机。
- 照明:铕和铽等稀土元素用于制造荧光粉和 LED 照明用荧光粉。 [3]
- 催化作用:铈等稀土元素在许多工业过程中用作催化剂,包括石油精炼和污染控制。
- 玻璃制造:铒和镱等稀土元素用于给玻璃着色,而铈则用于抛光玻璃。
- 医学成像:钆和铽等稀土元素用于 MRI 扫描的造影剂。 [4]
- 电子产品:镝和铽等稀土元素用于电子设备,例如微波滤波器和液晶屏。
- 国防:内部过渡金属用于国防技术,包括核武器和穿甲弹。
概括
内部过渡金属是一组化学元素,位于元素周期表的底部两行,就在主要过渡金属块的下方。
它们分为两组:镧系元素和锕系元素,原子序数分别为 57 至 71 和 89 至 103。
内部过渡金属的位置位于元素周期表的底部,因为它们的价电子位于f轨道,具有相似的化学性质。
内部过渡金属具有高熔点和沸点、形成络合离子和顺磁性。由于 f 轨道中存在多个价电子,它们还表现出一系列氧化态,包括高氧化态。
