亚硝酸钾 (KNO2) 是一种常用作食品防腐剂的化合物。众所周知,它可以抑制细菌生长并防止肉类和其他食物腐败。
| 国际纯粹和应用化学联合会名称 | 亚硝酸钾 |
| 分子式 | 硝酸钾 |
| CAS 号 | 7758-09-0 |
| 同义词 | 亚硝酸、钾盐;硝石(III);亚硝酸,化合物。与钾盐(1:1); E249 |
| 乙酰胆碱 | InChI=1S/K.NO2/c;2-1-3/q+1;-1 |
亚硝酸钾性质
亚硝酸钾配方
亚硝酸钾的化学式是KNO2。它代表化合物的组成原子的组成。亚硝酸钾的公式用于计算其摩尔质量和分子量。
亚硝酸钾 摩尔质量
KNO2 的摩尔质量为 85.103 g/mol。它源自钾 (39.10 g/mol)、氮 (14.01 g/mol) 和两个氧原子 (2 x 16.00 g/mol) 的原子质量之和。 KNO2 的摩尔质量对于确定给定质量或体积中存在多少物质至关重要。
亚硝酸钾的沸点
KNO2 的沸点为 320°C (608°F)。在此温度下,化合物从液相变为气相。 KNO2 的沸点取决于多种因素,例如压力和纯度。
亚硝酸钾熔点
KNO2 的熔点为 441°C (826°F)。在此温度下,固体化合物转变为液相。 KNO2 的熔点是决定其是否适合各种应用(例如食品保存和医药)的关键参数。
亚硝酸钾密度 g/mL
室温下 KNO2 的密度为 1.915 g/mL。物质的密度定义为每单位体积物质的质量。 KNO2 的密度在决定其物理性质(例如溶解度和化学反应性)方面起着重要作用。
亚硝酸钾分子量
KNO2 的分子量为 85.103 g/mol。它是确定涉及 KNO2 的反应的化学计量的关键参数。 KNO2 的分子量也用于确定其物理和化学性质。
亚硝酸钾的结构
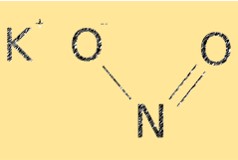
KNO2 的分子式为KNO2。它具有离子结构,含有钾阳离子 (K+) 和亚硝酸根阴离子 (NO2-)。亚硝酸根离子具有弯曲的分子几何形状,键角约为 115°。 KNO2 的结构对于决定其化学性质(例如溶解度和反应性)至关重要。
亚硝酸钾的溶解度
KNO2 极易溶于水,20°C 时溶解度约为 710 g/L。 KNO2 的溶解度取决于多种因素,如温度、压力和其他物质的存在。 KNO2 的溶解度是决定其是否适合各种应用(例如食品保存和医药)的关键参数。
| 外貌 | 白色至淡黄色结晶固体 |
| 比重 | 1,915 |
| 颜色 | 无色至白色 |
| 闻 | 无味 |
| 摩尔质量 | 85.103 克/摩尔 |
| 密度 | 1.915克/毫升 |
| 融合点 | 441°C (826°F) |
| 沸点 | 320°C(608°F) |
| 闪点 | 不适用 |
| 水中溶解度 | 极易溶解(20°C 时为 710 g/L) |
| 溶解度 | 溶于乙醇,微溶于氨水 |
| 蒸汽压力 | 25°C 时为 0.0038 毫米汞柱 |
| 蒸气密度 | 2.96(空气=1) |
| 酸度 | 3.35 |
| 酸碱度 | 5-8(5%溶液) |
亚硝酸钾的安全和危险
如果处理不当,KNO2 可能会很危险。吞咽或吸入有害,可能刺激眼睛、皮肤和呼吸系统。长期或反复接触 KNO2 会导致高铁血红蛋白血症,这是一种降低血液携氧能力的疾病。 KNO2也是一种强氧化剂,能与可燃材料发生剧烈反应,引起火灾或爆炸。处理 KNO2 时应采取适当的安全措施,例如使用防护设备、充分通风和安全储存。如果吞咽或吸入,请立即就医。
| 危险符号 | Xn |
| 安全说明 | S22、S24/25 |
| 联合国识别号 | 联合国1488 |
| 海关编码 | 2834.29.10 |
| 危险等级 | 5.1 |
| 包装组别 | 三、 |
| 毒性 | 吞咽或吸入有害,可能导致高铁血红蛋白血症 |
亚硝酸钾的合成方法
氢氧化钾 (KOH)与亚硝酸 (HNO2) 反应合成 KNO2。该反应产生副产物 KNO2 和水 (H2O)。工业上通常使用这种方法来制造大量的 KNO2。
反应方程式为:
2 KOH + HNO2 → KNO2 + 2 H2O
另一种合成 KNO2 的方法是使碳酸钾 (K2CO3)与一氧化氮 (NO) 反应。该反应产生副产物 KNO2、二氧化碳 (CO2) 和氮气 (N2)。获得一氧化氮既困难又昂贵,因此这种方法较少使用。
反应方程式为:
2 K2CO3 + 2 NO → 2 KNO2 + 2 CO2 + N2
KNO2 可以通过使用 SO2 或 FeSO4 等还原剂氧化 KNO3 来获得。
该反应产生副产物 KNO2、水和还原剂的还原形式。科学家使用这种方法的频率较低,通常将其保留用于小规模的实验室合成。
与二氧化硫的反应方程式为:
2 KNO3 + 3 SO2 + H2O → 2 KNO2 + 3 H2SO4
亚硝酸钾的用途
KNO2 由于其化学特性而具有多种工业和实验室应用。 KNO2 的一些常见用途包括:
- 食品防腐:用作腌肉中的防腐剂,以防止有害细菌的生长并延长其保质期。
- 化学工业:用作生产多种化学品的中间体,如亚硝酸、重氮化合物和有机亚硝酸盐。
- 农业:由于其高水溶性和释放氮的能力,用作肥料和土壤改良剂。
- 实验室试剂:在多种实验室应用中用作试剂,例如伯胺的检测和重氮盐的制备。
- 医药用途:因与氰化物离子反应生成无毒的氰化高铁血红蛋白,用于治疗氰化物中毒。
- 摄影:用作摄影显影剂的添加剂,以提高显影图像的质量和清晰度。
- 玻璃工业:在玻璃工业中用作漂白剂,以去除玻璃产品中不需要的颜色。
问题:
什么是亚硝酸钾?
答:KNO2 是一种无机化合物,常用于各种工业和实验室应用。
问:亚硝酸钾的化学式是什么?
答:亚硝酸钾的化学式是KNO2。
问:NH4OH 与 HNO3 反应生成什么盐? KNO2、NaNO3、NH4NO3 或 NH4NO2?
答:NH4OH 与 HNO3 反应时,生成的盐是 NH4NO3。
问:KNO2 是酸还是碱?
答:KNO2 是一种碱性化合物。
问:分子式为 KNO2 的化合物的名称是什么?
答:分子式为KNO2的化合物的名称是亚硝酸钾。
问:KNO2 是弱碱吗?
答:KNO2 被认为是弱碱。
问:KNO2 是酸性还是碱性?
答:KNO2 本质上是碱性的,可以作为温和的还原剂。
