二氧化碳溶解在水中时会形成碳酸 (H2CO3),它在调节海洋 pH 值和控制岩石风化方面发挥着至关重要的作用。
| 国际纯粹和应用化学联合会名称 | 碳酸 |
| 分子式 | 二氧化碳 |
| CAS 号 | 463-79-6 |
| 同义词 | 空气有酸味;空气有酸味; H2CO3;氧化二亚甲基甲烷;酸性碳酸盐;羟基酮;二羟基甲酮 |
| 乙酰胆碱 | InChI=1S/CH2O3/c2-1(3)4/h(H2,2,3,4) |
碳酸化学式
碳酸的化学式是H2CO3,这表明它由两个氢原子、一个碳原子和三个氧原子组成。该公式还显示了分子中原子的比例,这对于确定涉及碳酸的化学反应的化学计量很重要。
碳酸的摩尔质量
碳酸的摩尔质量约为 62.03 g/mol。它是二氧化碳溶解在水中时形成的弱酸,负责调节海洋的 pH 值。碳酸的摩尔质量对于计算溶液中达到特定 pH 值所需的酸量以及确定二氧化碳在水中的溶解量非常重要。
碳酸的沸点
碳酸没有明确的沸点,因为它在达到沸点之前会分解成水和二氧化碳。然而,在大气压力下,碳酸在大约 333 K (60 °C) 的温度下分解成水和二氧化碳。
碳酸的熔点
碳酸也没有明确的熔点,因为它在达到熔点之前会分解成水和二氧化碳。然而,在大气压下,碳酸在大约 273 K (-0.15 °C) 的温度下分解成水和二氧化碳。
碳酸密度g/ml
室温 (25°C) 下碳酸的密度约为 1.67 g/mL。该值可能会根据溶液的浓度以及环境的温度和压力而变化。
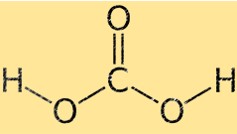
碳酸的结构
碳酸具有四面体分子几何形状,碳原子位于中心,周围的四个原子(两个氧和两个氢)位于四面体的角上。两个氧原子通过双键与碳原子连接,而两个氢原子通过单键连接。
碳酸的分子量
碳酸的分子量为62.03 g/mol。该值是通过将氢 (H)、碳 (C) 和氧 (O) 构成元素的原子量相加计算得出的。
| 外貌 | 无色液体或结晶固体 |
| 比重 | 1.67克/立方厘米 |
| 颜色 | 无色 |
| 闻 | 无味 |
| 摩尔质量 | 62.03 克/摩尔 |
| 密度 | 室温 (25°C) 下为 1.67 克/毫升 |
| 融合点 | 在约 273 K (-0.15 °C) 时分解 |
| 沸点 | 在约 333 K (60°C) 时分解 |
| 闪点 | 不适用 |
| 水中溶解度 | 完全溶解 |
| 溶解度 | 溶于水、乙醇、甲醇 |
| 蒸汽压力 | 不适用 |
| 蒸气密度 | 不适用 |
| 酸度 | 3.6(第一次解离) |
| 酸碱度 | 5.6(0.1M溶液中) |
碳酸 安全与危险
碳酸 (H2CO3) 通常被认为是安全的,但在某些情况下可能会造成一些危险。接触 H2CO3 会刺激眼睛、皮肤和呼吸系统,并导致咳嗽、喘息和呼吸短促。摄入 H2CO3 会导致胃部不适、恶心和呕吐。 H2CO3也是一种弱酸,可以与某些金属(例如铝和锌)反应,产生易燃的氢气。处理或使用 H2CO3 时,应采取适当的安全预防措施,包括穿着防护服和充分通风。如果接触,应立即就医。
| 危险符号 | 没有任何 |
| 安全说明 | 无毒 |
| 联合国识别号 | 1824年 |
| 海关编码 | 28111990 |
| 危险等级 | 8 – 腐蚀性物质 |
| 包装组别 | 三、 |
| 毒性 | 低毒 |
碳酸合成方法
H2CO3 可以通过不同的方法合成。一种常见的方法是在催化剂存在下使二氧化碳(CO2)与水(H2O)反应。这个过程称为水合,产生碳酸:
CO2 + H2O → H2CO3
另一种合成碳酸的方法包括使碳酸钙 (CaCO3) 与酸(例如盐酸 (HCl))反应。这个过程称为酸化,产生碳酸:
CaCO3 + 2HCl → CaCl2 + CO2 + H2O
草酸和碳酸盐(例如碳酸钠 (Na2CO3))之间的反应可以合成碳酸。该过程产生碳酸和盐,例如草酸钠:
H2C2O4 + Na2CO3 → 2H2CO3 + Na2C2O4
索尔维工艺通过碳酸钠 (Na2CO3) 与二氧化碳在水存在下反应产生碳酸和碳酸氢钠。
2NaHCO3 + CO2 → Na2CO3 + H2CO3
总的来说,有多种方法可用于合成碳酸,每种方法都有其自身的优点和局限性。方法的选择取决于多种因素,例如所需的产品纯度、原材料的可用性以及所需的生产规模。
碳酸的用途
碳酸 (H2CO3) 是一种多功能化合物,在工业、医学和日常生活中有着多种用途。 H2CO3 的一些主要用途包括:
- 碳酸饮料:H2CO3 是苏打水和啤酒等碳酸饮料特有的嘶嘶声的化合物。
- H2CO3 可缓冲各种工业过程中的 pH 值,例如水处理和食品加工。
- 它通过置换氧气并防止燃烧来抑制火灾。
- H2CO3 可以抑制某些类型食品中细菌和霉菌的生长,从而保护它们。
- 它充当温和的清洁剂,特别是去除矿物质沉积物。
- 医疗保健专业人员在某些应用中使用 H2CO3,包括治疗某些皮肤病变以及在肺功能测试期间诱导支气管收缩。
- 焊工使用 H2CO3 作为保护气体,以防止氧化并产生更清洁的焊缝。
总的来说,碳酸是一种有用且用途广泛的化合物,在各个领域都有广泛的应用。
问题:
问:碳酸是强酸吗?
答:碳酸是一种弱酸,这意味着它在水中仅部分解离产生氢离子 (H+) 和碳酸氢根离子 (HCO3-)。其酸解离常数(Ka)较低,表明它在水中不完全解离。
问:二氧化碳是酸性的吗?
答:二氧化碳 (CO2) 本身并不是酸性的,因为它是一种中性化合物,在水中不会产生氢离子 (H+)。然而,当CO2溶解在水中时,它可以与水分子反应形成碳酸,这是一种弱酸。该反应会导致 pH 值降低,使溶液呈酸性。因此,尽管二氧化碳本身不呈酸性,但与水反应时会导致溶液呈酸性。
