碳酸钾 (K2CO3) 是一种白色、无味粉末,常用于肥皂、玻璃和陶瓷的生产。还可用作食品添加剂和医药工业的缓冲剂。
| 国际纯粹和应用化学联合会名称 | 碳酸钾 |
| 分子式 | 碳酸钾 |
| CAS 号 | 584-08-7 |
| 同义词 | 碳酸、二钾盐;珍珠灰;钾肥;牙垢盐;碳酸氢钾;碳酸氢钾 |
| 乙酰胆碱 | InChI=1S/CH2O3.2K/c2-1(3)4;;/h(H2,2,3,4);;/q;2*+1/p-2/fCO3.2K/q-2;米 |
碳酸钾性质
碳酸钾配方
碳酸钾的化学式是K2CO3。该公式表示化合物中每种元素的确切原子数。该公式可用于计算化合物的摩尔质量和其他性质。
碳酸钾 摩尔质量
K2CO3 的摩尔质量为 138.21 g/mol。这意味着一摩尔 K2CO3 含有 138.21 克该化合物。摩尔质量对于确定特定反应或实验需要多少物质非常重要。它还用于将物质的质量转换为摩尔数。
碳酸钾的沸点
K2CO3 的沸点相对较高,为 1,620 °C (2,948 °F)。这使其可用于玻璃和陶瓷生产等高温应用。沸点是物质从液体转变为气体的温度。
碳酸钾熔点
K2CO3 的熔点为 891°C (1,636°F)。这种相对较高的熔点是由于该化合物的离子性质。加热时,钾离子和碳酸根离子之间的离子键必须断裂,物质才会熔化。
碳酸钾密度 g/mL
K2CO3 的密度在室温下为 2.43 g/mL。这意味着一定体积的K2CO3具有一定的质量。物质的密度是一个重要的特性,可以用来识别物质并计算物质在给定空间中的质量或体积。
碳酸钾分子量
K2CO3的分子量为138.21 g/mol。这是一摩尔化合物的质量,这在许多化学计算中很重要。
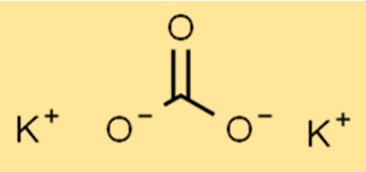
碳酸钾的结构
K2CO3具有离子结构,分子式为K2CO3。钾离子 (K+) 和碳酸根离子 (CO32-) 通过离子键结合在一起。碳酸根离子是由一个碳原子和三个氧原子组成的多原子离子。
| 外貌 | 白色结晶粉末 |
| 比重 | 2.43 |
| 颜色 | 白色的 |
| 闻 | 无味 |
| 摩尔质量 | 138.21 克/摩尔 |
| 密度 | 2.43克/毫升 |
| 融合点 | 891°C (1,636°F) |
| 沸点 | 1620°C (2948°F) |
| 闪点 | 不适用 |
| 水中溶解度 | 20°C 时为 112 克/100 毫升 |
| 溶解度 | 溶于水、甘油和醇 |
| 蒸汽压力 | 室温下可忽略不计 |
| 蒸气密度 | 不适用 |
| 酸度 | 上午 10:33 |
| 酸碱度 | 11.5(10克/升水溶液) |
碳酸钾的安全和危险
K2CO3 通常被认为可安全用于工业和家用产品。然而,它可能会刺激皮肤和眼睛,吸入粉末可能会引起呼吸道刺激。长时间接触高浓度的 K2CO3 粉尘会导致肺部损伤。处理该化合物时,务必佩戴适当的个人防护装备,包括手套、护目镜和口罩。 K2CO3 既不易燃又不易爆炸,但它可以与酸反应产生二氧化碳,这在密闭空间中可能很危险。如果吞咽或接触皮肤或眼睛,请立即就医。
| 危险符号 | 没有任何 |
| 安全说明 | 戴上手套、护目镜和口罩。避免长时间接触皮肤和眼睛。不要吸入粉末。 |
| 联合国识别号 | 联合国1863 |
| 海关编码 | 2836.40.00 |
| 危险等级 | 不危险 |
| 包装组别 | 不适用 |
| 毒性 | 碳酸钾不被认为是有毒的,但高浓度时会引起呼吸道和皮肤刺激。长时间暴露在高浓度的灰尘中会导致肺部损伤。 |
碳酸钾的合成方法
多种方法可以合成K2CO3
常见的方法是使氢氧化钾与二氧化碳反应。
为了防止二氧化碳逸出,该反应可以在密闭容器中进行。
另一种方法涉及使氯化钾与碳酸钠在水溶液中反应。生成的 K2CO3 从溶液中沉淀出来,可以通过过滤收集。
合成 K2CO3 的另一种方法是在木炭存在下使硫酸钾与碳反应。历史上,化学家使用勒布朗工艺在工业规模上生产 K2CO3。然而,由于环境问题,这一过程如今已很少见,因为它会释放二氧化硫。
K2CO3 可以通过将碳酸氢钾加热到高温来合成,使其分解成 K2CO3 和二氧化碳。烘箱或烘箱可以进行该反应。
碳酸钾的用途
K2CO3因其独特的性能在各行业有着广泛的应用。它的一些常见用途包括:
- 玻璃生产:用作助熔剂,降低二氧化硅和其他成分的熔点。
- 食品工业:用作食品添加剂调节酸度和烘焙中的离去剂。
- 肥皂和洗涤剂:也用于制造肥皂和洗涤剂作为水软化剂。
- 医药工业:在药物制剂中用作缓冲剂。
- 肥料:也用作农业肥料,为植物提供钾。
- 陶瓷生产:用作助熔剂,降低烧成温度,提高成品质量。
- 烟花:用于制作烟花,产生紫色火焰。
- 电池:用于电池生产中作为电解液。
- 纺织工业:用作染色剂。
问题:
问: 碳酸钾可溶吗?
答: 是的,碳酸钾易溶于水。
问:K2CO3 溶于水吗?
答:是的,K2CO3 溶于水。事实上,它的溶解度非常高,可以溶解在水中形成透明、无色的溶液。
问:制备 200 ml 2.5 M 溶液需要多少克碳酸钾?
答:要在 200 毫升水中制备 2.5 M K2CO3 溶液,您需要将 33.25 克 K2CO3 溶解在水中。
计算:摩尔浓度 = 摩尔 / 体积(升) 2.5 M = 摩尔 / 0.2 L 摩尔 = 0.5 摩尔质量 = 摩尔 x 摩尔质量 质量 = 0.5 摩尔 x 138.21 g/mol 质量 = 33.25g
问:假设完全解离,0.045 M K2CO3 溶液中 K 离子的浓度是多少?
答:当K2CO3在水中完全解离时,它形成两个K+离子和一个CO3 2- 离子。因此,0.045 M K2CO3 溶液中 K+ 离子的浓度将是 K2CO3 溶液摩尔浓度(0.090 M)的两倍。
