氧化锂(Li2O)是由锂和氧组成的化合物。它表现出强离子特性,由于其高电化学势而广泛应用于电池中。
| 国际纯粹和应用化学联合会名称 | 氧化锂 |
| 分子式 | 氧化锂 |
| CAS 号 | 12142-77-7 |
| 同义词 | 氧化锂(I);氧化二锂;莉西亚;氧锂; UNII-06T3K8P3KU |
| 乙酰胆碱 | InChI=1S/2Li.O |
氧化锂配方
氧化锂配方
二氧化锂的化学式是Li2O。它代表两个锂(Li)原子和一个氧(O)原子的组合。这种简单而稳定的化合物在各种工业应用中至关重要。
氧化锂 摩尔质量
Li2O的摩尔质量约为29.88 g/mol。它是通过将两个锂原子(每个 6.94 g/mol)和一个氧原子(16.00 g/mol)的原子质量相加计算得出的。
氧化锂的沸点
氧化二锂的沸点高达 2,463 摄氏度(4,465 华氏度),令人印象深刻。这种极高的沸点使其可用于需要极高耐热性的行业。
氧化锂的熔点
二锂氧化物的熔点约为 1,450 摄氏度(2,642 华氏度)。当暴露在这个温度下时,它会从固态变成液态,从而促进各种制造过程。
氧化锂密度 g/mL
氧化二锂的密度约为 2.01 g/mL。该值代表每单位体积化合物的质量,对于确定其性能和应用至关重要。
氧化锂的分子量
Li2O的分子量为29.88 g/mol。它是其组成元素锂和氧的原子量之和。该值有利于化学计量计算。
氧化锂的结构
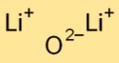
氧化二锂具有简单的离子晶体结构。它由通过强静电力结合在一起的锂阳离子 (Li+) 和氧化物阴离子 (O2-) 组成。这种排列有助于其稳定性和导电性。
氧化锂的溶解度
氧化二锂在水中的溶解度较低。它与水反应形成氢氧化锂,限制其溶解。然而,它在一些非水溶剂和熔盐中表现出一定的溶解度。
总之,氧化二锂是一种具有多种特性和应用的重要化合物。其稳定的结构、高熔点和沸点使其在陶瓷、玻璃制造等行业以及作为特种电池的组成部分具有重要价值。了解其特性使我们能够将其潜力用于各种目的。
| 外貌 | 白色固体 |
| 比重 | 2.01克/毫升 |
| 颜色 | 白色的 |
| 闻 | 无味 |
| 摩尔质量 | 29.88 克/摩尔 |
| 密度 | 2.01克/毫升 |
| 融合点 | 1,450°C (2,642°F) |
| 沸点 | 2463°C (4465°F) |
| 闪点 | 不适用 |
| 水中溶解度 | 与水发生反应 |
| 溶解度 | 水溶性差,呈氢氧化锂形式 |
| 蒸汽压力 | 无法使用 |
| 蒸气密度 | 无法使用 |
| 酸度 | 不适用 |
| 酸碱度 | 不适用 |
请注意,由于 Li2O 的化学性质和行为,闪点、蒸气压、蒸气密度、pKa 和 pH 等一些属性不适用于或不可用于 Li2O。
氧化锂的安全性和危险
氧化二锂会带来一定的安全问题和危险。它与水发生强烈反应,产生氢氧化锂,氢氧化锂具有腐蚀性,会刺激皮肤和眼睛。吸入其粉尘或烟雾可能会引起呼吸道刺激。该化合物不属于剧毒物质,但应小心处理,避免接触皮肤或眼睛。使用氧化二锂时,适当的通风和个人防护装备至关重要。如果意外摄入,需要立即就医。此外,应将其存放在远离不相容物质的地方,以避免任何潜在的火灾或爆炸风险。
| 危险符号 | 腐蚀性 |
| 安全说明 | 与水发生反应。引起皮肤和眼睛刺激。小心轻放。避免吸入灰尘或烟雾。 |
| 联合国识别号 | 不适用 |
| 海关编码 | 2825.70.00 |
| 危险等级 | 8(腐蚀性物质) |
| 包装组别 | 三、 |
| 毒性 | 毒性不大,但需谨慎。避免摄入和接触皮肤或眼睛。 |
氧化锂合成方法
有多种方法可以合成氧化二锂。
一种常见的方法是将锂金属与氧气或空气在高温下反应。在此过程中,氧气促进锂金属的加热,从而形成二锂氧化物。
另一种方法是在高温下热分解锂盐,例如碳酸锂或氢氧化锂。通过将这些盐加热,它们分解产生氧化二锂。
此外,为了生产二锂氧化物,可以使用氢氧化锂作为前体。首先通过加热使其脱水,将其转化为所需的氧化物形式。
另一种技术涉及使用含有锂的矿物或矿石。化学过程从这些天然来源中提取锂化合物,然后将其进一步加工以生产二锂氧化物。
值得注意的是,每种合成方法在成本、效率和纯度方面可能具有特定的优势和挑战。科学家和工程师在选择最合适的氧化二锂生产方法以满足特定工业或研究要求时会考虑这些因素。
氧化锂的用途
氧化二锂 (Li2O) 因其独特的性能而在各个行业有着广泛的应用。以下是一些关键用途:
- 陶瓷行业:氧化二锂是陶瓷的重要组成部分,可提高陶瓷的机械强度和热稳定性。它还可以降低烹饪温度,从而在制造过程中节省能源。
- 玻璃生产:在玻璃工业中,氧化二锂充当助熔剂,降低玻璃的熔化温度并提高其抗化学侵蚀能力,从而生产出高质量的玻璃产品。
- 电池技术:氧化二锂是锂离子电池生产的前体。它有助于电池的正极材料,从而提高其储能能力和整体性能。
- 干燥剂:氧化二锂对水的强亲和力使其成为一种有效的干燥剂,可用于去除某些环境中的湿气,例如空调和气体净化系统中的湿气。
- 冶金:在冶金过程中,氧化二锂通过去除杂质来帮助精炼金属。
- 特种玻璃:用于光学、电子和科学仪器等各种应用的特种玻璃的生产涉及氧化二锂的使用。
- 催化剂:氧化二锂在某些化学反应中充当催化剂,促进反应物转化为所需的产物。
- 核工业:在核工业中,氧化二锂充当中子慢化剂,控制核裂变反应的速率。
应用的多样性凸显了氧化二锂在技术、制造和科学研究进步中的重要性。其独特的性能持续推动各行业的创新,使其成为具有广泛实际用途的有价值的化合物。
问题:
问:什么方程表明氧化锂是由氧和锂反应形成的?
A: 4Li + O2 → 2Li2O
问:氧化锂 Li2O 的摩尔质量是多少?
答:Li2O的摩尔质量约为29.88 g/mol。
问:氧化锂的化学式是什么?
答:氧化二锂的分子式为Li2O。
问:氧化锂是离子型还是共价型?
答:氧化二锂是离子性的。
问:离子键中锂的氧化数是多少?
A:离子键中锂的氧化数为+1。
问:Li2O中锂的配位数?
答:Li2O中锂的配位数为4。
问:Li2O是离子型还是共价型?
答:Li2O是离子型。
问:以下哪个反应与 Li2O 的晶格能 (ΔH°latt) 有关?
A:反应:Li+(g) + O2-(g) → Li2O(s)
问:氧化锂 Li2O 的摩尔质量是多少?
答:Li2O的摩尔质量约为29.88 g/mol。
问:燃烧锂金属(Li)时会产生以下哪种物质? O2、LiO、H2O、Li2O?
答:金属锂(Li)燃烧时会产生Li2O。
问:4.5摩尔Li2O有多少克?
答:4.5 摩尔的 Li2O 大约含有 134.46 克。
