乙烯,又称乙烯,是一种无色、有甜味的易燃气体。它是化学工业的重要组成部分,用于生产塑料、溶剂和其他化学品。
| 国际纯粹和应用化学联合会名称 | 乙烯 |
| 分子式 | C2H4 |
| CAS 号 | 74-85-1 |
| 同义词 | 乙烯、乙烯(错误)、油化气体、Elayl、1,2-二氢乙烯 |
| 乙酰胆碱 | InChI=1S/C2H4/c1-2/h1-2H2 |
乙烯式
乙烯的化学式是C2H4。它代表乙烯分子中存在的原子数量和类型。该公式用于涉及乙烯的化学反应和计算,例如确定反应的化学计量或特定工业过程所需的乙烯量。
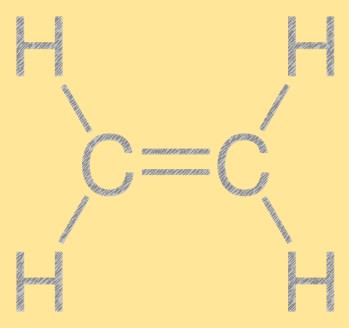
乙烯结构式
乙烯具有简单的线性结构,具有通过双键连接的两个碳原子和每个碳原子连接的四个氢原子。碳-碳双键负责乙烯的反应活性,使其成为化学工业中有用的组成部分。该分子具有平面结构,所有原子都位于同一平面上。
乙烯 摩尔质量
乙烯的摩尔质量为 28.05 g/mol。它是由两个碳原子和四个氢原子组成的简单有机分子,化学式为C2H4。摩尔质量是通过将分子中各个原子的原子质量相加来计算的。
摩尔质量是涉及乙烯的化学反应和计算中的重要参数。它用于确定反应中所需的乙烯量以及可以生产的产物的量。
乙烯的沸点
乙烯的沸点为-103.7°C (-154.7°F)。乙烯在常温常压下是气体,其沸点比水低得多,因此在工业过程中更容易与其他物质分离。
乙烯的沸点取决于样品的压力和纯度。在较高压力下,乙烯的沸点升高。同样,样品中存在的杂质也会导致沸点与预期值不同。
乙烯熔点
乙烯的熔点为-169.2°C (-272.6°F)。乙烯是一种具有线性形状的非极性分子,与许多其他有机化合物相比,它是一种相对简单的分子。这反映在它的低熔点上。
就像沸点一样,乙烯的熔点也会根据样品的纯度而变化。杂质会降低熔点,导致难以获得用于实验目的的纯样品。
乙烯密度g/ml
在标准温度和压力 (STP) 条件下,乙烯的密度为 0.958 g/mL,定义为 0°C (32°F) 和 1 atm 压力。乙烯的密度比空气小,这意味着它可以上升并分散在大气中。
密度是乙烯的重要物理性质,因为它在工业过程中用于确定给定体积空间所需的乙烯量。它还用于计算样品中乙烯的质量。
乙烯的分子量
乙烯的分子量为28.05克/摩尔。它是构成分子的原子的原子量之和。分子量是许多化学计算中的重要参数,特别是在确定反应的化学计量以及所需或产生的反应物和产物的量时。
| 外貌 | 无色气体 |
| 比重 | 20°C (68°F) 时为 0.968 克/毫升 |
| 颜色 | 无色 |
| 闻 | 甜、辣 |
| 摩尔质量 | 28.05 克/摩尔 |
| 密度 | 0°C 和 1 atm 下为 0.958 g/mL |
| 融合点 | -169.2°C (-272.6°F) |
| 沸点 | 1 atm 压力下 -103.7°C (-154.7°F) |
| 闪点 | -136°C (-213°F) |
| 水中溶解度 | 25°C (77°F) 时为 3.5 克/升 |
| 溶解度 | 不溶于水,溶于有机溶剂 |
| 蒸汽压力 | 20°C (68°F) 时为 114.6 kPa |
| 蒸气密度 | 0.97(空气=1) |
| 酸度 | 44 |
| 酸碱度 | 不适用,因为乙烯不是水溶液 |
乙烯安全和危害
乙烯是一种高度易燃气体,可与空气形成爆炸性混合物。如果浓度足够高,它可以在空气中自燃。乙烯也是一种窒息剂,可以在密闭空间中取代氧气,造成令人震惊的危险。
接触液体乙烯或暴露于高浓度气体可能会导致冻伤或烧伤。乙烯无毒,但其燃烧产物,包括一氧化碳和二氧化碳,可能对人体健康有害。
处理乙烯需要采取适当的安全措施,包括足够的通风、个人防护设备和消防安全预防措施。乙烯应贮存和运输于通风良好的地方,远离火源。
| 危险符号 | 易燃气体 (GHS02)、简单窒息剂 (GHS09) |
| 安全说明 | 远离火源——禁止吸烟。仅使用不产生火花的工具。不要吸入气体。仅在室外或通风良好的区域使用。戴防护手套/防护服/护目镜/面部防护罩。 |
| 联合国识别号 | UN 1962(压缩气体) |
| 海关编码 | 2901.21.00 |
| 危险等级 | 2.1(可燃气体) |
| 包装组别 | 不适用 |
| 毒性 | 无毒 |
乙烯合成方法
可以使用多种方法来合成乙烯,包括烃的热裂化和醇的脱水。
在热裂解中,该过程涉及在催化剂存在下将甲烷、丙烷和石脑油等碳氢化合物在高温(500至900°C)下加热,将长链分子分解成较小的分子,从而产生乙烯。产品。
另一种常见的方法是醇脱水,涉及使用氧化铝或二氧化硅等催化剂在高温(250-350℃)下使乙醇或其他醇脱水并形成乙烯和水。
蒸汽裂解是另一种用于生产乙烯的工艺,其中在高温(700-900°C)下将蒸汽添加到碳氢化合物中以生成乙烯和其他产品的混合物。
木材、纸张和塑料等有机材料的热分解也可产生乙烯。
合成乙烯的其他方法包括乙烷氧化脱氢和将甲醇转化为烯烃的过程。
乙烯的用途
乙烯是一种重要的工业化学品,用途广泛。
- 乙烯在聚乙烯(世界上使用最广泛的塑料之一)的生产中发挥着至关重要的作用。人们在包装、管道和建筑材料等各种应用中使用聚乙烯。
- 制造商使用乙烯作为生产其他聚合物(例如聚氯乙烯 (PVC))的关键成分。 PVC 可用于建筑材料、医疗器械和电缆。
- 乙烯在环氧乙烷的制造中也至关重要,而环氧乙烷是制造洗涤剂、溶剂和塑料的重要原材料。
- 制造商使用乙烯生产乙二醇、发动机冷却剂和防冻剂。它也是制造聚酯纤维、薄膜和树脂的原材料。
- 乙烯用作焊接和切割金属的燃料。它还可用作水果和蔬菜的催熟剂。
- 乙烯可用于合成各种有机化合物,包括乙醇和乙醛。
总体而言,乙烯的多功能性使其成为各种工业过程中的重要组成部分,为现代生活的许多方面做出了贡献。
问题:
哪些二烯会在狄尔斯-阿尔德反应中与乙烯反应?
任何含有两个共轭双键的二烯都可以与乙烯发生狄尔斯-阿尔德反应。这种二烯的实例包括1,3-丁二烯和异戊二烯。
乙烯中的氢原子是如何排列的?
在乙烯中,两个碳原子通过双键彼此连接。每个碳原子还与两个氢原子键合,其余化合价由每个碳原子上的两个不共享的电子对占据。每个碳周围的原子排列是三角形的。
当乙烯、C2H4 中发生 sp2 杂化时,会形成多少个 pi 键?
当乙烯中发生sp2杂化时,两个碳原子之间形成π键。 sp2杂化轨道参与碳原子和氢原子之间sigma键的形成,而每个碳原子的p轨道重叠形成pi键。乙烯被归类为不饱和烃,因为它的两个碳原子之间具有双键。该双键由一个西格玛键和一个π键组成,这意味着乙烯比具有相同碳原子数的饱和烃具有更少的氢原子。
