甲酸或HCOOH是一种无色液体,有刺激性气味。它广泛用作防腐剂和抗菌剂以及皮革、纺织品和橡胶的制造。
| 国际纯粹和应用化学联合会名称 | 甲酸 |
| 分子式 | 碳酸氢根 |
| CAS 号 | 64-18-6 |
| 同义词 | 氢羧酸、甲酰酸、氨基酸、甲酰酸、偏碳酸、亚硫酰甲酸等。 |
| 乙酰胆碱 | InChI=1S/CH2O2/c2-1-3/h1H,(H,2,3) |
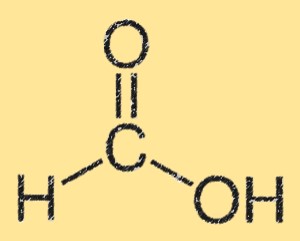
甲酸的结构
甲酸的结构特征是连接到单个碳原子上的羧酸基团(-COOH)。碳原子还与氢原子和氧原子键合。甲酸的结构是平面的并且在羧酸基团之间具有氢键。氢键使其在水中的溶解度很高。
甲酸分子式
甲酸的化学式是HCOOH。它是一种简单的有机化合物,含有一个碳原子、一个氧原子和两个氢原子。甲酸的分子式对于确定其化学和物理性质以及其在不同条件下的行为非常重要。它还用于各种化学计算,例如化学计量和摩尔浓度。
路易斯结构式HCOOH
甲酸(HCOOH)的路易斯结构如下:
H
|
碳=氧
|
哦
碳原子位于结构的中心,具有四个价电子。它与两个氢原子和氧原子形成单键,氧原子具有两对自由电子。氧原子还与另一个带有一对自由电子的碳原子形成双键。路易斯结构表明,由于碳原子和氧原子之间的电负性差异,分子具有极性共价键。
甲酸 摩尔质量
甲酸,也称为甲酸,的摩尔质量为 46.03 g/mol。其化学式为HCOOH,表示含有1个碳原子、1个氧原子和2个氢原子。摩尔质量是确定制备特定浓度溶液所需物质量的重要参数。例如,要制备 1 M 甲酸溶液,需要将 46.03 g 甲酸溶解在 1 升溶剂中。
甲酸的沸点
HCOOH的沸点为100.8°C (213.4°F)。它是一种无色液体,有刺激性气味,极易溶于水。 HCOOH的沸点相对较低,这意味着它很容易汽化和蒸馏。这一特性使其可用于各种工业应用,例如染料、塑料和药品的生产。
HCOOH 熔点
HCOOH的熔点为8.4°C (47.1°F)。它在室温下是固体,可以通过将其冷却到熔点以下来获得其纯净形式。 HCOOH晶体为白色,散发出刺激性气味。与其他羧酸相比,HCOOH 的熔点相对较低,使其成为某些化学反应的有用溶剂。
HCOOH 密度 g/mL
25°C (77°F) 时 HCOOH 的密度为 1,220 g/mL。它比水密度大,相同温度下水的密度为1000 g/mL。 HCOOH的密度是决定其在水和其他溶剂中溶解度的重要性质。这也会影响其在不同条件下的行为,例如温度和压力。
甲酸的分子量
甲酸的分子量为46.03 g/mol。它是一种简单的有机化合物,化学式为HCOOH。分子量是决定物质物理和化学性质的重要参数。它用于计算各种量,例如物质的摩尔数、质量和体积。
| 外貌 | 无色液体 |
| 比重 | 1.22 |
| 颜色 | 无色 |
| 闻 | 英亩 |
| 摩尔质量 | 46.03 克/摩尔 |
| 密度 | 1,220 克/毫升 |
| 融合点 | 8.4℃ |
| 沸点 | 100.8℃ |
| 闪点 | 68℃ |
| 水中溶解度 | 混溶 |
| 溶解度 | 溶于大多数有机溶剂 |
| 蒸汽压力 | 44.5毫米汞柱 |
| 蒸气密度 | 1.5(空气=1) |
| 酸度 | 3.75 |
| 酸碱度 | 2.4 |
甲酸的安全性和危险
HCOOH 会带来多种安全和危险风险。它是一种高度腐蚀性和有毒的物质,接触后会导致严重的皮肤灼伤和眼睛损伤。吸入 HCOOH 蒸气可能会导致呼吸道刺激和肺部损伤。它也是易燃的,在高温下会点燃,造成火灾危险。处理 HCOOH 时应采取适当的安全预防措施,包括使用防护服、手套和护目镜。应储存在阴凉、干燥、通风良好的区域,远离不相容物质,如氧化剂和碱。
| 危险符号 | 腐蚀性、有毒 |
| 安全说明 | 佩戴防护手套和眼睛/面部防护装置。若不慎接触眼睛,请立即用大量清水冲洗并就医。 |
| 联合国识别号 | 联合国1779 |
| 海关编码 | 2915.11.00 |
| 危险等级 | 8(腐蚀性) |
| 包装组别 | 二(中级) |
| 毒性 | LD50 1.8 g/kg(大鼠经口) |
甲酸的合成方法
甲酸可以通过多种方法合成。
- 一种常见的方法涉及一氧化碳和水在催化剂(例如铑或钴)存在下的反应。这就是 Formox 工艺。该过程产生甲酸和氢气。
- 另一种方法涉及在酸性条件下使用强氧化剂(例如铬酸或高锰酸钾)氧化甲醛。该反应产生甲酸和水。
- 合成甲酸的一种方法是甲酸钠与硫酸反应。该反应导致副产物甲酸和硫酸钠的形成。
- 蚂蚁产生甲酸作为一种天然防御机制,可以通过蒸馏从它们的体内获得。
- 另一种合成 HCOOH 的方法涉及二氧化碳与氢气在催化剂(例如亚铬酸铜或氧化锌)存在下反应。这个过程称为 HCOOH 合成反应,产生 HCOOH 和水。
- HCOOH 也可以从天然来源获得,例如荨麻叶,其中含量很少。
总的来说,HCOOH 的合成有多种方法,每种方法都有其优点和缺点。
甲酸的用途
甲酸在各行业有着广泛的应用。
- 甲酸具有防止有害微生物生长的能力,使其成为动物饲料和青贮饲料中防腐剂和抗菌剂的常见选择。
- 它有助于防止饲料和青贮饲料中有害微生物的生长,使其成为有用的添加剂。
- 纺织工业用甲酸作为织物染整剂,以提高色牢度,增加染料与纤维的亲和力。
- 甲酸在乙酸、甲酰胺和甲醇等各种化学品的生产中用作溶剂和中间体。
- 甲酸是皮革工业中使用的鞣剂,有助于改善皮革产品的质感和耐用性。
- 在橡胶生产中,甲酸作为凝固剂来辅助硫化过程。
- 制药工业使用甲酸作为疫苗的防腐剂和医疗设备的消毒剂。
- 此外,甲酸还可用于生产各种药物,包括利尿剂和抗组胺药。
- 甲酸是有机合成反应中的还原剂和聚合反应中的催化剂。
- 甲酸有助于增强各种产品的香气,可用于生产香精和香料。
总体而言,甲酸由于其独特的性质和多功能性而在各个行业中具有多样性的应用。
问题:
问:甲酸是强酸吗?
A. 甲酸是一种弱酸,pKa 值约为 3.75。这意味着它在水中不会完全解离,并且是比盐酸或硫酸等强酸更弱的酸。
问:甲酸和乙酸哪个酸性更强?
A. 甲酸的酸性比乙酸更强。这是由于乙酸中存在甲基,它稳定了共轭碱上的负电荷,使其不易解离。另一方面,甲酸的分子尺寸较小,负电性原子(氧)较强,更容易解离,酸性更强。
问:甲酸是由哪种蚂蚁产生的?
答:甲酸由多种蚂蚁产生,包括木蚁、火蚁和某些无刺蜂。这种酸储存在蚂蚁体内,用作抵御捕食者的防御机制。当受到威胁时,蚂蚁可能会从其毒刺中射出甲酸,或从体内的特殊腺体中释放甲酸。
