亚硫酸钾(K2SO3)是一种由钾、硫和氧组成的化合物。它通常在食品工业中用作防腐剂,以防止变色和腐败。
| 国际纯粹和应用化学联合会名称 | 亚硫酸钾 |
| 分子式 | 硫酸钾 |
| CAS 号 | 10117-38-1 |
| 同义词 | 亚硫酸氢钾;亚硫酸二钾盐;磺酸钾;硫磺和氧化钾 |
| 乙酰胆碱 | InChI=1S/2K.H2O3S/c;;1-4(2)3/h;;(H2,1,2,3)/q2*+1;/p-2 |
亚硫酸钾
亚硫酸钾配方
亚硫酸钾的化学式为K2SO3,表明它含有两个钾原子、一个硫原子和三个氧原子。该化合物是通过氢氧化钾 (KOH) 和二氧化硫 (SO2) 反应形成的。亚硫酸钾是一种离子化合物,这意味着它由带正电的钾离子和带负电的亚硫酸根离子组成。亚硫酸根离子的分子式为SO32-。
亚硫酸钾 摩尔质量
K2SO3 的摩尔质量为 158.26 g/mol。这是通过将公式中每种元素的原子质量相加计算得出的(2 x K 的原子质量)+ S 的原子质量+(3 x O 的原子质量)。化合物的摩尔质量很重要,因为它有助于计算给定反应所需的化合物的量或确定溶液的浓度。
亚硫酸钾的沸点
K2SO3 没有特定的沸点,因为它在达到沸点之前会分解。然而,当加热时,K2SO3 会发生热分解,形成硫酸钾 (K2SO4) 和二氧化硫 (SO2)。分解温度约为390°C。
亚硫酸钾熔点
K2SO3的熔点约为350°C。在此温度下,固体化合物变成液体。然而,如前所述,随着温度升高,K2SO3 会分解。
亚硫酸钾密度 g/mL
室温下 K2SO3 的密度为 2.44 g/mL。密度定义为每单位体积物质的质量。 K2SO3 的高密度表明它是一种相对较重的化合物。该性质对于确定化合物的物理性质(例如其溶解度和反应性)非常重要。
亚硫酸钾分子量
K2SO3 的分子量为 158.26 g/mol。该值表示化合物分子的平均质量。分子量对于计算给定体积或质量中物质的含量很重要,这在化学反应和实验室实验中很有用。
亚硫酸钾结构式
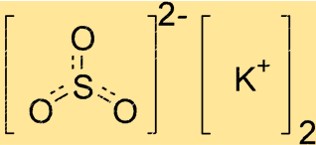
K2SO3 具有晶体结构,这意味着它的原子以重复模式排列。该化合物具有三角形平面几何形状,硫原子位于中心,三个氧原子对称排列在其周围。钾离子位于该结构之外,平衡亚硫酸根离子的负电荷。
亚硫酸钾的溶解度
K2SO3 极易溶于水。在室温下,它可溶于水形成澄清、无色的溶液。 K2SO3 的溶解度归因于其离子性质,这使得它能够在水中解离成其组成离子。 K2SO3的溶解度也受温度影响,随着温度升高,溶解度增大。
| 外貌 | 白色结晶粉末 |
| 比重 | 2.44 |
| 颜色 | 无色 |
| 闻 | 无味 |
| 摩尔质量 | 158.26 克/摩尔 |
| 密度 | 2.44克/毫升 |
| 融合点 | 350℃ |
| 沸点 | 390°C 分解 |
| 闪点 | 不适用 |
| 水中溶解度 | 极易溶于水 |
| 溶解度 | 溶于乙醇和甘油 |
| 蒸汽压力 | 不适用 |
| 蒸气密度 | 不适用 |
| 酸度 | 10.3(亚硫酸) |
| 酸碱度 | ~9(对于 0.1 M 溶液) |
亚硫酸钾的安全和危险
如果采取适当的预防措施,K2SO3 的处理和使用相对安全。然而,如果处理不当,可能会带来危险。如果该化合物接触到皮肤、眼睛和呼吸系统,可能会刺激这些身体部位。如果摄入 K2SO3,也会引起胃肠道问题。此外,该化合物在接触热或火焰时会造成潜在的火灾和爆炸危险。因此,在使用 K2SO3 时应采取适当的安全措施,例如穿戴防护装备并将化合物存放在远离热源和火源的地方。
| 危险符号 | 骷髅和交叉骨 |
| 安全说明 | 有毒,吞咽有害,刺激皮肤和眼睛 |
| 联合国识别号 | 联合国2697 |
| 海关编码 | 283210 |
| 危险等级 | 6.1(有毒物质) |
| 包装组别 | II(中等危险) |
| 毒性 | 口服 (LD50):345 mg/kg(大鼠) |
亚硫酸钾的合成方法
K2SO3可以通过不同的方法合成,包括氢氧化钾与二氧化硫或硫磺反应、碳酸钾与二氧化硫反应以及亚硫酸氢钾与氢氧化物反应。钾。
在第一种方法中,氢氧化钾溶液在水存在下与二氧化硫气体反应形成K2SO3。在第二种方法中,将碳酸钾和二氧化硫的混合物加热至高温以产生K2SO3。第三种方法是将亚硫酸氢钾与氢氧化钾混合以产生 K2SO3 和水。
合成 K2SO3 的另一种常见方法是二氧化硫与钾盐(例如氯化钾)在连二亚硫酸钠或硫酸铁 (II) 等还原剂存在下反应。该方法通常用于工业环境中生产大量 K2SO3。
亚硫酸钾的用途
K2SO3 由于其化学性质而在不同行业中有多种应用。以下是 K2SO3 的一些常见用途:
- 食品饮料行业:用作食品防腐剂,防止酒、干果、虾等食品腐败变色。
- 摄影:用作照相定影剂,防止胶片进一步显影,使图像永久化。
- 水处理:用作还原剂,去除水中的氯并处理废水。
- 造纸工业:在造纸过程中用作漂白剂,去除杂质、增白纸浆。
- 纺织工业:用作还原剂,去除织物上多余的染料,使纺织品增白。
- 化学工业:在化学反应中用作还原剂,将氧化剂转化为还原剂。
- 医药工业:用于某些医学治疗,以预防或缓解某些病症的症状。
问题:
问:亚硫酸钾的化学式是什么?
答:亚硫酸钾的分子式是K2SO3。
问:硫酸钾是亚硫酸盐吗?
答:不,硫酸钾不是亚硫酸盐。它是由钾、硫和氧组成的盐,化学式为K2SO4。
问:H2SO4 与 NaOH 反应生成什么盐? K2SO3、Na2SO4、Na2SO3、K2SO4
答:当 H2SO4 与 NaOH 反应时,生成的盐是 Na2SO4。
问:99.6 毫克 Na2SO3 中含有多少个 SO32-离子?
Na2SO3 的摩尔质量为 126.05 g/mol。答:要计算 SO32- 离子的数量,我们首先需要找到 Na2SO3 的摩尔数:99.6 mg / 126.05 g/mol = 0.000789 mol。由于 Na2SO3 每个分子含有两个 SO32- 离子,因此 0.000789 mol Na2SO3 中 SO32- 离子的数量为 0.000789 mol x 2 = 0.00158 mol。因此,99.6 mg Na2SO3 中有 0.00158 mol x 6.022 x 10^23 ions/mol = 9.52 x 10^20 SO32- 离子。
问:99.6 毫克 Na2SO3 中有多少个钠离子? Na2SO3 的摩尔质量为 126.05 g/mol。
答:要计算钠离子的数量,我们首先需要找到Na2SO3的摩尔数:99.6 mg / 126.05 g/mol = 0.000789 mol。由于每个Na2SO3分子含有两个钠离子,因此0.000789摩尔Na2SO3中钠离子的数量为0.000789mol x 2 = 0.00158mol。因此,99.6 mg Na2SO3 中有 0.00158 mol x 6.022 x 10^23 ions/mol = 9.52 x 10^20 钠离子。
问:Na2SO3 的化学名称是什么?
答:Na2SO3 的化学名称是亚硫酸钠。
问:分子式为Na2SO3的化合物的名称是什么?
答:分子式为Na2SO3的化合物的名称是亚硫酸钠。
