Le catalyseur Wilkinson ou RhCl(PPh3)2 est un catalyseur homogène très actif utilisé en synthèse organique, notamment pour les réactions d’hydrogénation. Il se compose d’un complexe de rhodium avec des ligands phosphine.
| Nom UICPA | Chloridotris(triphénylphosphine)rhodium(I) |
| Formule moléculaire | C54H45ClP3Rh |
| Numero CAS | 14694-95-2 |
| Synonymes | Complexe de chlorure de rhodium triphénylphosphine, catalyseur de Wilkinson, RhCl(PPh3)3, complexe de chlorure de rhodium(I) triphénylphosphine, chlorure de rhodium triphénylphosphine, chlorure de rhodium triphénylphosphine |
| InChI | InChI=1S/2C18H15P.2ClH.Rh/c21-4-10-16(11-5-1)19(17-12-6-2-7-13-17)18-14-8-3-9- 15-18;;;/h21-15H;2*1H;/q;;;;+3/p-3 |
Wilkinson Catalyseur Masse molaire
La masse molaire du catalyseur Wilkinson, également connu sous le nom de RhCl(PPh3)2, est 925,08 g/mol. Cette valeur est dérivée de la somme des masses atomiques des éléments constitutifs du complexe, parmi lesquels le rhodium, le chlore, le carbone, l’hydrogène et le phosphore. La masse molaire du catalyseur Wilkinson est un paramètre important pour déterminer la quantité de catalyseur nécessaire pour une réaction particulière.
Point d’ébullition du catalyseur Wilkinson
Le catalyseur Wilkinson est généralement utilisé comme catalyseur homogène et n’a donc pas de point d’ébullition bien défini. Cependant, sa température de décomposition serait d’environ 180°C. À des températures plus élevées, le catalyseur Wilkinson peut se décomposer et perdre son activité catalytique.
Wilkinson Catalyst Point de fusion
Le point de fusion du catalyseur Wilkinson, également connu sous le nom de RhCl(PPh3)3, est d’environ 207-209°C. Cette valeur peut varier légèrement en fonction de la pureté du catalyseur et de la méthode de mesure.
Densité du catalyseur Wilkinson g/ml
La densité du catalyseur Wilkinson serait d’environ 1,4 g/mL. Cette valeur peut également varier en fonction de la pureté du catalyseur et de la méthode de mesure.
Wilkinson Catalyst Poids moléculaire
Le poids moléculaire du catalyseur Wilkinson, également connu sous le nom de RhCl(PPh3)3, est de 925,08 g/mol. Cette valeur est calculée en additionnant les poids atomiques des atomes constitutifs du complexe. Le poids moléculaire est important pour déterminer la stœchiométrie des réactions impliquant le catalyseur.
Structure du catalyseur Wilkinson
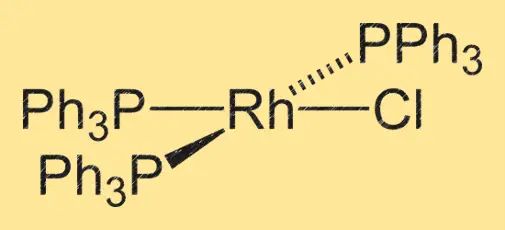
La structure du catalyseur Wilkinson, ou RhCl(PPh3)3, consiste en un atome de rhodium coordonné avec trois ligands triphénylphosphine (PPh3) et un ion chlorure (Cl-). Le complexe a une géométrie plane carrée, avec l’atome de rhodium au centre et les quatre ligands disposés autour de lui dans un plan plat. Les ligands PPh3 sont importants pour stabiliser le complexe et faciliter sa réactivité en synthèse organique.
Formule du catalyseur de Wilkinson
La formule du catalyseur de Wilkinson est RhCl(PPh3)3. Cette formule représente la stœchiométrie du complexe, indiquant qu’il y a un atome de rhodium, un ion chlorure et trois ligands triphénylphosphine dans le complexe. La formule est importante pour déterminer la quantité de catalyseur nécessaire pour une réaction particulière, ainsi que pour calculer le rendement théorique du produit.
| Apparence | Solide cristallin rouge foncé |
| Gravité spécifique | 1,4 g/ml |
| Couleur | Rouge foncé |
| Odeur | Inodore |
| Masse molaire | 925,08 g/mole |
| Densité | 1,4 g/ml |
| Point de fusion | 207-209°C |
| Point d’ébullition | Se décompose à ~180°C |
| Point d’éclair | N’est pas applicable |
| Solubilité dans l’eau | Insoluble |
| Solubilité | Soluble dans les solvants organiques tels que le benzène, le toluène et le chloroforme |
| Pression de vapeur | N’est pas applicable |
| Densité de vapeur | N’est pas applicable |
| pKa | N’est pas applicable |
| pH | N’est pas applicable |
Remarque : Les valeurs présentées dans ce tableau sont approximatives et peuvent varier selon la source d’information.
Le catalyseur de Wilkinson Sécurité et dangers
Lorsque vous travaillez avec le catalyseur de Wilkinson, il est important de prendre les précautions de sécurité appropriées pour éviter les dangers potentiels. Le complexe n’est pas considéré comme hautement toxique, mais il doit néanmoins être manipulé avec précaution pour éviter toute ingestion ou inhalation accidentelle. L’exposition des yeux ou de la peau doit être évitée et un équipement de protection approprié, tel que des gants et des lunettes de sécurité, doit être porté lors de la manipulation du catalyseur. De plus, le catalyseur de Wilkinson doit être stocké dans un endroit frais, sec et bien ventilé, loin des sources de chaleur ou de flammes. L’élimination du catalyseur inutilisé doit être effectuée conformément aux réglementations locales.
| Symboles de danger | Aucun attribué |
| Description de la sécurité | S22 : Ne pas respirer les poussières/fumées/gaz/brouillards/vapeurs/aérosols. S24/25 : Éviter le contact avec la peau et les yeux. S36/37/39 : Porter des vêtements de protection appropriés, des gants et un équipement de protection des yeux/du visage. |
| Numéros d’identification de l’ONU | N’est pas applicable |
| Code SH | 28500090 |
| Classe de danger | N’est pas applicable |
| Groupe d’emballage | N’est pas applicable |
| Toxicité | Faible toxicité ; n’est pas considéré comme hautement toxique, mais doit néanmoins être manipulé avec précaution pour éviter toute ingestion ou inhalation accidentelle |
Méthodes de synthèse du catalyseur de Wilkinson
La méthode couramment utilisée pour synthétiser le catalyseur de Wilkinson implique le traitement du chlorure de rhodium (III) hydraté avec un excès de triphénylphosphine dans de l’éthanol au reflux. Cette méthode peut être réalisée comme suit :
Tout d’abord, dissolvez le chlorure de rhodium (III) hydraté dans l’éthanol pour former une solution. Ajoutez ensuite un excès de triphénylphosphine à la solution et faites refluer le mélange pendant plusieurs heures. Surveillez la solution pour détecter la formation du catalyseur, qui peut être identifié par un changement de couleur du jaune au rouge.
Au cours du processus de synthèse, la triphénylphosphine agit à la fois comme ligand et comme agent réducteur. Trois équivalents de triphénylphosphine se coordonnent avec l’atome de rhodium pour former un complexe stable, tandis que le quatrième équivalent réduit le rhodium(III) en rhodium(I). En conséquence, le produit final de la réaction est RhCl(PPh3)3, avec trois ligands triphénylphosphine attachés au centre rhodium.
Après avoir terminé la synthèse du catalyseur Wilkinson, on peut isoler le catalyseur en filtrant le mélange réactionnel et en le lavant avec de l’éthanol et de l’éther diéthylique. Le solide obtenu est ensuite séché sous vide. Il est essentiel de manipuler le catalyseur avec précaution pour éviter toute exposition à l’air et à l’humidité, qui peuvent compromettre sa pureté et son activité.
Dans l’ensemble, cette méthode constitue un moyen relativement simple et efficace de synthétiser le catalyseur de Wilkinson à grande échelle.
Utilisations du catalyseur de Wilkinson
Le catalyseur de Wilkinson trouve des applications polyvalentes en synthèse organique.
- Il est largement utilisé pour favoriser l’hydrogénation de composés organiques insaturés tels que les alcènes et les alcynes.
- Le catalyseur est crucial dans l’hydroformylation, le processus de conversion des alcènes en alcools linéaires.
- Le catalyseur de Wilkinson est largement utilisé dans la synthèse de produits pharmaceutiques, agrochimiques et de matériaux polymères.
- Il peut favoriser diverses réactions, notamment la formation de liaisons CC et CO, conduisant à la synthèse de molécules organiques complexes.
- Le catalyseur est souvent utilisé en combinaison avec d’autres catalyseurs pour obtenir des résultats de réaction spécifiques.
L’utilisation du catalyseur de Wilkinson conduit à des processus chimiques plus efficaces et plus durables. Cela peut réduire la production de déchets et la consommation d’énergie, en favorisant des pratiques chimiques durables.
Des questions:
Hybridation du catalyseur de Wilkinson
L’hybridation du catalyseur de Wilkinson (RhCl(PPh3)3) implique que l’atome central de rhodium subisse une hybridation pour former des liaisons chimiques avec ses atomes environnants.
L’atome de rhodium dans le catalyseur de Wilkinson a une configuration électronique d8, ce qui signifie qu’il dispose de 8 électrons de valence disponibles pour la liaison chimique. En présence de trois ligands triphénylphosphine (PPh3) et d’un ligand chlorure (Cl), l’atome de rhodium forme un complexe avec une géométrie plan-carré déformée.
L’hybridation de l’atome de rhodium dans le catalyseur de Wilkinson est une hybridation sp3d2. Cela signifie que l’atome de rhodium utilise cinq orbitales atomiques, dont une orbitale 4s, trois orbitales 4p et une orbitale 4d, pour former cinq orbitales hybrides sp3d2.
Dans le catalyseur de Wilkinson, l’atome central de rhodium subit une hybridation sp3d2, résultant en cinq orbitales hybrides. L’une de ces orbitales hybrides forme une liaison sigma avec le ligand chlorure, tandis que les quatre orbitales hybrides restantes forment des liaisons sigma avec les trois ligands triphénylphosphine. Deux des orbitales 4d de l’atome de rhodium forment des liaisons pi avec les ligands, complétant ainsi la sphère de coordination.
Dans l’ensemble, l’hybridation sp3d2 de l’atome de rhodium dans le catalyseur de Wilkinson permet une forte liaison chimique avec ses ligands environnants, ce qui est crucial pour son efficacité en tant que catalyseur homogène dans diverses réactions organiques.
Sélectivité du catalyseur de Wilkinson
Le catalyseur de Wilkinson est un catalyseur hautement sélectif qui est souvent utilisé en synthèse organique pour obtenir des résultats de réaction spécifiques. Le catalyseur présente une sélectivité élevée en raison de ses propriétés électroniques et stériques uniques, qui lui permettent de faire la distinction entre différents types de réactifs et d’intermédiaires.
Dans les réactions d’hydrogénation, par exemple, il a été démontré que le catalyseur de Wilkinson présente une sélectivité élevée pour la réduction des liaisons C=C en présence d’autres groupes fonctionnels, tels que les liaisons C=O et C≡C. Cette sélectivité résulte des propriétés électroniques de l’ion iridium, qui lui permettent d’interagir préférentiellement avec la liaison C=C et de favoriser sa réduction.
De même, dans les réactions d’hydroformylation, le catalyseur de Wilkinson présente une sélectivité pour la formation d’aldéhydes linéaires, plutôt que d’aldéhydes ramifiés ou cycliques. Cette sélectivité provient des propriétés stériques des ligands, qui aident à contrôler l’orientation des réactifs et des intermédiaires au cours de la réaction.
Formule de catalyseur de Wilkinson
La formule du catalyseur de Wilkinson est RhCl(PPh3)3, qui représente le complexe formé entre l’atome de rhodium (Rh), un ion chlorure (Cl) et trois ligands triphénylphosphine (PPh3).
Dans le catalyseur Wilkinson, l’atome de rhodium présente activement un état d’oxydation +1 et forme des liaisons de coordination avec l’ion chlorure et trois ligands triphénylphosphine. Les ligands de l’ion chlorure et de la triphénylphosphine fonctionnent comme des donneurs d’électrons et stabilisent activement le complexe en interagissant avec l’atome de rhodium.
Les ligands triphénylphosphine sont constitués de trois cycles phényle attachés à un atome central de phosphore, qui est lié à l’atome de rhodium. Ces ligands jouent un rôle crucial dans la stabilisation du complexe et en influençant sa réactivité dans diverses réactions organiques.
La formule globale du catalyseur de Wilkinson, RhCl(PPh3)3, indique la stœchiométrie du complexe et la nature des ligands et de l’atome métallique central impliqués.
