Le bleu de bromophénol (BPB) est un indicateur de pH qui devient jaune en dessous de pH 3,0 et bleu au-dessus de pH 4,6. Il est couramment utilisé en biologie moléculaire comme colorant de suivi pour l’électrophorèse de l’ADN.
| Nom UICPA | 3′,3″,5′,5″-tétrabromophénolsulfonephtaléine |
| Formule moléculaire | C19H10Br4O5S |
| Numero CAS | 115-39-9 |
| Synonymes | 3′,3″,5′,5″-tétrabromophénolsulfonphtaléine, TBB, sel de sodium bleu de bromophénol et acide libre de bleu de bromophénol |
| InChI | InChI=1S/C19H10Br4O5S/c20-13-5-1-12(2-6-13)19(11-24)27(25,26)17-9-15(29(21,22)23)7- 3-14(17)18(10-16(19)30(25,26)28)31(4-8-32(25,26)27)33(34)35/h1-10,24H,11H2, (H,21,22,23) |
Bleu De Bromophénol Masse molaire
Le BPB a une masse molaire de 669,96 g/mol. La masse molaire fait référence à la masse d’une mole d’une substance, exprimée en grammes par mole. La masse molaire d’un composé peut être calculée en additionnant les masses atomiques de chacun de ses atomes constitutifs. Le BPB est un composé organique complexe qui contient des atomes de carbone, d’hydrogène, d’oxygène, de soufre et de brome, et sa masse molaire est calculée en additionnant les masses atomiques de chacun de ces éléments dans le composé.
Point d’ébullition du bleu de bromophénol
Le BPB a un point d’ébullition d’environ 600°C. Le point d’ébullition d’une substance est la température à laquelle la pression de vapeur de la substance est égale à la pression atmosphérique. A cette température, le liquide passe à l’état gazeux. Le BPB a un point d’ébullition élevé en raison de sa grande taille et de sa structure complexe, ce qui nécessite une quantité importante d’énergie pour briser les forces intermoléculaires qui maintiennent les molécules ensemble.
Bleu de bromophénol Point de fusion
Le BPB a un point de fusion d’environ 218°C. Le point de fusion d’une substance est la température à laquelle la forme solide de la substance passe à sa forme liquide. Le point de fusion du BPB est relativement élevé en raison des fortes forces intermoléculaires présentes dans le réseau cristallin.
Bleu de bromophénol Densité g/ml
Le BPB a une densité d’environ 1,8 g/ml. La densité est une propriété physique qui décrit la quantité de masse par unité de volume d’une substance. La densité du BPB est relativement élevée en raison de sa structure complexe, ce qui se traduit par une masse par unité de volume élevée.
Bleu De Bromophénol Poids moléculaire
Le poids moléculaire du BPB est de 669,96 g/mol. Le poids moléculaire est la somme des poids atomiques de tous les atomes d’une molécule. Le poids moléculaire d’une substance est utilisé dans divers calculs, tels que la détermination de la quantité de substance nécessaire pour préparer une concentration donnée d’une solution.
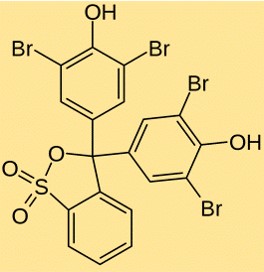
Structure du bleu de bromophénol
Le BPB a une structure sulfonéphtaléine qui contient quatre atomes de brome, deux groupes phénol et un groupe sulfonate. La molécule possède un atome de carbone central qui est connecté à deux groupes phénol et à un groupe sulfonate. La molécule contient également deux atomes de brome attachés à chacun des groupes phénol. Le groupe sulfonate est chargé négativement, ce qui fait du BPB un colorant soluble dans l’eau.
Formule bleue de bromophénol
La formule chimique du BPB est C19H10Br4O5S. La formule représente la composition de la molécule en termes de nombre et de type d’atomes présents. La formule indique que le BPB contient 19 atomes de carbone, 10 atomes d’hydrogène, quatre atomes de brome, cinq atomes d’oxygène et un atome de soufre.
| Apparence | Cristaux ou poudre bleu foncé |
| Gravité spécifique | 1,82 à 1,85 g/cm³ |
| Couleur | Bleu foncé |
| Odeur | Inodore |
| Masse molaire | 669,96 g/mole |
| Densité | 1,8 g/cm³ |
| Point de fusion | ~218 °C |
| Point d’ébullition | ~600 °C |
| Point d’éclair | N’est pas applicable |
| Solubilité dans l’eau | Soluble dans l’eau |
| Solubilité | Soluble dans l’éthanol, le DMSO et le DMF |
| La pression de vapeur | N’est pas applicable |
| Densité de vapeur | N’est pas applicable |
| pKa | 4,0–5,6 |
| pH | 3,0 (jaune)–4,6 (bleu) |
Sécurité et dangers du bleu de bromophénol
Le BPB est un composé relativement sûr lorsqu’il est manipulé correctement. Il n’est pas classé comme cancérigène, mutagène ou tératogène. Cependant, comme pour tous les produits chimiques, il est important de prendre les précautions appropriées lors de la manipulation du BPB. Cela peut provoquer une irritation de la peau et des yeux au contact. L’ingestion peut provoquer des nausées et des vomissements. En cas de contact avec la peau, laver abondamment à l’eau et au savon. En cas de contact avec les yeux, rincer abondamment à l’eau pendant plusieurs minutes. Il est également important d’éviter l’inhalation de poussières ou de vapeurs et d’utiliser un équipement de protection approprié, tel que des gants et des lunettes, lors de la manipulation du BPB.
| Symboles de danger | Aucun |
| Description de la sécurité | S24/25 – Éviter tout contact avec la peau et les yeux |
| S36/37/39 – Porter des vêtements de protection, des gants et des lunettes appropriés | |
| Numéros d’identification de l’ONU | Non réglementé |
| Code SH | 2934.99.9000 |
| Classe de danger | Non classés |
| Groupe d’emballage | N’est pas applicable |
| Toxicité | DL50 (orale, rat) : > 5 000 mg/kg |
Méthodes de synthèse du bleu de bromophénol
Il existe plusieurs méthodes pour synthétiser le bleu de bromophénol.
Une méthode courante est la réaction entre le 3,5-dibromo-4-hydroxybenzaldéhyde et le 4-aminophénol en présence d’hydroxyde de sodium. Cette réaction conduit à la formation de bleu de bromophénol sous forme de solide bleu-vert. Le produit peut être purifié par recristallisation dans l’eau ou l’éthanol.
Une autre méthode implique la réaction entre le 4-diméthylaminobenzaldéhyde et l’acide 3,5-dibromosalicylique en présence d’anhydride acétique et d’acide sulfurique. Cette réaction donne du bleu de bromophénol sous forme d’un solide bleu, qui peut être purifié par recristallisation dans l’éthanol.
Une autre méthode implique la réaction entre l’acide 3,5-dibromo-4-hydroxybenzoïque et le 4-aminophénol en présence d’hydroxyde de sodium. Cette réaction conduit à la formation d’un solide bleu-vert, qui peut être purifié par recristallisation dans l’eau ou l’éthanol.
Utilisations du bleu de bromophénol
Le bleu de bromophénol a de nombreuses utilisations dans différents domaines en raison de ses propriétés uniques. Voici quelques-unes des principales utilisations du bleu de bromophénol :
- Coloration biologique : utilisée comme colorant biologique dans les applications d’électrophorèse. Utilisé comme colorant de suivi pour surveiller la progression de la migration des protéines ou des acides nucléiques pendant l’électrophorèse sur gel.
- Indicateur de pH : utilisé comme indicateur de pH, avec une plage de transition entre pH 3,0 et 4,6. Sa couleur passe du jaune au bleu à mesure que le pH de la solution augmente.
- Indicateurs chimiques : Utilisés comme indicateur chimique pour détecter la présence d’acides et de bases faibles dans les solutions. Utilisé pour déterminer le point final des titrages acide-base.
- Réactif de laboratoire : utilisé comme réactif dans les expériences de laboratoire, en particulier celles impliquant la détermination de la concentration en protéines.
- Applications médicales : Utilisé dans les applications médicales comme outil de diagnostic. Utilisé pour tester la présence de protéines dans l’urine ou pour surveiller l’efficacité de la dialyse rénale.
Dans l’ensemble, le bleu de bromophénol est un composé polyvalent avec un large éventail d’applications dans divers domaines, notamment la biologie, la chimie et la médecine.
Des questions:
Q : Pourquoi du bleu de bromophénol est-il ajouté aux échantillons d’ADN individuels ?
R : Le bleu de bromophénol est souvent ajouté à des échantillons d’ADN individuels dans les expériences d’électrophorèse sur gel comme colorant de suivi. Il permet aux chercheurs de suivre la progression de la migration de l’ADN à travers le gel et d’identifier le moment où l’ADN a atteint l’extrémité du gel.
Q : Selon vous, qu’est-ce qui fait que le bleu de bromophénol dans le tampon d’échantillon apparaît en jaune, et pourquoi ?
R : Le BPB dans le tampon d’échantillon apparaît en jaune car il est sous sa forme acide. Le bleu de bromophénol est un indicateur de pH qui change de couleur du jaune au bleu à mesure que le pH de la solution augmente. Dans le tampon d’échantillon, le pH est généralement acide, ce qui fait apparaître le bleu de bromophénol en jaune.
Q : À quoi sert le colorant bleu de bromophénol présent dans les échantillons ?
R : Le but du colorant bleu de bromophénol présent dans les échantillons est de surveiller la progression de la migration de l’ADN au cours des expériences d’électrophorèse sur gel. Le bleu de bromophénol sert de colorant de suivi, permettant aux chercheurs de voir le mouvement de l’ADN à travers le gel et de déterminer quand l’ADN a atteint l’extrémité du gel. Cela permet de garantir que l’expérience se déroule comme prévu et permet aux chercheurs d’analyser les résultats de l’expérience.
