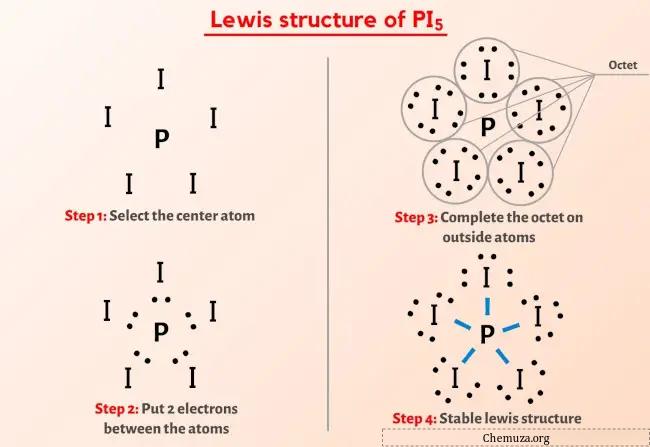
لقد رأيت الصورة أعلاه بالفعل، أليس كذلك؟
اسمحوا لي أن أشرح بإيجاز الصورة أعلاه.
يحتوي هيكل PI5 Lewis على ذرة فوسفور (P) في المنتصف محاطة بخمس ذرات من اليود (I). هناك 5 روابط فردية بين ذرة الفوسفور (P) وكل ذرة اليود (I).
إذا لم تفهم أي شيء من الصورة أعلاه لبنية لويس لـ PI5، فابق معي وستحصل على شرح تفصيلي خطوة بخطوة حول رسم بنية لويس لـ PI5 .
لذلك دعونا ننتقل إلى خطوات رسم بنية لويس لـ PI5.
خطوات رسم هيكل PI5 لويس
الخطوة 1: ابحث عن العدد الإجمالي لإلكترونات التكافؤ في جزيء PI5
من أجل العثور على العدد الإجمالي لإلكترونات التكافؤ في جزيء PI5، تحتاج أولاً إلى معرفة إلكترونات التكافؤ الموجودة في ذرة الفوسفور وكذلك ذرة اليود.
(إلكترونات التكافؤ هي الإلكترونات الموجودة في المدار الخارجي لأي ذرة).
سأخبرك هنا بكيفية العثور بسهولة على إلكترونات التكافؤ للفوسفور وكذلك اليود باستخدام الجدول الدوري.
إجمالي إلكترونات التكافؤ في جزيء PI5
→ إلكترونات التكافؤ المعطاة من ذرة الفسفور:
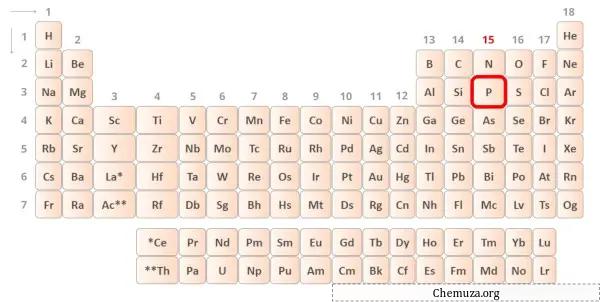
الفوسفور هو أحد عناصر المجموعة 15 من الجدول الدوري. [1] وبالتالي فإن إلكترونات التكافؤ الموجودة في الفوسفور هي 5 .

يمكنك رؤية إلكترونات التكافؤ الخمسة الموجودة في ذرة الفسفور، كما هو موضح في الصورة أعلاه.
→ إلكترونات التكافؤ المعطاة من ذرة اليود:
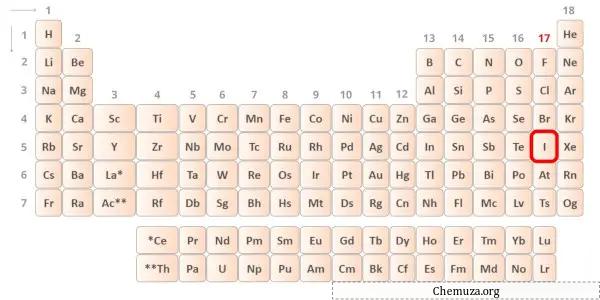
اليود هو عنصر في المجموعة 17 من الجدول الدوري. [2] وبالتالي فإن إلكترونات التكافؤ الموجودة في اليود هي 7 .
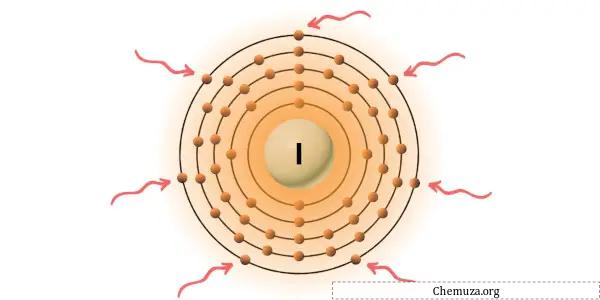
يمكنك رؤية إلكترونات التكافؤ السبعة الموجودة في ذرة اليود، كما هو موضح في الصورة أعلاه.
لذا،
إجمالي إلكترونات التكافؤ في جزيء PI5 = إلكترونات التكافؤ الممنوحة بواسطة ذرة فوسفور واحدة + إلكترونات التكافؤ المتبرع بها من 5 ذرات يود = 5 + 7(5) = 40 .
الخطوة 2: حدد الذرة المركزية
لاختيار الذرة المركزية، يجب أن نتذكر أن الذرة الأقل سالبية كهربية تبقى في المركز.
الآن هنا الجزيء المعطى هو PI5 ويحتوي على ذرات الفوسفور (P) وذرات اليود (I).
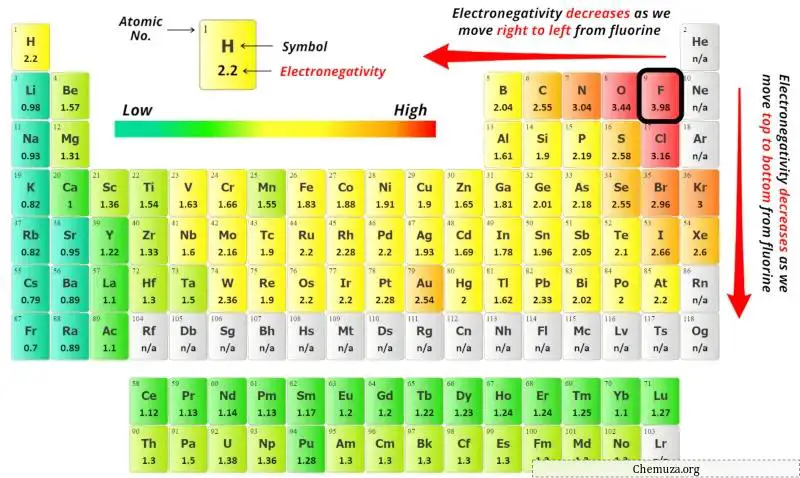
يمكنك رؤية قيم السالبية الكهربية لذرة الفوسفور (P) وذرة اليود (I) في الجدول الدوري أعلاه.
إذا قارنا قيم السالبية الكهربية للفوسفور (P) واليود (I)، فإن ذرة الفسفور تكون أقل سالبية كهربية .
هنا، ذرة الفوسفور (P) هي الذرة المركزية وذرات اليود (I) هي الذرات الخارجية.
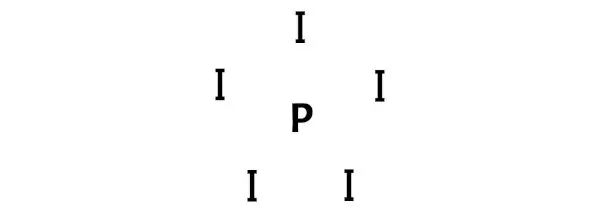
الخطوة 3: قم بتوصيل كل ذرة عن طريق وضع زوج من الإلكترونات بينهما
الآن في جزيء PI5، يجب علينا وضع أزواج الإلكترونات بين ذرة الفوسفور (P) وذرات اليود (I).
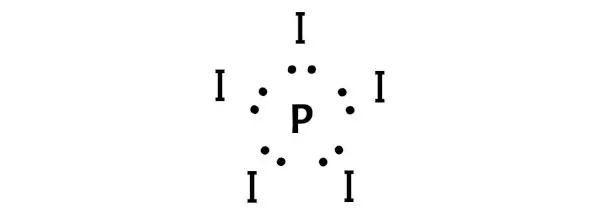
يشير هذا إلى أن الفوسفور (P) واليود (I) مرتبطان كيميائيًا ببعضهما البعض في جزيء PI5.
الخطوة 4: جعل الذرات الخارجية مستقرة
في هذه الخطوة تحتاج إلى التحقق من استقرار الذرات الخارجية.
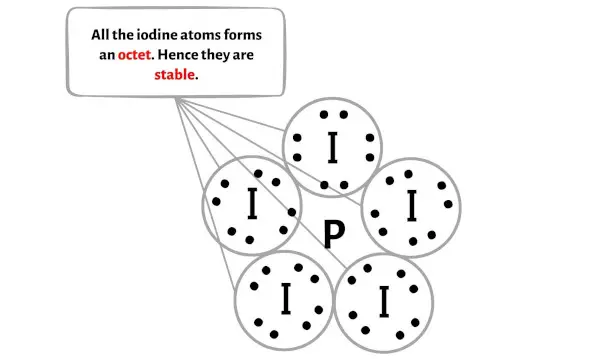
هنا في رسم جزيء PI5 يمكنك أن ترى أن الذرات الخارجية هي ذرات اليود.
تشكل ذرات اليود الخارجية هذه ثمانيًا وبالتالي فهي مستقرة.
بالإضافة إلى ذلك، في الخطوة 1، قمنا بحساب العدد الإجمالي لإلكترونات التكافؤ الموجودة في جزيء PI5.
يحتوي جزيء PI5 على إجمالي 40 إلكترونًا تكافؤًا ويتم استخدام جميع إلكترونات التكافؤ هذه في الرسم البياني أعلاه لـ PI5.
وبالتالي لا يوجد المزيد من أزواج الإلكترونات التي يمكن الاحتفاظ بها في الذرة المركزية.
والآن دعونا ننتقل إلى الخطوة التالية.
الخطوة 5: التحقق من استقرار هيكل لويس
لقد وصلت الآن إلى الخطوة الأخيرة التي تحتاج فيها إلى التحقق من استقرار بنية لويس لـ PI5.
يمكن التحقق من استقرار بنية لويس باستخدام مفهوم الشحن الرسمي .
باختصار، يجب علينا الآن إيجاد الشحنة الرسمية على ذرات الفوسفور (P) وكذلك على ذرات اليود (I) الموجودة في جزيء PI5.
لحساب الضريبة الرسمية، يجب عليك استخدام الصيغة التالية:
الشحنة الرسمية = إلكترونات التكافؤ – (الإلكترونات الرابطة)/2 – الإلكترونات غير الرابطة
يمكنك رؤية عدد الإلكترونات الرابطة والإلكترونات غير الرابطة لكل ذرة من جزيء PI5 في الصورة أدناه.
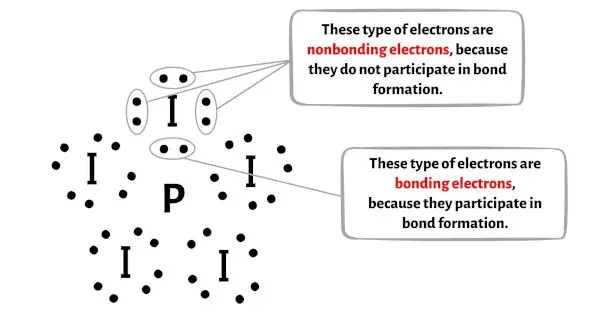
بالنسبة لذرة الفوسفور (P):
إلكترونات التكافؤ = 5 (لأن الفسفور موجود في المجموعة 15)
إلكترونات الرابطة = 10
الإلكترونات غير الرابطة = 0
لذرة اليود (I):
إلكترونات التكافؤ = 7 (لأن اليود موجود في المجموعة 17)
إلكترونات الرابطة = 2
الإلكترونات غير الرابطة = 6
| اتهام رسمي | = | إلكترونات التكافؤ | – | (الإلكترونات الملزمة)/2 | – | الإلكترونات غير الرابطة | ||
| ص. | = | 5 | – | 10/2 | – | 0 | = | 0 |
| أنا | = | 7 | – | 2/2 | – | 6 | = | 0 |
من حسابات الشحنة الرسمية أعلاه، يمكنك أن ترى أن ذرة الفوسفور (P) وكذلك ذرة اليود (I) لها شحنة رسمية “صفر” .
يشير هذا إلى أن بنية لويس المذكورة أعلاه لـ PI5 مستقرة ولا توجد تغييرات أخرى في البنية المذكورة أعلاه لـ PI5.
في بنية لويس النقطية أعلاه لـ PI5، يمكنك أيضًا تمثيل كل زوج من إلكترونات الترابط (:) كرابطة واحدة (|). سيؤدي القيام بذلك إلى بنية لويس التالية لـ PI5.
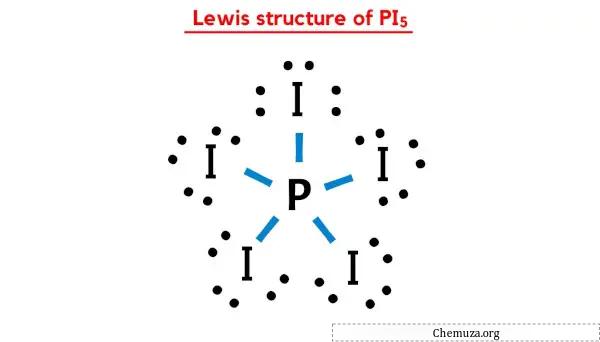
أتمنى أن تكون قد فهمت جميع الخطوات المذكورة أعلاه تمامًا.
لمزيد من التدريب والفهم الأفضل، يمكنك تجربة هياكل لويس الأخرى المدرجة أدناه.
جرب (أو على الأقل شاهد) هياكل لويس هذه لفهم أفضل:
