هيدروكسيد النحاس (Cu(OH)2) هو مادة صلبة زرقاء اللون تتشكل من تفاعل أملاح النحاس مع أيونات الهيدروكسيد. يتم استخدامه كمبيد للفطريات وفي العمليات الكيميائية المختلفة.
| اسم الأيوباك | هيدروكسيد النحاس الثنائي |
| الصيغة الجزيئية | النحاس (أوه)2 |
| CAS رقم | 20427-59-2 |
| المرادفات | هيدروكسيد النحاس؛ ثنائي هيدروكسيد النحاس؛ CuOH2 |
| إنتشي | InChI=1S/Cu.2H2O/h;2*1H2/q+2;;/p-2 |
خصائص هيدروكسيد النحاس
صيغة هيدروكسيد النحاس
الصيغة الكيميائية لهيدروكسيد النحاسيك هي Cu(OH)2. وهو يمثل مزيجًا من أيون النحاس (Cu2+) واثنين من أيونات OH المرتبطة معًا بواسطة روابط أيونية. يُستخدم هذا المركب الصلب الأزرق بشكل شائع في العديد من الصناعات نظرًا لخصائصه الفريدة.
هيدروكسيد النحاس الكتلة المولية
يمكن حساب الكتلة المولية لهيدروكسيد النحاسيك (Cu(OH)2) عن طريق إضافة الكتل الذرية للعناصر المكونة له. يحتوي النحاس (Cu) على كتلة ذرية تبلغ حوالي 63.55 جم / مول، ولكل أيون OH كتلة ذرية مجمعة تبلغ حوالي 17.01 جم / مول. وبالتالي فإن الكتلة المولية لهيدروكسيد النحاسيك تبلغ حوالي 97.55 جم / مول.
نقطة غليان هيدروكسيد النحاس
ليس لهيدروكسيد النحاس نقطة غليان مميزة لأنه يتحلل قبل أن يصل إلى نقطة الغليان. عند تسخينه، فإنه يخضع لتفاعل تحلل حراري لتكوين أكسيد النحاس وبخار الماء.
نقطة انصهار هيدروكسيد النحاس
يحتوي هيدروكسيد النحاس على نقطة انصهار تبلغ حوالي 200 درجة مئوية (392 درجة فهرنهايت). عند درجة الحرارة هذه، تمر المادة الصلبة بمرحلة انتقالية وتتحول إلى الحالة السائلة.
كثافة هيدروكسيد النحاس جم/مل
تبلغ كثافة هيدروكسيد النحاسيك حوالي 3.36 جم / مل. تمثل هذه القيمة كتلة مليلتر واحد من هيدروكسيد النحاسيك، مما يشير إلى تماسكه وتركيزه.
الوزن الجزيئي لهيدروكسيد النحاس
يبلغ الوزن الجزيئي لهيدروكسيد النحاسيك حوالي 97.55 جم / مول. ويتم حسابه عن طريق إضافة الأوزان الذرية لجميع الذرات الموجودة في جزيء هيدروكسيد النحاسيك.
هيكل هيدروكسيد النحاس
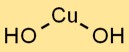
يتخذ هيدروكسيد النحاسيك بنية بلورية، مع أيونات Cu2+ محاطة بأيونات OH- في ترتيب مستو ثلاثي. يساهم هذا الترتيب الشبكي البلوري في استقراره وخصائصه المميزة.
ذوبان هيدروكسيد النحاس
هيدروكسيد النحاسريك له قابلية محدودة للذوبان في الماء. وهو يشكل معلقًا ضعيف الذوبان في الماء، مما يعني أن كمية صغيرة فقط من المركب تذوب في المذيب. يمكن أن تتأثر الذوبان بعوامل مثل درجة الحرارة ودرجة الحموضة.
| مظهر | الأزرق الصلبة |
| جاذبية معينة | ~3.36 جم/مل |
| لون | أزرق |
| يشم | عديم الرائحة |
| الكتلة المولية | ~97.55 جم/مول |
| كثافة | ~3.36 جم/مل |
| نقطة الانصهار | ~200 درجة مئوية (392 درجة فهرنهايت) |
| نقطة الغليان | متحللة |
| نقطة فلاش | لا يوجد |
| الذوبان في الماء | ضعيف الذوبان |
| الذوبان | محدود، ويختلف باختلاف درجة الحرارة ومستويات الرقم الهيدروجيني |
| ضغط البخار | لا يوجد |
| كثافة بخار | لا يوجد |
| pKa | لا يوجد |
| الرقم الهيدروجيني | قلوية (أساسية) |
سلامة ومخاطر هيدروكسيد النحاس
يطرح هيدروكسيد النحاس بعض اعتبارات السلامة والمخاطر. ويعتبر بشكل عام منخفض السمية، ولكنه قد يسبب تهيجًا للجلد والعينين والجهاز التنفسي عن طريق ملامسته أو استنشاقه. وينبغي اتخاذ تدابير وقائية كافية، مثل ارتداء القفازات ونظارات السلامة، عند التعامل مع هذا المركب. في حالة حدوث ابتلاع أو التعرض العرضي، مطلوب رعاية طبية فورية. بالإضافة إلى ذلك، يجب تخزين هيدروكسيد النحاس في منطقة آمنة وجيدة التهوية بعيدًا عن المواد غير المتوافقة. ويجب اتباع إجراءات التخلص المناسبة لتجنب تلوث البيئة. يعد اتباع احتياطات السلامة أمرًا بالغ الأهمية لتقليل المخاطر المحتملة المرتبطة بهيدروكسيد النحاس.
| رموز الخطر | لا أحد |
| وصف الأمان | سمية منخفضة. مهيج |
| أرقام تعريف الأمم المتحدة | غير قابل للتطبيق |
| رمز النظام المنسق | 2825.90.5000 |
| فئة الخطر | لا تصنف على أنها خطيرة |
| مجموعة التعبئة | غير مصنف |
| تسمم | ضعيف |
طرق تصنيع هيدروكسيد النحاس
هناك عدة طرق فعالة لتصنيع هيدروكسيد النحاسيك.
يتضمن النهج الشائع تفاعل ملح النحاس، مثل CuSO4 مع قاعدة قوية مثل هيدروكسيد الصوديوم (NaOH) أو هيدروكسيد البوتاسيوم (KOH) . خلال هذه العملية، تحل أيونات الهيدروكسيد (OH-) من القاعدة محل أيونات الكبريتات (SO4^2-) في CuSO4 ، لتشكل هيدروكسيد النحاسيك (Cu(OH)2) كراسب أزرق.
تتضمن الطريقة الأخرى تفاعل ملح النحاس الثنائي مع الأمونيا (NH3). بإضافة الأمونيا إلى محلول Cu(II)، يترسب هيدروكسيد النحاسيك بسبب اتحاد أيونات Cu2+ مع أيونات هيدروكسيد الأمونيا.
يسمح التحليل الكهربائي بتخليق هيدروكسيد النحاس عن طريق غمر قطب النحاس في محلول إلكتروليت وتطبيق تيار كهربائي مباشر. يؤدي اختزال الماء عند الكاثود إلى توليد أيونات الهيدروكسيد، مما يؤدي إلى تكوين هيدروكسيد النحاسيك.
توفر طرق التوليف النشطة هذه وسائل مراقبة وفعالة لإنتاج هيدروكسيد النحاسيك لمختلف التطبيقات الصناعية والبحثية.
استخدامات هيدروكسيد النحاس
يجد هيدروكسيد النحاس تطبيقات متعددة في مختلف الصناعات بسبب خصائصه الفريدة وطبيعته المتنوعة. بعض الاستخدامات البارزة تشمل:
- مبيد الفطريات: يستخدمه المزارعون على نطاق واسع كمبيد فطري وقائي للسيطرة على الأمراض الفطرية في المحاصيل مثل الفواكه والخضروات ونباتات الزينة.
- الوسطيات الكيميائية: يعمل كوسيط كيميائي قيم في تخليق مركبات النحاس المختلفة، مثل أكسيد النحاس وأملاح النحاس.
- مادة حافظة للخشب: تعمل على معالجة الخشب وتوفير الحماية ضد الحشرات آكلة الخشب والفطريات المسببة للعفن، وبالتالي إطالة عمر الهياكل الخشبية.
- عامل مضاد للبكتيريا: في بعض التركيبات، يعمل كعامل مضاد للبكتيريا، ويجد تطبيقات في البيئات الطبية والرعاية الصحية.
- المعالجة المائية: يساعد على مكافحة الطحالب والأعشاب المائية في البرك والبحيرات والمسطحات المائية الأخرى، مما يحافظ على التوازن البيئي.
- صناعة السيراميك والزجاج: يستخدمه المصنعون كملون لإضفاء ألوان زرقاء وخضراء نابضة بالحياة على منتجات السيراميك والزجاج.
- الألعاب النارية: تساهم في تلوين الألعاب النارية والمشاعل، وتلعب دوراً في تطبيقات الألعاب النارية.
- تصنيع البطاريات: يجد استخدامه في إنتاج البطاريات كمادة قطب كهربائي، مما يسهل تخزين الطاقة.
- الطلاء والطلاءات: تدمجها بعض تركيبات الطلاء لإضفاء خصائص وقائية ومضادة للميكروبات.
يسلط تنوع التطبيقات الضوء على أهمية هيدروكسيد النحاس في صناعات متعددة، مما يجعله مركبًا قيمًا لمختلف الاستخدامات العملية.
أسئلة:
س: هل هيدروكسيد النحاس قابل للذوبان؟
ج: هيدروكسيد النحاسريك له قابلية ذوبان محدودة في الماء، مما يشكل معلقًا ضعيف الذوبان.
س: ما عدد المولات الموجودة في 68 جرامًا من هيدروكسيد النحاس الثنائي Cu(OH)2؟
ج: يوجد ما يقرب من 0.697 مول من Cu(OH)2 في 68 جرامًا.
س: هل هيدروكسيد النحاس II قابل للذوبان في الماء؟
ج: هيدروكسيد النحاسيك II له قابلية ذوبان محدودة في الماء.
س: هل هيدروكسيد الصوديوم وكبريتات النحاس تفاعل كيميائي؟
ج: نعم، يؤدي التفاعل بين NaOH وCuSO4 إلى تكوين هيدروكسيد النحاسيك وكبريتات الصوديوم.
س: هل هيدروكسيد النحاس الثنائي قابل للذوبان؟
ج: هيدروكسيد النحاس الثنائي ذو قابلية ذوبان محدودة في الماء.
س: ما هو لون هيدروكسيد النحاس؟
ج: هيدروكسيد النحاسيك أزرق اللون.
س: هل هيدروكسيد النحاس قلوي؟
ج: هيدروكسيد النحاس مادة قاعدة ولكنها غير مصنفة على أنها قلوية.
س: هل هيدروكسيد النحاس قاعدة قوية؟
ج: لا يعتبر هيدروكسيد النحاس قاعدة قوية.
س: هل Cu(OH)2 قابل للذوبان في الماء؟
ج: Cu(OH)2 له قابلية ذوبان محدودة في الماء.
س: ما عدد المولات الموجودة في 68 جرامًا من هيدروكسيد النحاس الثنائي Cu(OH)2؟
ج: يوجد ما يقرب من 0.697 مول من Cu(OH)2 في 68 جرامًا.
س: كم عدد المولات الموجودة في 34 جرامًا من Cu(OH)2؟
ج: يوجد ما يقرب من 0.3485 مول من Cu(OH)2 في 34 جرامًا.
س: هل يتشكل Cu(OH)2 الصلب عند إذابة 0.075 جم من KOH في 1.0 لتر من Cu(NO3)2 عند 1.0 × 10^−3 M؟
ج: نعم، يتشكل Cu(OH)2 الصلب على شكل راسب بسبب التفاعل بين KOH وCu(NO3)2.
