كبريتيت الصوديوم، المعروف أيضًا باسم Na2SO3، هو مسحوق بلوري أبيض يستخدم عادة كمادة حافظة في صناعة المواد الغذائية وكعامل اختزال في التصوير الفوتوغرافي.
| اسم الأيوباك | كبريتات الصوديوم |
| الصيغة الجزيئية | Na2SO3 |
| CAS رقم | 7757-83-7 |
| المرادفات | كبريتات الصوديوم كبريتيت الصوديوم. حمض الكبريتيك، ملح ثنائي الصوديوم؛ سلفونات الصوديوم. كبريتات الصوديوم |
| إنتشي | InChI=1S/2Na.H2O3S/c;;1-4(2)3/h;;(H2,1,2,3)/q2*+1;/p-2 |
خصائص كبريتيت الصوديوم
صيغة كبريتات الصوديوم
الصيغة الكيميائية لكبريتات الصوديوم هي Na2SO3. وهو يتألف من أيونين Na+ وأيون SO32-. تحمل أيونات Na+ شحنة موجبة بينما تحمل أيونات SO32- شحنة سالبة. كبريتيت الصوديوم هو مركب أيوني يشكل مسحوق بلوري أبيض.
كبريتات الصوديوم الكتلة المولية
الكتلة المولية لـ Na2SO3 هي 126.04 جم/مول. يتم الحصول على هذه القيمة عن طريق إضافة الكتل الذرية لكل عنصر في المركب. تبلغ الكتل الذرية للصوديوم والكبريت والأكسجين 22.99 جم/مول و32.06 جم/مول و15.99 جم/مول على التوالي. تعد الكتلة المولية معلمة مهمة تستخدم في الحسابات المتكافئة ويمكن استخدامها أيضًا لتحديد كمية المادة الموجودة في العينة.
نقطة غليان كبريتات الصوديوم
يحتوي Na2SO3 على نقطة غليان عالية نسبيًا تبلغ 1650 درجة مئوية. ويرجع ذلك إلى الروابط الأيونية القوية بين أيونات Na+ وSO32-، والتي تتطلب كمية كبيرة من الطاقة لكسرها. نقطة الغليان هي درجة الحرارة التي تتحول عندها المادة من الحالة السائلة إلى الحالة الغازية. عند درجة الحرارة هذه، يكون ضغط بخار السائل مساويًا للضغط الجوي.
نقطة انصهار كبريتات الصوديوم
نقطة انصهار Na2SO3 هي 33.4 درجة مئوية. ترجع نقطة الانصهار المنخفضة نسبيًا هذه إلى ضعف القوى الجزيئية بين جزيئات Na2SO3. عند تسخينه، يتم التغلب على القوى بين الجزيئات ويذوب Na2SO3 الصلب إلى سائل.
كثافة كبريتيت الصوديوم جم/مل
تبلغ كثافة Na2SO3 2.633 جم/مل. يتم تعريف الكثافة على أنها كتلة المادة لكل وحدة حجم. تعود الكثافة العالية لـ Na2SO3 إلى طبيعته الأيونية ووجود أيونين صوديوم لكل أيون كبريتيت في بنيته.
الوزن الجزيئي لكبريتات الصوديوم
الوزن الجزيئي لـ Na2SO3 هو 126.04 جم / مول. يتم الحصول على هذه القيمة عن طريق إضافة الأوزان الذرية لكل عنصر في المركب. يعد الوزن الجزيئي معلمة مهمة تستخدم في الحسابات المتكافئة ويمكن استخدامه أيضًا لتحديد كمية المادة الموجودة في العينة.
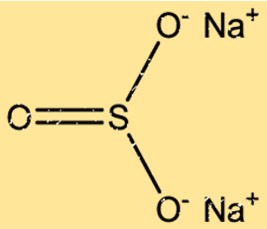
هيكل كبريتيت الصوديوم
يحتوي Na2SO3 على بنية بلورية تحتوي على أيونين Na+ وأيون SO32- مرتبة في نمط متكرر. يتم ترتيب أيونات Na+ في شبكة مكعبة مركزية الوجه، بينما تشغل أيونات SO32- مواقع ثماني السطوح في الشبكة. تؤدي الروابط الأيونية بين أيونات Na+ وSO32- إلى بنية بلورية مستقرة.
ذوبان كبريتيت الصوديوم
Na2SO3 قابل للذوبان بدرجة عالية في الماء، مع قابلية ذوبان تبلغ 22.4 جم / 100 مل عند 20 درجة مئوية. ترجع هذه القابلية العالية للذوبان إلى الطبيعة الأيونية لـ Na2SO3، والتي تسمح لها بالتفكك في الماء وتكوين أيونات Na+ وSO32-. تزداد قابلية ذوبان Na2SO3 في الماء مع زيادة درجة الحرارة، حيث تزداد الطاقة الحركية للجزيئات ويتم إطلاق المزيد من الأيونات في المحلول.
| مظهر | مسحوق بلوري أبيض |
| جاذبية معينة | 2.633 جم/سم3 |
| لون | عديم اللون إلى الأبيض |
| يشم | عديم الرائحة |
| الكتلة المولية | 126.04 جرام/مول |
| كثافة | 2,633 جم/مل |
| نقطة الانصهار | 33.4 درجة مئوية |
| نقطة الغليان | 1650 درجة مئوية |
| نقطة فلاش | غير قابل للتطبيق |
| الذوبان في الماء | قابل للذوبان للغاية |
| الذوبان | قابل للذوبان في الجلسرين، قابل للذوبان بشكل طفيف في الإيثانول |
| ضغط البخار | 0 ملم زئبق عند 20 درجة مئوية |
| كثافة بخار | غير قابل للتطبيق |
| pKa | 6:35 صباحًا |
| الرقم الهيدروجيني | 8.3 – 9.5 (محلول 5%) |
السلامة ومخاطر كبريتيت الصوديوم
يمكن أن يكون Na2SO3 خطيرًا إذا لم يتم التعامل معه بشكل صحيح. قد يسبب تهيج الجلد والعين، وإذا تم تناوله قد يسبب الغثيان والقيء وآلام في البطن. وقد يسبب أيضًا تهيجًا في الجهاز التنفسي في حالة استنشاقه. بالإضافة إلى ذلك، يمكن أن يتفاعل Na2SO3 مع مواد كيميائية أخرى لإنتاج غازات سامة، مثل ثاني أكسيد الكبريت، والذي يمكن أن يكون ضارًا بصحتك. لذلك من المهم ارتداء معدات الحماية الشخصية المناسبة عند التعامل مع Na2SO3 وتجنب التعرض للعينين والجلد والأغشية المخاطية. يجب أيضًا تخزين Na2SO3 في منطقة باردة وجافة وجيدة التهوية بعيدًا عن المواد غير المتوافقة.
| رموز الخطر | شي، أو |
| وصف الأمان | تجنب ملامسة الجلد والعينين. في حالة ملامسة المنتج، اشطفه فورًا بالكثير من الماء واستشر الطبيب. لا يبتلع. تجنب استنشاق الغبار. ارتداء معدات الحماية الشخصية المناسبة. الابتعاد عن الحرارة، والشرر واللهب. |
| معرف | 1384 |
| رمز النظام المنسق | 283210 |
| فئة الخطر | 8- المواد المسببة للتآكل |
| مجموعة التعبئة | ثالثا |
| تسمم | LD50 (عن طريق الفم، الفئران) – 1640 ملغم / كغم؛ LC50 (استنشاق، الفئران) – 63 ملغم/م3 |
طرق تصنيع كبريتيت الصوديوم
يمكن لطرق مختلفة تصنيع Na2SO3.
الطريقة الشائعة هي تفاعل هيدروكسيد الصوديوم مع غاز ثاني أكسيد الكبريت في وجود الماء. ينتج عن التفاعل Na2SO3 والماء كمنتجات ثانوية.
وفي طريقة أخرى، تتفاعل كربونات الصوديوم مع غاز ثاني أكسيد الكبريت في وجود الماء، منتجة Na2SO3 وغاز ثاني أكسيد الكربون. لزيادة إنتاجية Na2SO3، يمكن إجراء هذا التفاعل عند درجات حرارة وضغوط عالية.
يمكن لتفاعل ثنائي كبريتيت الصوديوم مع هيدروكسيد الصوديوم تصنيع Na2SO3. ينتج عن هذا التفاعل Na2SO3 والماء وكلوريد الصوديوم كمنتجات ثانوية.
تتضمن الطريقة الأخرى تفاعل كبريتيد الصوديوم مع غاز ثاني أكسيد الكبريت في وجود الماء لإنتاج Na2SO3 وغاز كبريتيد الهيدروجين.
لتصنيع Na2SO3، يجب معالجة كبريتات الصوديوم بغاز ثاني أكسيد الكبريت في وجود عامل اختزال، مثل الكربون المنشط. ينتج عن هذا التفاعل Na2SO3 وثاني أكسيد الكربون.
كل من هذه الطرق لها مزاياها وعيوبها، واختيار الطريقة يعتمد على عوامل مختلفة، مثل العائد المطلوب، ونقاء وتكلفة المنتج، وتوافر الكواشف والمعدات.
استخدامات كبريتيت الصوديوم
Na2SO3 له العديد من الاستخدامات الصناعية والتجارية الهامة، بما في ذلك:
- التصوير الفوتوغرافي: يستخدم كعامل اختزال وكمادة حافظة في حلول تطوير التصوير الفوتوغرافي. وهذا يساعد على استقرار الصورة ومنع بهتانها.
- معالجة المياه: تستخدم لإزالة الكلور والأكسجين الزائد من الماء في محطات معالجة المياه الصناعية والبلدية. كما أنه يساعد على منع تآكل الأنابيب والمعدات.
- صناعة الورق واللب: يستخدم في إنتاج الورق واللب لتبييض وتقليل محتوى اللجنين في اللب. وهذا يساعد على تحسين جودة ولون الورق.
- صناعة المواد الغذائية: يستخدم كمادة حافظة ومضاد للأكسدة في صناعة المواد الغذائية. يساعد على منع تغير لون الأطعمة وفسادها، مثل الفواكه المجففة والنبيذ والبيرة.
- صناعة النسيج: يستخدم كعامل اختزال وعامل تبييض في صناعة النسيج لإزالة الصبغة الزائدة وتحسين ثبات لون الأقمشة.
- الصناعة الكيميائية: تستخدم كعامل اختزال في التفاعلات الكيميائية المختلفة، مثل إنتاج الأصباغ والمستحضرات الصيدلانية والبوليمرات.
- استخدامات أخرى: يستخدم أيضًا في صناعة المنظفات والمنتجات الجلدية ومنتجات العناية الشخصية، مثل صبغات الشعر والشامبو.
أسئلة:
س: ما هو كبريتيت الصوديوم الطبيعي في الغلاية؟
ج: يتراوح التركيز الطبيعي لـ Na2SO3 في الغلاية عمومًا بين 20 و40 جزءًا في المليون (ppm)، اعتمادًا على ضغط التشغيل وعوامل أخرى.
س: كيف يتم موازنة ثاني أكسيد الكبريت مع هيدروكسيد الصوديوم لتكوين كبريتات الصوديوم والماء؟
ج: لموازنة معادلة تفاعل ثاني أكسيد الكبريت وهيدروكسيد الصوديوم لتكوين Na2SO3 والماء يجب التأكد من وجود عدد متساو من ذرات كل عنصر في طرفي المعادلة. ستكون المعادلة المتوازنة هي SO2 + 2NaOH → Na2SO3 + H2O.
س: ما هو كبريتات الصوديوم؟
ج: Na2SO3 هو مركب بلوري أبيض يستخدم عادة في مختلف التطبيقات الصناعية والتجارية، مثل التصوير الفوتوغرافي ومعالجة المياه وإنتاج الورق وحفظ الأغذية.
س: ما هي صيغة كبريتات الصوديوم؟
ج: صيغة كبريتيت الصوديوم هي Na2SO3.
س: هل أساس كبريتات الصوديوم؟
ج: Na2SO3 هو ملح ذو قاعدة قوية (هيدروكسيد الصوديوم) وحمض ضعيف (حمض الكبريتيك) وبالتالي له خصائص أساسية. ومع ذلك، لا يعتبر بشكل عام أساسًا متينًا.
س: هل كبريتيت الصوديوم مستقر في الماء؟
ج: Na2SO3 مستقر نسبيًا في الماء، لكنه يمكن أن يتحلل تدريجيًا بمرور الوقت، خاصة في وجود الأكسجين أو العوامل المؤكسدة الأخرى.
س: هل كبريتيت الصوديوم قابل للاشتعال؟
ج: Na2SO3 غير قابل للاشتعال، لكنه يمكن أن يتفاعل مع بعض العوامل المؤكسدة لإطلاق ثاني أكسيد الكبريت، وهو مهيج للجهاز التنفسي ويمكن أن يكون قابلاً للاشتعال.
س: أين يمكن شراء كبريتات الصوديوم محليا؟
ج: يمكن شراء Na2SO3 من شركات توريد المواد الكيميائية والموردين الصناعيين وبعض تجار التجزئة المتخصصين. قد يكون متاحًا أيضًا في بعض متاجر الأجهزة المحلية أو مراكز تحسين المنزل.
س: ما هي الأطعمة التي تحتوي على كبريتات الصوديوم؟
ج: يستخدم Na2SO3 بشكل شائع كمادة حافظة في الأطعمة مثل النبيذ والبيرة والفواكه المجففة وبعض اللحوم المصنعة.
س: ما هو المنتج الذي يساوي كبريتات الصوديوم؟
ج: ثنائي كبريتيت الصوديوم مركب مشابه يمكن استخدامه كبديل لـ Na2SO3 في بعض التطبيقات. قد تشمل البدائل الأخرى ميتابيسلفيت الصوديوم أو ميتابيسلفيت البوتاسيوم.
