أيون الكربونات، CO32-، هو أيون سالب الشحنة يتكون من ذرة كربون واحدة، وثلاث ذرات أكسجين، وشحنة إجمالية تبلغ -2. ويوجد عادة في المعادن مثل الكالسيت والدولوميت، وكذلك في المحاليل المائية مثل البيكربونات. إنه يلعب دورًا حاسمًا في التحكم في مستويات الرقم الهيدروجيني في المحيطات والمسطحات المائية الأخرى.
| اسم الأيوباك | أيون الكربونات |
| الصيغة الجزيئية | ثاني أكسيد الكربون- |
| CAS رقم | 497-19-8 |
| المرادفات | حمض الكربونيك، ثالث أكسيد الكربون |
| إنتشي | InChI=1S/CH2O3.2K/c2-1(3)4;/h(H2,2,3,4);/q;+2/p-2 |
خصائص أيونات الكربونات
صيغة الكربونات
يتم تمثيل صيغة أيون الكربونات بواسطة CO3^2-، حيث يمثل C الكربون، ويمثل O الأكسجين، ويمثل الرمز 2- الشحنة السالبة للأيون. تشير هذه الصيغة إلى وجود ثلاث ذرات أكسجين وذرة كربون واحدة في أيون الكربونات، مما يمنحه تركيبه الجزيئي المميز.
شحنة كربونات ثاني أكسيد الكربون
أيون الكربونات، CO3^2-، له شحنة سالبة 2 بسبب وجود ثلاث ذرات أكسجين وذرة كربون واحدة في تركيبته الكيميائية. تنتج الشحنة السالبة من وجود إلكترونات إضافية في أيون الكربونات، مما يجعله أيونًا سالب الشحنة.
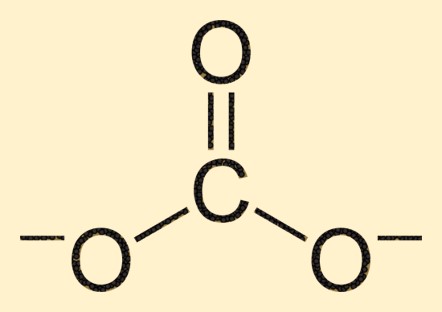
هيكل كربونات
يتكون أيون الكربونات من ذرة كربون في مركزه، محاطة بثلاث ذرات أكسجين في ترتيب مستو ثلاثي. تشكل ذرة الكربون رابطة مزدوجة مع ذرة الأكسجين، بينما ترتبط ذرتا الأكسجين الأخريان بذرة الكربون من خلال روابط فردية. يعطي هذا الهيكل أيون ثاني أكسيد الكربون شكله وخصائصه المميزة.
الوزن الجزيئي لأيون الكربونات
يبلغ الوزن الجزيئي لأيون الكربونات حوالي 60.01 جم/مول، ويتم حسابه بناءً على الأوزان الذرية للعناصر المكونة له (الكربون والأكسجين). الوزن الجزيئي لحمض الكربونيك مهم في تحديد كمية حمض الكربونيك في العينة، وكذلك تحديد خصائصه الفيزيائية والكيميائية.
| مظهر | مسحوق أبيض صلب |
| جاذبية معينة | 2.5 |
| لون | أبيض |
| يشم | لا أحد |
| الكتلة المولية | 100.09 جرام/مول |
| كثافة | 2.83 جم/سم3 |
| نقطة الانصهار | 825 درجة مئوية |
| نقطة الغليان | 1484 درجة مئوية |
| نقطة فلاش | غير قابل للتطبيق |
| الذوبان في الماء | يذوب في الماء |
| الذوبان | قابل للذوبان في الأحماض |
| ضغط البخار | غير قابل للتطبيق |
| كثافة بخار | غير قابل للتطبيق |
| PKa | 10:33 صباحًا |
| الرقم الهيدروجيني | 8.6 |
السلامة ومخاطر أيونات الكربونات
يستخدم أيون الكربونات، CO32-، على نطاق واسع في مختلف الصناعات، ولكن يجب التعامل معه بحذر. استنشاق كميات كبيرة من غبار الكربونات يمكن أن يسبب مشاكل في الجهاز التنفسي، في حين أن تناوله بكميات كبيرة يمكن أن يسبب مشاكل في الجهاز الهضمي. ملامسة الجلد قد تسبب تهيجًا وآفات جلدية. كما أنه قابل للاشتعال ويمكن أن يتفاعل مع المواد الكيميائية الأخرى لإنتاج غازات خطيرة. من المهم اتباع تدابير السلامة، مثل ارتداء معدات الحماية الشخصية وتخزين أيونات الكربونات في حاويات مناسبة، لتقليل مخاطر الحوادث.
| رمز الخطر | لا أحد |
| وصف الأمان | لا يعتبر خطيرًا ولا يرتبط بأي رموز خطر محددة. |
| معرف | لا يوجد |
| رمز النظام المنسق | لا يوجد |
| فئة الخطر | لا يوجد |
| مجموعة التعبئة | لا يوجد |
| تسمم | غير سام |
طرق تصنيع أيون الكربونات
يمكن تصنيع أيونات الكربونات (CO3 2- ) بعدة طرق مختلفة. الطريقة الأكثر شيوعًا لإنتاج أيونات ثاني أكسيد الكربون هي تفاعل ثاني أكسيد الكربون مع الماء. ينتج عن هذا التفاعل محلول حمض الكربونيك، والذي يمكن بعد ذلك تحييده باستخدام مادة قلوية، مثل هيدروكسيد الصوديوم، لإنتاج حمض الكربونيك. يمكن أيضًا إنتاج حمض الكربونيك عن طريق التحليل الكهربائي لمحلول ملحي، حيث تتشكل أيونات الكربونات عند الكاثود. ويمكن أيضًا إنتاج هذه الأيونات في المختبر عن طريق تفاعل كيميائي بين حمض وملح كربونات.
استخدامات أيونات الكربونات
تستخدم الصناعات حمض الكربونيك على نطاق واسع لأغراض مختلفة. عادةً ما يقوم مصنعو مسحوق الخبز ومنتجو مضادات الحموضة وشركات المشروبات بدمج حمض الكربونيك في منتجاتهم. تتحكم صناعة معالجة المياه في مستويات الرقم الهيدروجيني في مياه الشرب وحمامات السباحة باستخدام أيونات الكربونات. تستخدم صناعة البناء والتشييد أيونات ثاني أكسيد الكربون كمكون رئيسي للأسمنت لصنع الخرسانة. ويضيف المزارعون أيونات الكربونات إلى التربة لتحسين قلويتها وتعزيز نمو المحاصيل. تستخدم الصناعة الكيميائية أيونات الكربونات كمحفز وكاشف في التفاعلات الكيميائية المختلفة. تحافظ صناعة المواد الغذائية على الغذاء من خلال دمج أيونات الكربونات. نظرًا لتعدد استخداماتها، تلعب أيونات الكربونات دورًا أساسيًا في العديد من المنتجات والعمليات الصناعية اليومية.
