والفوسجين هو غاز سام يستخدم في العمليات الصناعية وفي الحروب. ويشكل استنشاقه مخاطر صحية خطيرة، ويسبب تلفًا في الجهاز التنفسي ويمكن أن يكون مميتًا.
| اسم الأيوباك | ثنائي كلوريد الكربونيل |
| الصيغة الجزيئية | COCl2 |
| CAS رقم | 75-44-5 |
| المرادفات | ثنائي كلوريد الكربونيك، غاز الفوسجين، كلوريد الكربونيل |
| إنتشي | InChI=1S/CCl2O/c2-1(3)4 |
خصائص الفوسجين
صيغة الفوسجين
الصيغة الكيميائية للفوسجين أو ثاني كلوريد الكربون هي COCl2. ويتكون من ذرة كربون واحدة (C)، وذرة أكسجين واحدة (O)، وذرتين من الكلور (Cl). هذا التركيب الجزيئي ضروري لفهم خصائصه وتفاعلاته.
الكتلة المولية للفوسجين
تبلغ الكتلة المولية لثاني كلوريد الكربون حوالي 98.92 جم / مول. ويتم حسابه عن طريق إضافة الكتل الذرية لمكوناته، وهي الكربون (12.01 جم/مول)، والأكسجين (16.00 جم/مول)، والكلور (35.45 جم/مول لكل منهما).
نقطة غليان الفوسجين
يحتوي ثاني كلوريد الكربون على نقطة غليان منخفضة نسبيًا تبلغ حوالي -23.3 درجة مئوية (-9.94 درجة فهرنهايت). عند درجة الحرارة هذه، يتغير من حالته السائلة إلى الحالة الغازية، وهو أمر بالغ الأهمية لتطبيقه في العمليات الصناعية المختلفة.
نقطة انصهار الفوسجين
نقطة انصهار ثاني أكسيد الكربون منخفضة جدًا، حوالي -118.3 درجة مئوية (-180.94 درجة فهرنهايت). عند درجة الحرارة هذه، يتحول الشكل الصلب لثاني كلوريد الكربون إلى سائل. إن فهم هذه الخاصية مهم للتعامل مع ثاني كلوريد الكربون بأمان.
كثافة الفوسجين جم / مل
تبلغ كثافة ثنائي كلوريد الكربون حوالي 1.432 جم/مل عند درجة حرارة الغرفة (25 درجة مئوية أو 77 درجة فهرنهايت). هذه الخاصية حاسمة في تحديد سلوكها وتفاعلاتها مع المواد الأخرى.
الوزن الجزيئي للفوسجين
الوزن الجزيئي لثاني كلوريد الكربون هو 98.92 جم / مول. هذه القيمة حيوية لمختلف العمليات الحسابية في الكيمياء، بما في ذلك قياس العناصر الكيميائية وتحديد كمية ثاني كلوريد الكربون اللازمة للتفاعلات.
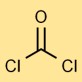
هيكل الفوسجين
يحتوي ثاني كلوريد الكربون على بنية جزيئية خطية، حيث ترتبط ذرة الكربون بشكل مزدوج بذرة الأكسجين وترتبط منفردة بكل ذرة كلور. يؤثر هذا الترتيب على استجابته واستقراره.
ذوبان الفوسجين
ثنائي كلوريد الكربون قليل الذوبان في الماء، حيث تذوب كمية صغيرة فقط من الغاز في السائل. ومع ذلك، فإنه يمكن أن يتفاعل مع الماء لإنتاج حمض الهيدروكلوريك وثاني أكسيد الكربون، مما يجعله خطيرًا في البيئات المائية.
يعد فهم خصائص ثاني كلوريد الكربون أمرًا ضروريًا للتعامل مع المادة الكيميائية واستخدامها بأمان في التطبيقات الصناعية وغيرها من الإعدادات. يجب دائمًا اتخاذ الاحتياطات المناسبة عند التعامل مع هذا المركب السام والمتفاعل لمنع الحوادث والمخاطر الصحية.
| مظهر | غاز عديم اللون |
| جاذبية معينة | 3.428 (غاز) |
| لون | لا يوجد |
| يشم | الاختناق، لاذع |
| الكتلة المولية | 98.92 جرام/مول |
| كثافة | 1,432 جم/مل (سائل) |
| نقطة الانصهار | -118.3 درجة مئوية (-180.94 درجة فهرنهايت) |
| نقطة الغليان | -23.3 درجة مئوية (-9.94 درجة فهرنهايت) |
| نقطة فلاش | لا يوجد |
| الذوبان في الماء | يتفاعل مع الماء |
| الذوبان | يتفاعل مع الماء لينتج حمض الهيدروكلوريك وثاني أكسيد الكربون |
| ضغط البخار | 736 ملم زئبق (25 درجة مئوية) |
| كثافة بخار | 2.98 (الهواء = 1) |
| pKa | لا يوجد |
| الرقم الهيدروجيني | لا يوجد |
توفر هذه الخصائص الفيزيائية والكيميائية معلومات أساسية عن ثاني كلوريد الكربون، مما يسهل التعامل معه بشكل آمن وفهم سلوكه في البيئات المختلفة.
سلامة ومخاطر الفوسجين
يشكل ثاني كلوريد الكربونيك مخاطر كبيرة على السلامة بسبب طبيعته السامة والتفاعلية. عند التعامل مع ثاني كلوريد الكربون، قم بارتداء معدات الحماية الشخصية المناسبة (PPE)، بما في ذلك حماية الجهاز التنفسي والقفازات وحماية العين. التأكد من التهوية الكافية في مناطق العمل لتجنب التعرض عن طريق الاستنشاق. تجنب ملامسة الجلد والعينين لأن ذلك قد يسبب تهيجًا وحروقًا خطيرة. غاز ثاني كلوريد الكربون ليس له رائحة، مما يجعل من الصعب اكتشافه. ولذلك فإن أجهزة المراقبة أمر بالغ الأهمية. إذا تعرضت، اطلب العناية الطبية على الفور. تخزين ونقل ثاني كلوريد الكربون بأمان، وفقًا للوائح وأفضل الممارسات. إن فهم مخاطرها أمر ضروري لمنع الحوادث وحماية صحة الإنسان والبيئة.
| رموز الخطر | جمجمة وعظمتين متقاطعتين |
| وصف الأمان | غاز شديد السمية. تعامل بحذر شديد. استخدم معدات الوقاية الشخصية المناسبة. تجنب الاستنشاق وملامسة الجلد. |
| أرقام تعريف الأمم المتحدة | UN1076 |
| رمز النظام المنسق | 2812.10.0000 |
| فئة الخطر | 2.3 (غاز سام) |
| مجموعة التعبئة | أنا |
| تسمم | الفوسجين شديد السمية ويمكن أن يكون مميتًا عن طريق الاستنشاق أو ملامسة الجلد. استخدام تدابير أمنية صارمة. |
يعد فهم جوانب المخاطر والسلامة لثاني كلوريد الكربون أمرًا بالغ الأهمية للتعامل الآمن ومنع الحوادث. وهو شديد السمية ويشكل مخاطر صحية كبيرة، مما يجعل إجراءات السلامة والاحتياطات المناسبة ضرورية.
طرق تركيب الفوسجين
هناك عدة طرق تسمح بتخليق ثاني كلوريد الكربون.
النهج الشائع هو “عملية الشماس”، حيث يتفاعل غاز الكلور مع أول أكسيد الكربون عند درجات حرارة مرتفعة في وجود محفز مناسب مثل كلوريد النحاس (II) . تتضمن الطريقة الأخرى “الكلورة المباشرة” لأول أكسيد الكربون بغاز الكلور، والتي يتم تسهيلها بواسطة الحديد أو كلوريدات المعادن الأخرى كمحفزات.
يتضمن إنتاج ثاني كلوريد الكربونيك “الكربونيل التأكسدي” لكلوريد الميثيلين أو كلوريد الميثيل، باستخدام الأكسجين ومحفز معدني مثل كلوريد النحاسوز. هناك طريقة أخرى لتصنيع ثاني كلوريد الكربونيك وهي “طريق اليوريا”، الذي يولد ثاني كلوريد الكربون كمنتج ثانوي أثناء إنتاج اليوريا.
ومع ذلك، فمن الضروري أن نلاحظ أن ثاني كلوريد الكربون مادة خطيرة للغاية وأن تركيبها يتطلب أقصى قدر من العناية والخبرة. يجب على العمال إجراء هذه العمليات في بيئات صناعية يتم التحكم فيها بشكل جيد مع اتخاذ تدابير سلامة صارمة ومعدات وقائية لتجنب التعرض للغازات السامة وضمان سلامتهم وسلامة البيئة.
استخدامات الفوسجين
لثنائي كلوريد الكربونيك تطبيقات صناعية مختلفة بسبب خصائصه الفريدة، ولكن من المهم ملاحظة أنه يجب التعامل مع استخداماته بحذر شديد بسبب طبيعته السامة. وهذه بعض استخداماته:
- الوسطيات الكيميائية: يساعد ثاني كلوريد الكربون في إنتاج العديد من المواد الكيميائية الأساسية، بما في ذلك الأيزوسيانات، التي تلعب دورًا أساسيًا في تصنيع رغاوي البولي يوريثان والطلاءات والمواد اللاصقة.
- إنتاج المبيدات الحشرية: يسهل ثاني كلوريد الكربون تخليق بعض المبيدات الحشرية ومبيدات الأعشاب، مما يساهم في حماية المحاصيل ومكافحة الآفات.
- إنتاج البولي كربونات: يعد ثاني أكسيد الكربون عنصرًا حاسمًا في إنتاج بلاستيك البولي كربونات، ويستخدم في مجموعة واسعة من المنتجات، بدءًا من النظارات وحتى زجاجات المياه.
- صناعة النسيج: يدخل ثاني كلوريد الكربون في إنتاج أصباغ محددة ومواد كيميائية أخرى تستخدم في صناعة النسيج.
- إنتاج الرغوة: يلعب ثاني أكسيد الكربون دوراً رئيسياً في صناعة المواد الرغوية، بما في ذلك بعض أنواع الرغوة المستخدمة في العزل.
- المستحضرات الصيدلانية: يعمل ثاني كلوريد الكربون كمادة كيميائية وسيطة في إنتاج بعض الأدوية.
- الأبحاث المعملية: يستخدم الباحثون أحيانًا ثاني كلوريد الكربون في التجارب المعملية.
- إنتاج المطاط الصناعي: يعتبر ثاني أكسيد الكربون جزءاً لا يتجزأ من إنتاج بعض أنواع المطاط الصناعي.
- تنقية المياه: سبق استخدام ثاني كلوريد الكربون بكميات صغيرة لتنقية المياه، ولكن في الوقت الحاضر أصبحت البدائل الأكثر أمانًا أكثر شيوعًا لهذا الغرض.
على الرغم من أن ثاني كلوريد الكربون له استخدامات صناعية مهمة، إلا أن سميته العالية وخصائصه الخطرة تتطلب اتخاذ تدابير سلامة صارمة أثناء المناولة والتخزين والنقل لمنع وقوع الحوادث وضمان رفاهية العمال والناس. البيئة.
أسئلة:
س: ماذا يفعل غاز الفوسجين للإنسان؟
ج: يمكن أن يسبب غاز ثاني كلوريد الكربون إصابة في الجهاز التنفسي، مما يؤدي إلى صعوبة في التنفس وربما وذمة رئوية مميتة.
س: ما هو الفوسجين؟
ج: ثاني أكسيد الكربون مركب كيميائي شديد السمية يستخدم في العمليات الصناعية المختلفة.
س: ما هو غاز الفوسجين؟
ج: غاز ثاني كلوريد الكربون هو الشكل الغازي للمركب الكيميائي المعروف بآثاره الخانقة والسامة على الجهاز التنفسي.
س: ماذا يفعل الفوسجين بالجسم؟
ج: يمكن أن يؤدي ثاني أكسيد الكربون إلى إتلاف الرئتين، مما يسبب تراكم السوائل وضيقًا شديدًا في التنفس.
س: كم مرة يتفاعل جرينارد مع الفوسجين؟
ج: يتفاعل كاشف جرينارد مع ثاني كلوريد الكربون مرة واحدة فقط مكونًا الكيتون.
س: ما هو العضو البشري الذي يهاجمه غاز الكلور والفوسجين؟
ج: غازات الكلور وثاني كلوريد الكربون تهاجم الرئتين بشكل رئيسي.
س: كيف يقتلك غاز الفوسجين؟
ج: يسبب غاز ثاني كلوريد الكربون تهيجًا شديدًا للرئة، مما يؤدي إلى تراكم السوائل والاختناق.
س: من مخترع غاز الفوسجين؟
ج: اكتشف الكيميائي البريطاني جون ديفي غاز ثاني أكسيد الكربون عام 1812.
س: آثار غاز ثاني كلوريد الكربون؟
ج: يمكن أن يتسبب غاز ثاني كلوريد الكربون في تلف الجهاز التنفسي، والوذمة الرئوية، وفي الحالات الشديدة، الوفاة.
س: تركيب لويس لثاني أكسيد الكربون؟
ج: يتكون تركيب لويس لثاني كلوريد الكربون من ذرة كربون مرتبطة بشكل مزدوج بالأكسجين ورابطة واحدة بذرتي الكلور.
س: غاز ثاني كلوريد الكربون الحرب العالمية الأولى؟
ج: تم استخدام ثاني كلوريد الكربون كسلاح كيميائي خلال الحرب العالمية الأولى، مما تسبب في آثار مدمرة على الجنود.
س: متى تم استخدام غاز الفوسجين لأول مرة؟
ج: تم استخدام غاز ثاني كلوريد الكربون لأول مرة كسلاح كيميائي خلال الحرب العالمية الأولى في عام 1915.
س: من أين يأتي الفوسجين؟
ج: يتم إنتاج ثاني أكسيد الكربون عادة عن طريق تفاعل الكلور مع أول أكسيد الكربون أو مركبات أخرى تحتوي على الكربون.
