الميثانول (CH3OH) هو سائل عديم اللون وقابل للاشتعال وله رائحة حلوة. يتم استخدامه كمذيب ووقود ومضاد للتجمد. يمكن أن تكون سامة إذا تم تناولها وتسبب العمى أو الوفاة.
| اسم الأيوباك | الميثانول |
| الصيغة الجزيئية | CH4O |
| CAS رقم | 67-56-1 |
| المرادفات | كحول الميثيل، كحول الخشب، هيدروكسي ميثان، كاربينول، نافثا الخشب، الروح الاستعمارية |
| إنتشي | إنشي=1S/CH4O/c1-2/h2H,1H3 |
ملحوظة: InChI عبارة عن سلسلة طويلة تمثل البنية الفريدة للجزيء. قد لا يتم عرضه بشكل صحيح على بعض الأجهزة.
خصائص الميثانول
الكتلة المولية للميثانول
الكتلة المولية للميثانول هي 32.04 جم / مول. ويتم حسابه عن طريق إضافة الأوزان الذرية لذرات الكربون والهيدروجين والأكسجين في جزيء واحد من الميثانول. هذه القيمة مفيدة لتحديد كمية الميثانول اللازمة لتحضير تركيز معين من المحلول أو لتحديد قياس العناصر الكيميائية للتفاعل الكيميائي.
نقطة غليان الميثانول
تبلغ درجة غليان الميثانول 64.7 درجة مئوية (148.46 درجة فهرنهايت). نقطة الغليان المنخفضة نسبيًا هذه تجعل الميثانول مفيدًا كمذيب في العديد من التطبيقات الصناعية، بما في ذلك إنتاج الفورمالديهايد وحمض الأسيتيك وميثاكريلات الميثيل. ومع ذلك، فإن نقطة غليان الميثانول المنخفضة تجعله أيضًا مادة متطايرة وقابلة للاشتعال، مما قد يشكل مخاطر على السلامة أثناء التخزين والمناولة والنقل.
نقطة انصهار الميثانول
CH3OH لديه نقطة انصهار تبلغ -97.6 درجة مئوية (-143.68 درجة فهرنهايت). وهذا يعني أن CH3OH سائل في درجة حرارة الغرفة ولكن يمكن تجميده بسهولة إلى شكل صلب عن طريق تبريده إلى ما دون نقطة الانصهار. تعتبر نقطة الانصهار المنخفضة لـ CH3OH مفيدة أيضًا في بعض التطبيقات المعملية، مثل تحضير المذيبات المبردة للتحليل الطيفي بالرنين المغناطيسي النووي.
كثافة الميثانول جم / مل
تبلغ كثافة CH3OH 0.792 جم / مل عند 20 درجة مئوية (68 درجة فهرنهايت). وهذا يعني أن CH3OH أقل كثافة من الماء ويمكن أن تطفو عليه. يمكن أيضًا استخدام كثافة CH3OH لحساب حجم CH3OH اللازم للحصول على كتلة معينة أو تركيز معين من المحلول.
الوزن الجزيئي للميثانول
الوزن الجزيئي لـ CH3OH هو 32.04 جم / مول. يتم حساب هذه القيمة عن طريق إضافة الأوزان الذرية لذرات الكربون والهيدروجين والأكسجين في جزيء واحد CH3OH. الوزن الجزيئي لـ CH3OH مفيد في تحديد خواصه الفيزيائية، مثل درجة الغليان، ونقطة الانصهار، والكثافة.
هيكل الميثانول
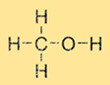
يحتوي الميثانول على بنية بسيطة تتكون من مجموعة الميثيل (CH3) ومجموعة الهيدروكسيل (-OH) المرتبطة بذرة كربون واحدة. الصيغة الجزيئية للميثانول هي CH3OH. الميثانول هو جزيء قطبي بسبب وجود مجموعة الهيدروكسيل، مما يجعله قابل للذوبان في المذيبات القطبية مثل الماء والإيثانول.
صيغة الميثانول
الصيغة الكيميائية للميثانول هي CH3OH. وهذا يعني أن كل جزيء ميثانول يحتوي على ذرة كربون واحدة وأربع ذرات هيدروجين وذرة أكسجين واحدة. يمكن استخدام صيغة الميثانول لتحديد الوزن الجزيئي والخواص الفيزيائية الأخرى للميثانول. تعتبر الصيغة الكيميائية للميثانول مفيدة أيضًا في كتابة المعادلات الكيميائية وموازنة التفاعلات الكيميائية التي تتضمن الميثانول.
| مظهر | سائل عديم اللون |
| جاذبية معينة | 0.792 جم/مل عند 20 درجة مئوية |
| لون | عديم اللون |
| يشم | حلو، حار |
| الكتلة المولية | 32.04 جم/مول |
| كثافة | 0.792 جم/مل عند 20 درجة مئوية |
| نقطة الانصهار | -97.6 درجة مئوية |
| نقطة الغليان | 64.7 درجة مئوية |
| نقطة فلاش | 11.1 درجة مئوية |
| الذوبان في الماء | قابلة للامتزاج |
| الذوبان | يمتزج مع الإيثانول والأثير والأسيتون والعديد من المذيبات العضوية |
| ضغط البخار | 13.02 كيلو باسكال عند 20 درجة مئوية |
| كثافة بخار | 1.11 (الهواء = 1) |
| pKa | 15.5 |
| الرقم الهيدروجيني | 7 (محايد) |
ملاحظة: القيم المدرجة في هذا الجدول تقريبية وقد تختلف حسب الظروف المحددة ومصادر الميثانول.
السلامة ومخاطر الميثانول
يشكل CH3OH العديد من مخاطر السلامة ويجب التعامل معه بحذر. وهو سائل قابل للاشتعال وقد يشتعل إذا تعرض للحرارة أو الشرر أو اللهب. يمكن لأبخرة CH3OH أيضًا أن تشكل مخاليط متفجرة مع الهواء. استنشاق أبخرة CH3OH يمكن أن يسبب الدوخة والصداع والغثيان ومشاكل صحية أخرى. CH3OH سام أيضًا ويمكن امتصاصه عن طريق الجلد أو تناوله، مما يسبب مضاعفات صحية خطيرة بما في ذلك العمى والغيبوبة والموت. من المهم ارتداء ملابس واقية والتعامل مع CH3OH في منطقة جيدة التهوية باستخدام معدات السلامة المناسبة، مثل النظارات الواقية والقفازات وجهاز التنفس الصناعي. يجب تنظيف الانسكابات على الفور والتخلص منها بشكل صحيح.
| رموز الخطر | الجمجمة والعظمتين المتقاطعتين، قابلة للاشتعال |
| وصف الأمان | يُحفظ بعيدًا عن الحرارة/الشرر/اللهب المكشوف/الأسطح الساخنة. استخدم معدات كهربائية/تهوية/إضاءة مقاومة للانفجار. الحفاظ على حاوية مغلقة بإحكام. حاوية أرضية/مكفولة ومعدات الاستقبال. استخدم فقط الأدوات التي لا تسبب شرارة. اتخاذ تدابير وقائية ضد التفريغ ثابت. تجنب استنشاق الأبخرة. يغسل جيدا بعد المناولة. لا تأكل أو تشرب أو تدخن أثناء استخدام هذا المنتج. |
| معرفات | UN1230 |
| رمز النظام المنسق | 29051100 |
| فئة الخطر | 3 |
| مجموعة التعبئة | ثانيا |
| تسمم | الميثانول مادة سامة ويمكن أن تسبب العمى والغيبوبة والموت إذا تم تناولها أو استنشاقها أو امتصاصها عن طريق الجلد. يمكن أن يسبب أيضًا تهيجًا واحمرارًا وحروقًا عند ملامسته. يمكن أن يسبب التعرض لأبخرة الميثانول الصداع والدوار والغثيان ومشاكل صحية أخرى. يجب التعامل مع الميثانول بحذر شديد وباستخدام معدات الحماية المناسبة. |
ملاحظة: القيم المدرجة في هذا الجدول تقريبية وقد تختلف حسب الظروف المحددة ومصادر الميثانول. من المهم الرجوع إلى صحيفة بيانات السلامة واللوائح المعمول بها عند التعامل مع الميثانول.
طرق تصنيع الميثانول
الأكسدة المباشرة للميثان، والأكسدة الجزئية للغاز الطبيعي، وتغويز الفحم، والتوليف من ثاني أكسيد الكربون والهيدروجين كلها توليف الميثانول.
إحدى الطرق الأكثر شيوعًا لتصنيع الميثانول هي التحويل التحفيزي للغاز الاصطناعي، وهو خليط من أول أكسيد الكربون وثاني أكسيد الكربون والهيدروجين. تتضمن هذه العملية استخدام محفز، عادةً ما يكون أساسه النحاس، لتسهيل التفاعل. ويتم إدخال الغاز الاصطناعي إلى مفاعل يحتوي على المحفز عند درجات حرارة وضغوط عالية، مما يؤدي إلى إنتاج الميثانول.
هناك طريقة أخرى لتصنيع الميثانول تتضمن أكسدة الميثان مباشرة، والتي تتضمن استخدام درجات حرارة وضغوط عالية في وجود محفز مثل البلاتين أو البلاديوم. تعتبر هذه الطريقة أكثر صعوبة وأكثر تكلفة من طريقة الغاز الاصطناعي، ولكنها أكثر كفاءة ويمكن أن تنتج عوائد أعلى.
الأكسدة الجزئية للغاز الطبيعي هي طريقة أخرى لتخليق الميثانول، والتي تنطوي على استخدام الأكسجين أو الهواء لأكسدة الغاز الطبيعي جزئيًا، وإنتاج خليط من أول أكسيد الكربون والهيدروجين. يتم بعد ذلك إدخال الخليط إلى مفاعل يحتوي على محفز، مما يؤدي إلى إنتاج الميثانول.
تغويز الفحم هو طريقة أخرى لتخليق الميثانول، والتي تتضمن تحويل الفحم إلى غاز اصطناعي، تليها نفس عملية التحويل الحفزي كما هو موضح أعلاه.
يؤدي احتجاز الكربون واستخدامه إلى تحويل انبعاثات ثاني أكسيد الكربون الناتجة عن العمليات الصناعية إلى ميثانول، وذلك باستخدام الهيدروجين كعامل اختزال.
استخدامات الميثانول
للميثانول مجموعة واسعة من الاستخدامات في مختلف الصناعات، بما في ذلك:
- الوقود: يمكن للمركبات والمولدات والمعدات الصناعية الأخرى استخدام الميثانول كوقود.
- المذيب: الميثانول مذيب ممتاز للعديد من المواد، بما في ذلك الراتنجات والأصباغ والزيوت. يستخدم المصنعون الميثانول لإنتاج الدهانات والورنيش والطلاءات الأخرى.
- الوسيط الكيميائي: يستخدم كمادة خام لإنتاج الفورمالديهايد وحمض الخليك والمواد الكيميائية الأخرى.
- مضاد التجمد: يستخدم كعامل مضاد للتجمد في أنظمة تبريد السيارات.
- عامل إزالة الجليد: يستخدم كعامل إزالة الجليد لأجنحة الطائرات ومدارج المطارات.
- المنظف: يستخدم كمنظف في العمليات الصناعية المختلفة.
- المستحضرات الصيدلانية: يستخدم كمذيب في إنتاج العديد من المنتجات الصيدلانية.
- الطاقة البديلة: تمت دراستها كوقود بديل لخلايا الوقود وكوسيلة محتملة لتخزين الطاقة.
- الميثانول إلى الأوليفينات (MTO): الأوليفينات مثل الإيثيلين والبروبيلين تأتي من تحويل الميثانول.
- الميثانول إلى البنزين (MTG): عملية تسمى MTG تحول الميثانول إلى بنزين.
أسئلة:
س: ما هو الميثانول؟
ج: الميثانول، المعروف أيضًا باسم كحول الخشب، هو سائل عديم اللون وقابل للاشتعال وله رائحة حلوة. وهو أبسط كحول وصيغته الكيميائية هي CH3OH.
س: هل الميثانول قطبي أم غير قطبي؟
ج: الميثانول جزيء قطبي. وله شحنة جزئية موجبة على ذرات الهيدروجين وشحنة جزئية سالبة على ذرة الأكسجين، مما يؤدي إلى عزم ثنائي القطب.
س: ما هو استخدام الميثانول؟
ج: للميثانول نطاق واسع من الاستخدامات في العديد من الصناعات، بما في ذلك استخدامه كوقود، ومذيب، ووسيط كيميائي، ومضاد للتجمد، وعامل إزالة الجليد، ومنظف، ومذيب دوائي، ووسائط تخزين الطاقة المحتملة. كما أنها تستخدم في إنتاج الفورمالديهايد وحمض الخليك والمواد الكيميائية الأخرى. بالإضافة إلى ذلك، يتم تحويل الميثانول إلى الأوليفينات مثل الإيثيلين والبروبيلين، والتي تستخدم كمواد خام لإنتاج البلاستيك.
