إيثيل فينيل إيثر (C4H8O) هو مركب عضوي متطاير يستخدم كمذيب وفي إنتاج البوليمرات. لها رائحة طيبة وقابلة للاشتعال.
| اسم الأيوباك | إيثوكسي إيثيلين |
| الصيغة الجزيئية | C4H8O |
| CAS رقم | 109-92-2 |
| المرادفات | فينيل إيثيل الأثير، إيثوكسي إيثيلين، EVE، EEE، VEVE |
| إنتشي | إنتشي = 1S/C4H8O/c1-2-5-4-3-6-1/h1-4H2 |
خصائص إيثيل فينيل الأثير
صيغة إيثيل فينيل الأثير
الصيغة الكيميائية للإيثوكسي إيثيلين هي C4H8O. ويصور تركيب هذا المركب، مشيراً إلى أنه يحتوي على أربع ذرات كربون، وثماني ذرات هيدروجين، وذرة أكسجين واحدة.
إيثيل فينيل الأثير الكتلة المولية
يتم حساب الكتلة المولية للإيثوكسي إيثيلين عن طريق إضافة الكتل الذرية للعناصر المكونة له. وفي هذه الحالة يبلغ حوالي 72.11 جرامًا لكل مول. يتم استخدام الكتلة المولية لتحديد كمية المادة الموجودة في عينة معينة.
درجة غليان إيثيل فينيل إيثر
تبلغ درجة غليان الإيثوكسي إيثيلين حوالي 35 إلى 36 درجة مئوية (95 إلى 97 درجة فهرنهايت). تشير نقطة الغليان المنخفضة نسبيًا إلى أنه يمكن أن يتبخر بسهولة ويتحول إلى الحالة الغازية عند تسخينه.
نقطة انصهار إيثيل فينيل إيثر
تبلغ نقطة انصهار الإيثوكسي إيثيلين حوالي -102 درجة مئوية (-152 درجة فهرنهايت). يشير هذا إلى أنه مركب متطاير يوجد في صورة سائلة في درجة حرارة الغرفة ويتحول إلى مادة صلبة عند درجات حرارة منخفضة جدًا.
كثافة إيثيل فينيل الأثير جم/مل
تبلغ كثافة الإيثوكسي إيثيلين حوالي 0.73 جرام لكل ملليلتر. هذه القيمة تعني كتلة المركب لكل وحدة حجم. كثافة المادة مهمة لمختلف التطبيقات، بما في ذلك تحديد الطفو والذوبان.
إيثيل فينيل الأثير الوزن الجزيئي
يبلغ الوزن الجزيئي للإيثوكسي إيثيلين حوالي 72.11 جرامًا لكل مول. وهو يمثل مجموع الأوزان الذرية لجميع الذرات الموجودة في الجزيء. الوزن الجزيئي أمر بالغ الأهمية في الحسابات الكيميائية المختلفة، مثل قياس العناصر الكيميائية وتحديد التركيزات.
هيكل إيثيل فينيل الأثير
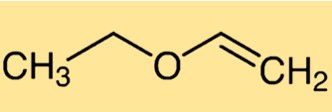
يتكون الإيثوكسي إيثيلين من سلسلة كربون بها أربع ذرات كربون (C4)، وذرة أكسجين (O)، ومجموعة إيثيل (-C2H5) متصلة بمجموعة الفينيل (-CH=CH2). يشبه الهيكل سلسلة كربون خطية مع ذرة أكسجين في المنتصف، متصلة بمجموعتين من الكربون.
ذوبان إيثيل فينيل الأثير
الإيثوكسي إيثيلين قابل للذوبان بشكل معتدل في الماء، مع قابلية ذوبان حوالي 6.2 جرام لكل 100 ملليلتر عند 25 درجة مئوية (77 درجة فهرنهايت). ومع ذلك، فإنه يظهر قابلية ذوبان أفضل في المذيبات العضوية مثل الإيثانول والأسيتون. تتأثر ذوبان الإيثوكسي إيثيلين بقطبيته وتفاعلاته الجزيئية مع جزيئات المذيب.
| مظهر | سائل عديم اللون |
| جاذبية معينة | 0.73 جم/مل |
| لون | عديم اللون |
| يشم | جَذّاب |
| الكتلة المولية | 72.11 جرام/مول |
| كثافة | 0.73 جم/مل |
| نقطة الانصهار | -102 درجة مئوية |
| نقطة الغليان | 35-36 درجة مئوية |
| نقطة فلاش | -20 درجة مئوية |
| الذوبان في الماء | معتدل |
| الذوبان | قابل للذوبان في المذيبات العضوية مثل الإيثانول والأسيتون |
| ضغط البخار | 159 ملم زئبق عند 25 درجة مئوية |
| كثافة بخار | 2.5 (الهواء = 1) |
| pKa | 12.7 |
| الرقم الهيدروجيني | حيادي |
السلامة ومخاطر إيثيل فينيل الأثير
يشكل الإيثوكسي إيثيلين بعض مخاطر السلامة ويجب التعامل معه بحذر. وهو شديد الاشتعال، حيث تصل نقطة وميضه إلى -20 درجة مئوية (-4 درجات فهرنهايت)، مما يعني أنه يمكن أن يشتعل بسهولة. وينبغي أن تبقى بعيدا عن اللهب المكشوف والشرر ومصادر الحرارة. قد يسبب المركب أيضًا تهيجًا للجلد والعينين والجهاز التنفسي من خلال التلامس أو الاستنشاق. التهوية الكافية ضرورية لتقليل التعرض. يجب تخزين الإيثوكسي إيثيلين في حاويات مغلقة بإحكام، بعيدًا عن المواد غير المتوافقة. من المهم اتباع إجراءات التعامل الصحيحة، وارتداء معدات الحماية المناسبة ومراجعة أوراق بيانات السلامة للحصول على معلومات السلامة الكاملة.
| رموز الخطر | قابل للاشتعال (و) |
| وصف الأمان | يُحفظ بعيدًا عن الحرارة/الشرر/اللهب المكشوف. استخدام في مناطق جيدة التهوية. تجنب ملامسة العينين والجلد، والملابس. |
| أرقام تعريف الأمم المتحدة | رقم الأمم المتحدة 1151 |
| رمز النظام المنسق | 29091900 |
| فئة الخطر | الفئة 3 – السوائل القابلة للاشتعال |
| مجموعة التعبئة | جنرال الكتريك الثاني |
| تسمم | قد يسبب تهيج الجلد والعينين والجهاز التنفسي. تجنب التعرض لفترات طويلة أو متكررة. |
طرق تصنيع إيثيل فينيل إيثر
يمكن لطرق مختلفة تصنيع الإيثوكسي إيثيلين. يتضمن النهج الشائع التفاعل بين الإيثانول والأسيتيلين في وجود محفز أساسي قوي، مثل هيدروكسيد البوتاسيوم (KOH). يستمر التفاعل من خلال عملية إزالة، حيث تتحد مجموعة الهيدروكسيل (-OH) من الإيثانول مع ذرة هيدروجين من جزيء الأسيتيلين ، لتكوين الماء. يتبع تكوين رابطة إيثر الفينيل بين جزيء الأسيتيلين ومجموعة -C2H5 المتبقية من الإيثانول هذه الخطوة.
تتضمن الطريقة الأخرى التفاعل بين الكحول الإيثيلي وأسيتات الفينيل في وجود محفز حمضي، مثل حمض الكبريتيك (H2SO4). يساهم المحفز الحمضي في عملية الأسترة، حيث يتحد الكحول والحمض لتكوين مركب إستر. في هذه الحالة، يخضع الإستر الناتج لتحلل حراري لاحق، مما يؤدي إلى تكوين إيثوكسي إيثيلين.
يمكن للتفاعل بين الكحول الإيثيلي والأسيتيلين في وجود محفز البلاديوم تحضير الإيثوكسي إيثيلين. تسمح هذه الطريقة، المعروفة باسم تفاعل الاقتران المحفز بالـ Pd، بالتحويل المباشر للكحول والأسيتيلين إلى إيثر الفينيل المطلوب.
تمهد طرق التوليف هذه الطريق لإنتاج الإيثوكسي إيثيلين، والذي يجد تطبيقات في صناعات مختلفة مثل تصنيع البوليمرات والمذيبات والوسائط الكيميائية. تعد المعالجة السليمة والالتزام ببروتوكولات السلامة أمرًا ضروريًا أثناء عملية التوليف بسبب القابلية للاشتعال والمخاطر المحتملة المرتبطة بالإيثوكسي إيثيلين.
استخدامات إيثيل فينيل إيثر
فيما يلي بعض الاستخدامات الشائعة للإيثوكسي إيثيلين نظرًا لخصائصه الفريدة:
- المذيب: يستخدم الإيثوكسي إيثيلين كمذيب للمركبات العضوية المختلفة، وخاصة في إنتاج الراتنجات والورنيشات والورنيش.
- البلمرة: يعمل كمونومر في تركيب البوليمرات المختلفة، مثل البولي (إيثر الفينيل) والبولي (إيثوكسي إيثيلين)، والتي تجد تطبيقات في المواد اللاصقة والطلاءات ومعدلات السطح.
- الوسطيات الكيميائية: تعمل كمقدمة لتخليق المركبات الأخرى. ويخضع لتفاعلات كيميائية مختلفة لإنتاج مواد وسيطة قيمة تستخدم في الصناعات الدوائية والكيماويات الزراعية والعطور.
- مادة مضافة للوقود: تستخدمها الصناعات كمادة مضافة في البنزين لتحسين كفاءة الاحتراق وتقليل الانبعاثات.
- الكاشف المختبري: يعمل ككاشف في التخليق العضوي، وخاصة في تحضير مركبات الفينيل والإيثرات والجزيئات العضوية الوظيفية الأخرى.
- النكهة والعطر: يلعب دوراً في إنتاج النكهات والعطور الاصطناعية، وإضفاء الروائح الطيبة والمرغوبة لمختلف المنتجات الاستهلاكية.
- البحوث الكيميائية: يتم تطبيقها كمركب مرجعي في تقنيات التحليل الكيميائي مثل التحليل اللوني للغاز والتحليل الطيفي.
- مذيب الاستخلاص: يعمل كمذيب لاستخلاص المنتجات الطبيعية، مثل الزيوت العطرية والمنكهات.
تسمح الطبيعة المتنوعة للإيثوكسي إيثيلين بالمساهمة في العديد من الصناعات، والوفاء بأدوار تتراوح من المذيبات والمونومرات إلى الكواشف والمواد المضافة.
أسئلة:
س: هل يمكن اقتران إيثيل فينيل إيثر؟
ج: لا، لا يُظهر الإيثوكسي إيثيلين اقترانًا بسبب عدم وجود روابط باي مترافقة في بنيته.
س: ما هو دور إيثيل فينيل إيثر في تفاعلات ROMP؟
ج: يعمل الإيثوكسي إيثيلين كمونومر في تفاعلات بلمرة استبدال فتح الحلقة (ROMP)، حيث يشارك في تكوين بوليمرات ذات خصائص وهياكل فريدة.
س: كحول إيثيل فينيل الأثير؟
ج: لا يحتوي الإيثوكسي إيثيلين على مجموعة وظيفية كحولية؛ وهو مركب الأثير.
س: طيف الأشعة تحت الحمراء من إيثيل فينيل الأثير؟
ج: يُظهر طيف الأشعة تحت الحمراء (IR) للإيثوكسي إيثيلين عمومًا قممًا مميزة تتراوح بين 3000 إلى 3100 سم^-1 (امتداد CH) ومن 1600 إلى 1650 سم^-1 (امتداد C=C).
س: كثافة إيثيل فينيل الأثير؟
ج: تبلغ كثافة الإيثوكسي إيثيلين حوالي 0.73 جرام لكل مليلتر (جم/مل).
س: هل يمكن اقتران إيثيل فينيل إيثر؟
ج: لا، لا يُظهر الإيثوكسي إيثيلين اقترانًا نظرًا لبنيته الجزيئية التي تفتقر إلى روابط باي المترافقة.
س: استقرار إيثيل فينيل الأثير؟
ج: يعتبر الإيثوكسي إيثيلين مستقرًا نسبيًا ولكن يجب التعامل معه وتخزينه بحذر نظرًا لقابليته للاشتعال والمخاطر المحتملة.
س: مصنعي إيثيل فينيل الأثير؟
ج: يتم إنتاج الإيثوكسي إيثيلين من قبل العديد من مصنعي وموردي المواد الكيميائية حول العالم، بما في ذلك شركات المواد الكيميائية والكواشف الدقيقة.
