الأنيلين (C6H5NH2) هو أمين عطري يستخدم في إنتاج الأصباغ والأدوية والمواد الكيميائية المطاطية. لها رائحة مميزة وهي مقدمة للمركبات العضوية المختلفة.
| اسم الأيوباك | الأنيلين |
| الصيغة الجزيئية | C6H7N |
| CAS رقم | 62-53-3 |
| المرادفات | أمينوبنزين، بنزينامين |
| إنتشي | إنشي=1S/C6H7N/c7-6-4-2-1-3-5-6/h1-5H,7H2 |
خصائص الأنيلين
صيغة الأنيلين
صيغة الأنيلين هي C6H7N. ويتكون من ست ذرات كربون وسبع ذرات هيدروجين وذرة نيتروجين واحدة. ترتيب هذه الذرات يعطي الأنيلين خواصه الكيميائية الفريدة.
كتلة الأنيلين المولية
يتم حساب الكتلة المولية لـ C6H5NH2 عن طريق إضافة الكتل الذرية لجميع العناصر المكونة له. تبلغ الكتلة المولية لـ C6H5NH2 حوالي 93.13 جرامًا لكل مول (جم / مول). هذه القيمة مفيدة في الحسابات والتفاعلات الكيميائية المختلفة التي تتضمن C6H5NH2.
نقطة غليان الأنيلين
تبلغ درجة غليان C6H5NH2 حوالي 184 درجة مئوية (184 درجة مئوية). عند درجة الحرارة هذه، يخضع C6H5NH2 لتغير الطور من السائل إلى الغاز. تعتبر نقطة الغليان خاصية مهمة تحدد الظروف التي يمكن بموجبها تبخير C6H5NH2.
نقطة انصهار الأنيلين
تبلغ نقطة انصهار C6H5NH2 حوالي -6 درجة مئوية (-6 درجة مئوية). هذه هي درجة الحرارة التي يتحول عندها C6H5NH2 الصلب إلى الحالة السائلة. تعتبر نقطة الانصهار مهمة في تحديد الحالة الفيزيائية لـ C6H5NH2 في ظل ظروف درجات الحرارة المختلفة.
كثافة الأنيلين جم / مل
تبلغ كثافة C6H5NH2 حوالي 1.02 جرام لكل ملليلتر (جم / مل). تمثل الكثافة كتلة المادة لكل وحدة حجم. توفر قيمة كثافة C6H5NH2 معلومات حول ضغطها أو تركيزها في حجم معين من الفضاء.
الوزن الجزيئي للأنيلين
يبلغ الوزن الجزيئي لـ C6H5NH2 حوالي 93.13 جرامًا لكل مول (جم / مول). وهو مجموع الأوزان الذرية لجميع الذرات الموجودة في الصيغة الكيميائية C6H5NH2. يلعب الوزن الجزيئي دورًا حاسمًا في الحسابات المتكافئة وفي تحديد كمية C6H5NH2 اللازمة للتفاعلات.
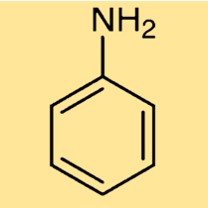
هيكل الأنيلين
يحتوي C6H5NH2 على بنية تتكون من حلقة بنزين (حلقة سداسية من ذرات الكربون) مع مجموعة أمينية متصلة (-NH2) بدلاً من ذرة الهيدروجين. يعطي هذا الهيكل C6H5NH2 خصائصه العطرية والأساسية، مما يجعله مفيدًا في التطبيقات الصناعية المختلفة.
ذوبان الأنيلين
C6H5NH2 قليل الذوبان في الماء ولكنه يذوب بسهولة في المذيبات العضوية مثل الإيثانول والأثير والكلوروفورم. تتأثر قابلية ذوبانه بالقطبية والقوى الجزيئية بين C6H5NH2 والمذيب. تسمح هذه الخاصية بدمج C6H5NH2 بسهولة في العمليات والتركيبات الكيميائية المختلفة.
| مظهر | عديم اللون إلى سائل أصفر شاحب |
| جاذبية معينة | 1.02 جرام/مل |
| لون | عديم اللون إلى أصفر شاحب |
| يشم | رائحة مميزة |
| الكتلة المولية | 93.13 جرام/مول |
| كثافة | 1.02 جرام/مل |
| نقطة الانصهار | -6 درجة مئوية |
| نقطة الغليان | 184 درجة مئوية |
| نقطة فلاش | 70 درجة مئوية |
| الذوبان في الماء | ضعيف الذوبان |
| الذوبان | قابل للذوبان في المذيبات العضوية |
| ضغط البخار | 5.60 ملم زئبق |
| كثافة بخار | 3.24 (الهواء=1) |
| pKa | 4.61 |
| الرقم الهيدروجيني | محايدة تقريبًا |
سلامة ومخاطر الأنيلين
يشكل C6H5NH2 مخاطر محتملة على السلامة ويجب التعامل معه بحذر. وهو ضار إذا تم ابتلاعه أو استنشاقه أو امتصاصه عن طريق الجلد. الاتصال المباشر مع C6H5NH2 قد يسبب تهيج العينين والجلد والجهاز التنفسي. قد يؤدي التعرض لفترات طويلة أو متكررة إلى آثار أكثر خطورة، بما في ذلك التهاب الجلد واضطرابات الدم. كما أن C6H5NH2 قابل للاشتعال ويمكن أن تشكل أبخرته مخاليط متفجرة في الهواء. يجب استخدام التهوية الكافية ومعدات الحماية الشخصية عند العمل مع C6H5NH2. تعتبر ممارسات التخزين والتعامل والتخلص المناسبة ضرورية لتقليل المخاطر وضمان سلامة الأشخاص والبيئة.
| رموز الخطر | تي، ن |
| وصف الأمان | تجنب ملامسة الجلد والعينين. استخدام في منطقة جيدة التهوية. التعامل مع القفازات والملابس الواقية. |
| أرقام تعريف الأمم المتحدة | الأمم المتحدة 1547 |
| رمز النظام المنسق | 2921.43.0000 |
| فئة الخطر | 6.1 (المواد السامة) |
| مجموعة التعبئة | ثالثا |
| تسمم | سام إذا تم ابتلاعه أو استنشاقه أو امتصاصه عن طريق الجلد. قد يسبب تهيج والتهاب الجلد واضطرابات في الدم. |
طرق تركيب الأنيلين
يمكن لطرق مختلفة تصنيع C6H5NH2.
الطريقة الشائعة هي تقليل النيتروبنزين . في هذه العملية، يتفاعل عامل اختزال، مثل برادة الحديد أو القصدير، مع النيتروبنزين في وجود حمض قوي، مثل حمض الهيدروكلوريك. وينتج عن هذا التفاعل تحويل مجموعة النيترو (-NO2) إلى مجموعة أمينية (-NH2)، مما ينتج عنه C6H5NH2.
تتضمن الطريقة الأخرى اختزال النيتروبنزين باستخدام غاز الهيدروجين فوق محفز، مثل البلاديوم أو البلاتين. تستخدم الطريقة الصناعية لإنتاج C6H5NH2 على نطاق واسع عملية تسمى الهدرجة الحفزية.
للحصول على C6H5NH2، يمكن استخدام كبريتيد الصوديوم أو ثنائي كبريتيت الصوديوم في اختزال النيتروبنزين . تعمل عوامل الاختزال هذه على تسهيل تحويل مجموعة النيترو إلى المجموعة الأمينية.
لتصنيع C6H5NH2، يمكن معالجة كلوروبنزين بالأمونيا في وجود قاعدة قوية، مثل هيدروكسيد الصوديوم. هذه العملية، المعروفة باسم تفاعل ساندماير، تؤدي إلى استبدال الكلور بمجموعة أمينية، مما ينتج عنه C6H5NH2.
بالإضافة إلى ذلك، يمكن تحضير C6H5NH2 عن طريق تقليل الآزوبنزين أو الآزوكسيبنزين، والذي يتضمن كسر رابطة النيتروجين والنيتروجين لتشكيل مجموعة أمينية.
توفر طرق التوليف هذه طرقًا مختلفة للحصول على C6H5NH2، مما يسمح بإنتاجه على المستوى المختبري والصناعي. يعتمد اختيار الطريقة على عوامل مثل توفر المواد الخام، وظروف التفاعل، والنقاء المطلوب للمنتج النهائي.
استخدامات الأنيلين
يجد C6H5NH2 تطبيقات في مختلف الصناعات نظرًا لخصائصه المتنوعة. فيما يلي بعض استخداماته الشائعة:
- إنتاج الأصباغ: يعتبر C6H5NH2 بمثابة مادة خام رئيسية لتصنيع العديد من الأصباغ، بما في ذلك الأصباغ الاصطناعية والأصباغ المستخدمة في صناعات النسيج والجلود والورق.
- صناعة الأدوية: تعتبر مشتقات C6H5NH2 حاسمة في تصنيع الأدوية الصيدلانية، مثل المسكنات وخافضات الحرارة والعوامل المضادة للملاريا.
- المواد الكيميائية المطاطية: يعمل C6H5NH2 بشكل فعال على تحسين أداء ومتانة المنتجات المطاطية من خلال كونه عنصرًا حاسمًا في إنتاج المسرعات ومضادات الأكسدة داخل صناعة المطاط.
- مبيدات الأعشاب والمبيدات الحشرية: يستخدم المزارعون بشكل فعال مشتقات C6H5NH2 في تركيب مبيدات الأعشاب والمبيدات الحشرية، وبالتالي السيطرة بشكل فعال على الأعشاب الضارة والآفات في الزراعة.
- إنتاج البولي يوريثان: يعتبر C6H5NH2 مكونًا أساسيًا في تصنيع رغاوي البولي يوريثان والطلاءات والمواد اللاصقة، المستخدمة على نطاق واسع في صناعات البناء والسيارات.
- الوسطيات الكيميائية: C6H5NH2 بمثابة لبنة بناء متعددة الاستخدامات لتخليق المركبات العضوية المختلفة، مثل المواد الكيميائية المطاطية، والمستحضرات الصيدلانية، والكيماويات الزراعية.
- مذيب لمختلف المواد: يعمل C6H5NH2 على إذابة المواد المختلفة بما في ذلك الدهون والزيوت والشموع والراتنجات.
- الكاشف المعملي: في التجارب المعملية للتخليق العضوي، يستخدم الباحثون C6H5NH2 ككاشف ويستخدمونه كمحفز في بعض التفاعلات.
- المواد الكيميائية الفوتوغرافية: تساهم مشتقات C6H5NH2 بشكل فعال في إنتاج المواد الكيميائية الفوتوغرافية، مثل المطورين والأصباغ.
- بادئ البلمرة: يعمل C6H5NH2 كبادئ في بعض تفاعلات البلمرة، مما يسمح بتكوين بوليمرات ذات خصائص محددة.
تسلط هذه التطبيقات المتنوعة الضوء على أهمية C6H5NH2 في الصناعات التي تتراوح من المنسوجات والأدوية إلى الزراعة والتصنيع.
أسئلة:
س: ما هو المركب الأكثر قاعدية من الأنيلين؟
ج: الأمونيا (NH3) أكثر أساسية من C6H5NH2.
س: ما هي غرزة الأنيلين؟
ج: النقطة C6H5NH2 هي أدنى درجة حرارة تكون عندها أحجام متساوية من C6H5NH2 ومذيب محدد قابلة للامتزاج تمامًا.
س: ما هو الأنيلين؟
ج: الأنيلين هو أمين عطري له الصيغة الكيميائية C6H7N، ويستخدم عادة في الأصباغ والمستحضرات الصيدلانية والمواد الكيميائية المطاطية.
س: كيفية فصل النفثالين والأنيلين؟
ج: يمكن فصل النفثالين عن C6H5NH2 بعملية تسمى التقطير التجزيئي، وذلك باستخدام الفرق في نقاط غليانهما.
س: كيف يتم تحضير الفينول من الأنيلين؟
ج: يمكن تصنيع الفينول من C6H5NH2 من خلال عملية تسمى الديازوتة، يليها التحلل المائي لتكوين الفينول.
س: كيفية تنظيف جلد الأنيلين؟
ج: لتنظيف جلد C6H5NH2، استخدم قطعة قماش ناعمة ورطبة لإزالة البقع بلطف وتجنب استخدام المواد الكيميائية القاسية أو الرطوبة الزائدة.
س: ما القاعدة المرافقة لحمض البنزويك والحمض المرافق للأنيلين؟
ج: القاعدة المرافقة لحمض البنزويك هي أيون البنزوات (C6H5COO-) والحمض المرافق لـ C6H5NH2 هو أيون الأنيلينيوم (C6H5NH3+).
س: ما هو جلد الأنيلين؟
ج: جلد C6H5NH2 هو نوع من الجلد المصبوغ بأصباغ C6H5NH2، مما يحافظ على الملمس والمظهر الطبيعي للجلد مع الحفاظ على ملمس ناعم وفاخر.
