كبريتيت المغنيسيوم (MgSO3) هو مركب يتكون من أيونات المغنيسيوم والكبريتيت. ويستخدم عادة كمادة حافظة للأغذية ومضادات الأكسدة في صناعة المواد الغذائية.
| اسم الأيوباك | كبريتيت المغنيسيوم |
| الصيغة الجزيئية | ملغسو3 |
| CAS رقم | 7757-88-2 |
| المرادفات | سلفونات المغنيسيوم، ثالث أكسيد الكبريت المغنيسيوم، E-536 |
| إنتشي | InChI=1S/Mg.H2O3S/c;1-4(2)3/h;(H2,1,2,3)/q+2;/p-2 |
خصائص كبريتيت المغنيسيوم
صيغة كبريتيت المغنيسيوم
يحتوي كبريتيت المغنيسيوم على الصيغة الكيميائية MgSO3، مما يدل على أنه يتكون من ذرة مغنيسيوم واحدة، وذرة كبريت واحدة، وثلاث ذرات أكسجين. أيون الكبريتيت هو أيون متعدد الذرات صيغته SO3 2-، ويتكون من ذرة كبريت مركزية مرتبطة بثلاث ذرات أكسجين. يحتوي أيون Mg على شحنة +2، بينما يحمل أيون SO3 2- شحنة -2، مما يجعل المركب متعادلًا كهربائيًا.
كبريتيت المغنيسيوم الكتلة المولية
الكتلة المولية لـ MgSO3 هي 104.37 جم/مول، وهو ما يتوافق مع مجموع الكتل الذرية لذرة مغنيسيوم واحدة وذرة كبريت واحدة وثلاث ذرات أكسجين. هذه القيمة مهمة لحساب كمية MgSO3 المطلوبة لتفاعل معين، وكذلك تحديد قياس العناصر الكيميائية للمعادلات الكيميائية.
درجة غليان كبريتيت المغنيسيوم
يتحلل MgSO3 قبل أن يصل إلى درجة غليانه، لذلك ليس له نقطة غليان محددة. وبدلاً من ذلك، يبدأ بالتحلل إلى أكسيد المغنيسيوم وثاني أكسيد الكبريت عند درجات حرارة أعلى من 700 درجة مئوية. يمكن تسريع عملية التحلل هذه عن طريق التعرض للهواء أو الرطوبة، مما يجعل MgSO3 مركبًا غير مستقر نسبيًا.
نقطة انصهار كبريتيت المغنيسيوم
تبلغ نقطة انصهار MgSO3 حوالي 150 درجة مئوية. عند درجة الحرارة هذه، يبدأ المركب بالتحلل إلى أكسيد المغنيسيوم وثاني أكسيد الكبريت. عملية التحلل طاردة للحرارة، مما يعني أنها تطلق الحرارة. تعتبر نقطة انصهار MgSO3 مهمة لفهم خصائصه كمادة صلبة، مثل قابليته للذوبان وبنيته البلورية.
كثافة كبريتيت المغنيسيوم جم/مل
تختلف كثافة MgSO3 تبعًا لشكله المادي، ولكنها تتراوح عمومًا من 2.5 إلى 3.0 جم/مل. هذه القيمة مهمة لتحديد كتلة حجم معين من MgSO3، وكذلك لفهم سلوكه في المحلول. يمكن أيضًا استخدام كثافة MgSO3 لحساب كثافته، وهو مقياس لكثافته النسبية مقارنة بالماء.
الوزن الجزيئي لكبريتات المغنيسيوم
الوزن الجزيئي لـ MgSO3 هو 104.37 جم/مول. هذه القيمة مهمة لفهم الخواص الفيزيائية والكيميائية للمركب، وكذلك لحساب كمية MgSO3 المطلوبة لتفاعل معين. يمكن حساب الوزن الجزيئي لـ MgSO3 عن طريق إضافة الأوزان الذرية لذرة مغنيسيوم واحدة، وذرة كبريت واحدة، وثلاث ذرات أكسجين.
هيكل كبريتيت المغنيسيوم
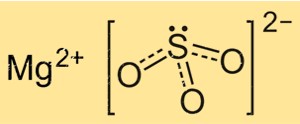
يعتمد هيكل MgSO3 على شبكة بلورية مكونة من أيونات Mg+2 وSO32- أيونات. أيونات Mg+2 محاطة بست ذرات أكسجين، مرتبة بشكل ثماني السطوح، بينما ترتبط أيونات SO32- بأيونات المغنيسيوم عبر ذرتي أكسجين. يعد التركيب البلوري لـ MgSO3 مهمًا لفهم خصائصه الفيزيائية والكيميائية، مثل قابليته للذوبان والتفاعل.
ذوبان كبريتيت المغنيسيوم
MgSO3 قليل الذوبان في الماء، مع قابلية ذوبان تبلغ حوالي 7.5 جم / لتر في درجة حرارة الغرفة. ويرجع هذا الذوبان المنخفض إلى التركيب البلوري للمركب، مما يجعل من الصعب على جزيئات الماء اختراق المادة الصلبة والذوبان فيها. يكون MgSO3 أكثر قابلية للذوبان في المحاليل الحمضية لأن الحمض يمكن أن يتفاعل مع أيون الكبريتيت لتكوين ثنائي كبريتيت وحمض الكبريت. تعد قابلية ذوبان MgSO3 مهمة لفهم سلوكه في المحلول، بالإضافة إلى تحديد فعاليته كمادة حافظة للأغذية ومضاد للأكسدة.
| مظهر | مسحوق أبيض أو بلورات |
| جاذبية معينة | 2.5 – 3.0 |
| لون | أبيض |
| يشم | عديم الرائحة |
| الكتلة المولية | 104.37 جم/مول |
| كثافة | 2.5 إلى 3.0 جم/مل |
| نقطة الانصهار | حوالي 150 درجة مئوية |
| نقطة الغليان | يتحلل فوق 700 درجة مئوية |
| نقطة فلاش | غير قابل للتطبيق |
| الذوبان في الماء | قابل للذوبان قليلا، حوالي 7.5 جم / لتر في درجة حرارة الغرفة |
| الذوبان | أكثر قابلية للذوبان في المحاليل الحمضية |
| ضغط البخار | غير قابل للتطبيق |
| كثافة بخار | غير قابل للتطبيق |
| pKa | غير قابل للتطبيق |
| الرقم الهيدروجيني | غير قابل للتطبيق |
السلامة ومخاطر كبريتيت المغنيسيوم
لا يعتبر MgSO3 مادة خطرة للغاية. ومع ذلك، فإنه قد يسبب تهيج العينين والجلد والجهاز التنفسي عن طريق الاتصال أو الاستنشاق. قد يؤدي تناول MgSO3 إلى تهيج الجهاز الهضمي وربما القيء. قد يؤدي التعرض لفترات طويلة لتركيزات عالية إلى تلف الرئة أو تهيج الجهاز التنفسي. ولذلك فمن المهم التعامل مع MgSO3 بعناية، وارتداء معدات الحماية الشخصية المناسبة وتجنب استنشاق الغبار أو الأبخرة. يجب تخزين MgSO3 في منطقة باردة وجافة وجيدة التهوية بعيدًا عن المواد غير المتوافقة مثل المؤكسدات القوية والأحماض والقواعد.
| رموز الخطر | لا أحد |
| وصف الأمان | تجنب استنشاق الغبار أو الأبخرة. ارتداء معدات الحماية الشخصية المناسبة. |
| أرقام تعريف الأمم المتحدة | غير منتظم |
| رمز النظام المنسق | 2833.29 |
| فئة الخطر | لا تصنف على أنها خطيرة |
| مجموعة التعبئة | غير قابل للتطبيق |
| تسمم | سمية منخفضة، قد تسبب تهيج العينين والجلد والجهاز التنفسي عن طريق الاتصال أو الاستنشاق. قد يسبب ابتلاع الدواء تهيج الجهاز الهضمي وربما القيء. قد يؤدي التعرض لفترات طويلة لتركيزات عالية إلى تلف الرئة أو تهيج الجهاز التنفسي. |
طرق تصنيع كبريتيت المغنيسيوم
يمكن تصنيع MgSO3 بطرق مختلفة، مثل تفاعل حمض الكبريتيك أو غاز ثاني أكسيد الكبريت مع أكسيد المغنيسيوم أو هيدروكسيد المغنيسيوم.
في إحدى الطرق، يؤدي تفاعل أكسيد المغنيسيوم مع الماء إلى تكوين هيدروكسيد المغنيسيوم ، والذي يتفاعل بعد ذلك مع حمض الكبريتوز لإنتاج MgSO3.
تتضمن الطريقة الأخرى تفاعل هيدروكسيد المغنيسيوم مع غاز ثاني أكسيد الكبريت في وجود الماء لتكوين MgSO3.
وفي طريقة أخرى، يمكن لتفاعل كبريتات المغنيسيوم مع كبريتيت الصوديوم أو كبريتيت البوتاسيوم تصنيع MgSO3. وينتج عن هذا التفاعل راسب من MgSO3، والذي يمكن للباحثين عزله عن طريق الترشيح والتجفيف.
من تفاعل خلات المغنسيوم مع غاز ثاني أكسيد الكبريت في وجود الماء يمكن تحضير MgSO3. ثم اغسل وجفف راسب MgSO3 الناتج.
يمكن استخدام هذه الطرق لإنتاج MgSO3 لمجموعة متنوعة من التطبيقات، بما في ذلك إنتاج الورق واللب، وتجهيز الأغذية والمشروبات، ومعالجة المياه.
استخدامات كبريتيت المغنيسيوم
MgSO3 له استخدامات مختلفة في صناعات مختلفة. فيما يلي بعض استخداماته الشائعة:
- معالجة المياه: يستخدم كمنظف للأكسجين في معالجة مياه الغلايات لمنع التآكل وتكوين القشور.
- معالجة الأغذية والمشروبات: يستخدم كمادة حافظة ومضاد للأكسدة في معالجة الأغذية والمشروبات لإطالة مدة الصلاحية ومنع التلف.
- إنتاج اللب والورق: يستخدم كعامل تبييض في صناعة اللب والورق لتحسين سطوع ولون المنتجات الورقية.
- صناعة المنسوجات: يستخدم كعامل اختزال في صناعة المنسوجات لإزالة الأكسجين الزائد وتحسين جودة المنتج النهائي.
- الزراعة: يستخدم رشاً ورقياً لتحسين نمو النباتات وزيادة إنتاجية المحاصيل.
- الطب: يستخدم في الطب التقليدي لخصائصه المضادة للأكسدة والمضادة للالتهابات.
- مستحضرات التجميل: يستخدم في مستحضرات التجميل كمستحلب ومثبت ومنظم للأس الهيدروجيني.
- استخدامات أخرى: يستخدم أيضًا في إنتاج المواد اللاصقة والدهانات والطلاءات وكذلك عمليات معالجة مياه الصرف الصحي.
أسئلة:
س: ما هي صيغة كبريتيت المغنيسيوم؟
ج: صيغة كبريتيت المغنيسيوم هي MgSO3.
س: ما هي كمية كبريتيت المغنيسيوم الموجودة في عينة حجمها 2.4 مول؟
ج: في عينة مكونة من 2.4 مول من MgSO3، يوجد 2.4 مول من MgSO3.
س: ما هي النسبة المئوية الكتلية لكل عنصر في 1 مول من كبريتيت المغنيسيوم؟
ج: في مول واحد من كبريتات المغنسيوم تكون نسبة كتلة الماغنيسيوم 32.44%، والكبريت 29.44%، والأكسجين 38.12%.
س: هل يوقف كبريتيت المغنيسيوم تشنجات العضلات؟
ج: لا يوجد دليل علمي يشير إلى أن MgSO3 يمكنه إيقاف تقلصات العضلات. ومع ذلك، تم استخدام كبريتات المغنيسيوم (ملح إبسوم) لهذا الغرض.
س: ما تأثير إضافة كبريتات المغنيسيوم إلى التفاعلات؟
ج: يمكن أن تعمل إضافة MgSO3 كعامل اختزال في بعض التفاعلات عن طريق إزالة الأكسجين. يمكن أن يعمل أيضًا كمادة حافظة ومضاد للأكسدة في بعض التطبيقات.
س: هل كبريتيت المغنيسيوم أيوني أم جزيئي؟
ج: MgSO3 مركب أيوني.
