سيليكات الكالسيوم (Ca2SiO4) هو مركب معدني يستخدم في مواد البناء والعزل ومقاومة الحرائق. يتم تصنيعه عن طريق الجمع بين أكسيد الكالسيوم والسيليكا. توفر سيليكات الكالسيوم عزلًا حراريًا ومقاومة للحريق.
| اسم الأيوباك | سيليكات الكالسيوم |
| الصيغة الجزيئية | Ca2SiO4 |
| CAS رقم | 1344-95-2 |
| المرادفات | حمض السيليك، ملح الكالسيوم (2:1)؛ ميتاسيليكات الكالسيوم؛ الكالسيوم وأكسيد السيليكون. أورثوسيليكات الكالسيوم |
| إنتشي | إنتشي = 1S/Ca.2O.Si/q+2;2*-1; |
خصائص سيليكات الكالسيوم
سيليكات الكالسيوم الكتلة المولية
يحتوي Ca2SiO4 على كتلة مولية تبلغ 172.237 جم/مول. يتم حساب هذه القيمة عن طريق إضافة الكتل الذرية للكالسيوم والسيليكون والأكسجين، وهي 40.078 جم/مول، 28.085 جم/مول و15.999 جم/مول على التوالي. الكتلة المولية مهمة في تحديد كمية Ca2SiO4 اللازمة للتفاعلات الكيميائية أو تحضير المحاليل.
نقطة غليان سيليكات الكالسيوم
ليس لدى Ca2SiO4 نقطة غليان محددة لأنه يتحلل قبل أن يصل إلى نقطة الغليان. عندما يتم تسخين Ca2SiO4، فإنه يخضع لسلسلة من التفاعلات الكيميائية التي تؤدي إلى إطلاق الماء وتكوين أكسيد الكالسيوم والسيليكا. تعتمد درجة حرارة تحلل Ca2SiO4 على النوع المحدد وتكوين المركب.
نقطة انصهار سيليكات الكالسيوم
درجة انصهار Ca2SiO4 هي 2130 درجة مئوية. عند درجة الحرارة هذه، يتغير Ca2SiO4 من الحالة الصلبة إلى الحالة السائلة. نقطة انصهار Ca2SiO4 عالية نسبيًا، مما يجعلها مناسبة لتطبيقات درجات الحرارة العالية مثل المواد المقاومة للحرارة والعزل ومقاومة الحرائق.
كثافة سيليكات الكالسيوم جم/مل
تختلف كثافة Ca2SiO4 تبعًا لنوع المركب وتكوينه. تتراوح كثافة Ca2SiO4 من 2.2 إلى 2.8 جم / مل. الكثافة العالية لـ Ca2SiO4 تجعلها مفيدة للتطبيقات التي يمثل فيها الوزن مشكلة. على سبيل المثال، يتم استخدامه كركام خفيف الوزن في الخرسانة.
الوزن الجزيئي لسليكات الكالسيوم
الوزن الجزيئي لـ Ca2SiO4 هو 172.237 جم/مول. يتم تحديد هذه القيمة بإضافة الأوزان الذرية للكالسيوم والسيليكون والأكسجين إلى المركب. يتم استخدام الوزن الجزيئي لـ Ca2SiO4 في حسابات مختلفة، مثل تحديد تركيز المحاليل أو كمية المركب اللازمة للتفاعلات الكيميائية.
هيكل سيليكات الكالسيوم
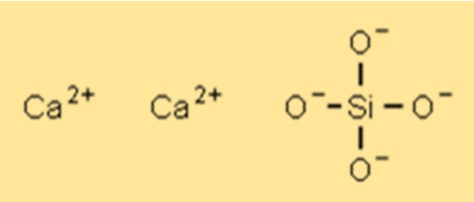
يحتوي Ca2SiO4 على بنية بلورية يمكن أن تختلف اعتمادًا على نوع المركب وتكوينه. التركيب البلوري الأكثر شيوعًا هو النظام البلوري أحادي الميل. يمنح التركيب البلوري لـ Ca2SiO4 خصائص معينة مثل القوة العالية والثبات الحراري والمقاومة الكيميائية.
صيغة سيليكات الكالسيوم
الصيغة الكيميائية لسليكات الكالسيوم هي Ca2SiO4. تمثل هذه الصيغة نسبة الكالسيوم والسيليكون والأكسجين في المركب. تعتبر صيغة سيليكات الكالسيوم مهمة في تحديد خصائصها واستخدامها في التطبيقات المختلفة مثل الأسمنت والعزل ومقاومة الحرائق.
| مظهر | بودرة بيضاء |
| جاذبية معينة | 2.2 – 2.8 جم/سم3 |
| لون | أبيض |
| يشم | عديم الرائحة |
| الكتلة المولية | 172,237 جم/مول |
| كثافة | 2.2 – 2.8 جم/سم3 |
| نقطة الانصهار | 2130 درجة مئوية |
| نقطة الغليان | ينهار قبل الغليان |
| نقطة فلاش | غير قابل للتطبيق |
| الذوبان في الماء | لا يتحلل في الماء |
| الذوبان | غير قابلة للذوبان في الماء، قابل للذوبان في الأحماض |
| ضغط البخار | غير قابل للتطبيق |
| كثافة بخار | غير قابل للتطبيق |
| pKa | غير قابل للتطبيق |
| الرقم الهيدروجيني | 7.0 – 9.0 |
سلامة ومخاطر سيليكات الكالسيوم
يعتبر Ca2SiO4 بشكل عام آمنًا للاستخدام في مجموعة متنوعة من التطبيقات، بما في ذلك مواد البناء والعزل والمضافات الغذائية. ومع ذلك، فإن استنشاق غبار Ca2SiO4 لفترة طويلة أو بشكل مفرط قد يؤدي إلى تهيج الجهاز التنفسي. قد يؤدي أيضًا ملامسة الجلد والعين لـ Ca2SiO4 إلى حدوث تهيج. على الرغم من أن Ca2SiO4 لا يعتبر مادة خطرة، فمن المهم التعامل معها بحذر واتباع احتياطات السلامة عند العمل مع هذه المادة. يجب ارتداء معدات الحماية الشخصية مثل القفازات ونظارات السلامة وحماية الجهاز التنفسي عند التعامل مع Ca2SiO4 لتقليل المخاطر الصحية المحتملة.
| رموز الخطر | غير قابل للتطبيق |
| وصف الأمان | ليست مادة خطيرة |
| أرقام تعريف الأمم المتحدة | غير قابل للتطبيق |
| رمز النظام المنسق | 6810.19 |
| فئة الخطر | غير قابل للتطبيق |
| مجموعة التعبئة | غير قابل للتطبيق |
| تسمم | سمية منخفضة. قد يسبب تهيج الجهاز التنفسي والجلد في حالة التعرض لفترة طويلة أو مفرطة |
طرق تصنيع سيليكات الكالسيوم
يمكن لطرق مختلفة تصنيع Ca2SiO4.
في إحدى الطرق، يتفاعل أكسيد الكالسيوم (CaO) مع السيليكا (SiO2) لإنتاج خليط من سيليكات الكالسيوم. يسمح الفرن ذو درجة الحرارة العالية بتخليق Ca2SiO4. يشتمل الخليط على Ca2SiO4 وCa3SiO5. مزيد من المعالجة وطحن الخليط ينتج درجات مختلفة من مسحوق Ca2SiO4.
تتضمن الطريقة الأخرى التفاعل بين هيدروكسيد الكالسيوم (Ca(OH)2) والسيليكا في الأوتوكلاف عند ضغط ودرجة حرارة مرتفعين. تنتج هذه العملية شكلًا نقيًا من Ca2SiO4، يُعرف باسم ولاستونيت (CaSiO3)، والذي له نطاق واسع من التطبيقات، بما في ذلك استخدامه كحشو في المواد البلاستيكية والطلاءات.
تشمل الطرق الأخرى لتصنيع Ca2SiO4 التفاعل بين كلوريد الكالسيوم (CaCl2) وسيليكات الصوديوم (Na2SiO3) لإنتاج هيدرات Ca2SiO4 (CSH)، وهو الرابط الرئيسي في الأسمنت البورتلاندي.
تسمح الكواشف والطرق المختلفة بتخليق Ca2SiO4 عن طريق ترسيبه من محلول أيونات الكالسيوم والسيليكات.
استخدامات سيليكات الكالسيوم
يحتوي Ca2SiO4 على مجموعة واسعة من التطبيقات بسبب خصائصه الفريدة، مثل مقاومة درجات الحرارة العالية، والتوصيل الحراري المنخفض والمقاومة الممتازة للحريق. فيما يلي بعض الاستخدامات الشائعة لـ Ca2SiO4:
- العزل: يستخدم كمادة عازلة في تطبيقات درجات الحرارة المرتفعة مثل بطانات الأفران وعزل الغلايات وخطوط البخار. إن موصليتها الحرارية المنخفضة تجعلها عازلاً فعالاً في هذه البيئات.
- مواد البناء: تستخدم في مواد البناء المختلفة مثل الطوب والبلاط والأسمنت. إن مقاومتها لدرجات الحرارة المرتفعة والنار تجعلها مادة مثالية للاستخدام في الجدران والأسقف المقاومة للحريق.
- المضافات الغذائية: تستخدم كعامل مضاد للتكتل في المنتجات الغذائية مثل السكر البودرة والملح. إن قدرته على امتصاص الرطوبة ومنع التكتل تجعله خيارًا شائعًا لدى مصنعي المواد الغذائية.
- المستحضرات الصيدلانية: يستخدم كسواغ في المنتجات الصيدلانية، حيث يعمل كمادة رابطة ومفككة وعامل تدفق.
- مستحضرات التجميل: تستخدم في مستحضرات التجميل كمادة منتفخة وماصة. يساعد على تحسين ملمس وملمس المنتجات مثل مساحيق الوجه وكريم الأساس.
- استخدامات أخرى: يستخدم أيضًا في إنتاج السيراميك والمواد المقاومة للحرارة وكمادة مالئة للمطاط والبلاستيك.
أسئلة:
س: كيف يمكنك إزالة سيليكات الكالسيوم من حمام السباحة؟
ج: لإزالة Ca2SiO4 من حمام السباحة، استخدم منظف بلاط حمام السباحة أو محلول حمض المرياتيك والماء. ضع المنظف أو المحلول على المنطقة المصابة وافركها بفرشاة صلبة. شطف مع الكثير من الماء بعد التنظيف.
س: كيفية صنع سيليكات الكالسيوم المقاومة للحرارة في المنزل؟
ج: لا يُنصح بتصنيع مادة Ca2SiO4 المقاومة للحرارة في المنزل بسبب درجات الحرارة المرتفعة والمعدات المتخصصة المطلوبة. من الأفضل شراء منتجات حرارية Ca2SiO4 مسبقة الصنع من مورد حسن السمعة.
س: مركبات سيليكات الكالسيوم ترطب لتكوين أي مركبين؟
ج: يتم ترطيب مركبات Ca2SiO4 لتكوين Ca2SiO4 المائي (CSH) وهيدروكسيد الكالسيوم (Ca(OH)2). تلعب هذه المركبات دورًا مهمًا في تكوين وقوة الخرسانة والمواد الأسمنتية الأخرى.
