ثلاثي فلوريد النيتروجين أو NF3 هو أحد غازات الدفيئة القوية المستخدمة في صناعة الإلكترونيات لحفر البلازما وتنظيفها. وله عمر طويل في الغلاف الجوي ويساهم في تغير المناخ.
| اسم الأيوباك | ثلاثي فلوريد النيتروجين |
| الصيغة الجزيئية | NF3 |
| CAS رقم | 7783-54-2 |
| المرادفات | ثلاثي فلورامين، فلوريد النيتروجين (NF3)، فلوريد النيتروجين (1: 3)، فلوريد النيتروجين (NF3)، فلوريد النيتروجين (III)، فلوريد النيتروجين، أقراص، رقم الأمم المتحدة 2451 |
| إنتشي | إنتشي = 1S/F3N/c1-4(2)3 |
الكتلة المولية لثلاثي فلوريد النيتروجين
الكتلة المولية لـ NF3 هي 71.0 جم/مول. وهذا يعني أن المول الواحد من NF3 يحتوي على 6,022 × 10^23 جزيء.
نقطة غليان ثلاثي فلوريد النيتروجين
NF3 لديه نقطة غليان -129.04 درجة مئوية أو -200.27 درجة فهرنهايت. وهذا منخفض نسبيًا مقارنة بالغازات الأخرى، مما يسهل التعامل معه في التطبيقات الصناعية.
نقطة انصهار ثلاثي فلوريد النيتروجين
يحتوي ثلاثي فلوريد النيتروجين على نقطة انصهار تبلغ -206.73 درجة مئوية أو -340.11 درجة فهرنهايت. وهذا يعني أنه في درجة حرارة الغرفة، يكون NF3 في حالة غازية.
كثافة NF3 جم/مل
تبلغ كثافة NF3 1.88 جم / مل عند درجة الحرارة والضغط القياسيين. وهذا يعني أن ثلاثي فلوريد النيتروجين أكثر كثافة من الهواء وسوف يهبط إلى الأرض إذا تم إطلاقه في الغلاف الجوي.
الوزن الجزيئي لثلاثي فلوريد النيتروجين
الوزن الجزيئي لـ NF3 هو 71.0 جم / مول. وهو مجموع الأوزان الذرية للنيتروجين والفلور في المركب.
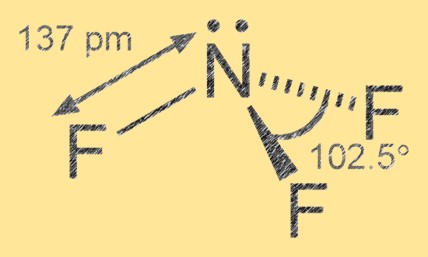
هيكل ثلاثي فلوريد النيتروجين
يحتوي ثلاثي فلوريد النيتروجين على هندسة جزيئية هرمية مثلثية مع النيتروجين كذرة مركزية وثلاث ذرات فلور تحيط به. رابطة النيتروجين-الفلور هي رابطة تساهمية قطبية، حيث تكون ذرات الفلور أكثر سالبية كهربية من النيتروجين، مما يؤدي إلى شحنة سالبة جزئية على ذرات الفلور وشحنة موجبة جزئية على ذرة النيتروجين.
صيغة ثلاثي فلوريد النيتروجين
الصيغة الكيميائية لثلاثي فلوريد النيتروجين هي NF3، مما يشير إلى أن جزيء واحد من NF3 يحتوي على ذرة نيتروجين واحدة وثلاث ذرات فلور.
| مظهر | غاز عديم اللون |
| جاذبية معينة | 2.62 |
| لون | عديم اللون |
| يشم | عديم الرائحة |
| الكتلة المولية | 71.0 جرام/مول |
| كثافة | 1.88 جم/مل عند STP |
| نقطة الانصهار | -206.73 درجة مئوية أو -340.11 درجة فهرنهايت |
| نقطة الغليان | -129.04 درجة مئوية أو -200.27 درجة فهرنهايت |
| نقطة فلاش | غير قابل للتطبيق |
| الذوبان في الماء | 0.41 جم/100 مل عند 25 درجة مئوية |
| الذوبان | قابل للذوبان في المذيبات العضوية |
| ضغط البخار | 315 كيلو باسكال عند 20 درجة مئوية |
| كثافة بخار | 2.01 (الهواء = 1) |
| pKa | غير قابل للتطبيق |
| الرقم الهيدروجيني | غير قابل للتطبيق |
سلامة ومخاطر ثلاثي فلوريد النيتروجين
يعتبر ثلاثي فلوريد النيتروجين (NF3) آمنًا بشكل عام إذا تم التعامل معه بشكل صحيح، ولكنه قد يشكل العديد من المخاطر إذا تم التعامل معه بشكل غير صحيح. قد يسبب تهيج الجلد والعين، كما أن استنشاق تركيزات عالية منه قد يسبب ضيق في التنفس. يمكن لغاز NF3 أن يحل محل الأكسجين في المناطق سيئة التهوية، مما يؤدي إلى الاختناق. وهو أيضًا أحد غازات الدفيئة القوية التي تساهم في تغير المناخ. في حالة نشوب حريق، قد يطلق NF3 غاز فلوريد الهيدروجين السام. من الضروري اتباع بروتوكولات السلامة المناسبة، بما في ذلك التهوية الكافية واستخدام معدات الحماية، عند التعامل مع NF3 لتجنب هذه المخاطر.
| رموز الخطر | ت، ج |
| وصف الأمان | تجنب استنشاقه وملامسته للجلد والعينين. لا تستخدم سوى في مناطق جيدة التهوية. |
| أرقام تعريف الأمم المتحدة | UN2451 |
| رمز النظام المنسق | 28129090 |
| فئة الخطر | 2.3 |
| مجموعة التعبئة | ثانيا |
| تسمم | سام جدا |
طرق تصنيع ثلاثي فلوريد النيتروجين
توجد عدة طرق لتصنيع ثلاثي فلوريد النيتروجين (NF3):
تتضمن الطريقة الشائعة تفاعل الأمونيا اللامائية (NH3) مع غاز الفلور (F2) في وجود محفز مثل الحديد أو النيكل أو البلاتين. ينتج عن التفاعل NF3 وفلوريد الهيدروجين (HF). تستخدم الصناعات عادةً هذه الطريقة لإنتاج NF3.
تتضمن الطريقة الأخرى التحلل الحراري لفلوريد الأمونيوم (NH4F) عند درجات حرارة عالية. ينتج عن التفاعل NF3 وغاز الأمونيا (NH3). يعتبر تفاعل NH3 مع F2 أكثر كفاءة من هذه الطريقة، لذلك فهو أقل استخدامًا.
تتضمن الطريقة الأخرى تفاعل أكسيد النيتريك (NO) مع غاز الفلور في وجود محفز. ينتج عن التفاعل غازات NF3 وثاني أكسيد النيتروجين (NO2).
يمكن أيضًا تصنيع NF3 كهروكيميائيًا عن طريق تمرير تفريغ كهربائي عبر خليط من غازات N2 وF2. تشكل البلازما الناتجة NF3 ومركبات النيتروجين والفلور الأخرى.
بغض النظر عن الطريقة المستخدمة، فمن الأهمية بمكان التعامل مع الكواشف شديدة التفاعل والتي يحتمل أن تكون خطرة مع احتياطات السلامة المناسبة. ومع ذلك، يجب على الباحثين التحكم بعناية في عملية التوليف لضمان إنتاجية عالية ونقاء المنتج النهائي.
استخدامات ثلاثي فلوريد النيتروجين
يحتوي ثلاثي فلوريد النيتروجين (NF3) على تطبيقات صناعية مختلفة نظرًا لخصائصه الفريدة.
- تستخدم صناعة أشباه الموصلات NF3 كعامل تنظيف لرقائق السيليكون. يستخدم NF3 أيضًا في إنتاج شاشات العرض المسطحة والخلايا الشمسية والأنظمة الكهروميكانيكية الدقيقة (MEMS).
- يستخدم تصنيع المكونات الإلكترونية NF3 كغاز حفر البلازما. يُظهر تفاعلًا عاليًا ويزيل مواد معينة بشكل انتقائي بينما يترك مواد أخرى سليمة.
- تستخدم أنظمة التبريد أيضًا NF3 كمبرد نظرًا لانخفاض احتمالية الاحتباس الحراري مقارنة بوسائل التبريد الأخرى، مما يجعله خيارًا أكثر صداقة للبيئة.
- تستخدم صناعة الطيران NF3 كوقود دافع بسبب نبضه النوعي العالي، والذي يتيح الدفع الفعال للمركبات الفضائية.
على الرغم من استخداماته العديدة، هناك مخاوف بشأن التأثير البيئي لـ NF3. وهو أحد غازات الدفيئة القوية وله عمر طويل في الغلاف الجوي. يمكن أن يساهم إنتاج واستخدام NF3 في تغير المناخ إذا لم يتم اتخاذ الاحتياطات المناسبة. ولهذا السبب تُبذل الجهود لتقليل استخدامه وتطوير بدائل أكثر استدامة.
أسئلة:
س: هل ثلاثي فلوريد النيتروجين (NF3) قطبي؟
ج: نعم، NF3 قطبي. وله هندسة جزيئية هرمية مثلثية، مع ذرة النيتروجين في المركز وثلاث ذرات الفلور مرتبة حوله. يسبب الشكل غير المتماثل للجزيء توزيعًا غير متساوٍ لكثافة الإلكترون، مما يؤدي إلى جزيء قطبي.
س: ما هي صيغة ثلاثي فلوريد النيتروجين؟
ج: صيغة ثلاثي فلوريد النيتروجين هي NF3، مما يشير إلى أن الجزيء يتكون من ذرة نيتروجين واحدة وثلاث ذرات فلور.
س: من أين يأتي ثلاثي فلوريد النيتروجين؟
ج: يمكن إنتاج NF3 بطرق مختلفة، بما في ذلك تفاعل الأمونيا اللامائية مع غاز الفلور، والتحلل الحراري لفلوريد الأمونيوم، والتوليف الكهروكيميائي. ويشيع استخدامه في صناعة أشباه الموصلات كعامل تنظيف وفي تصنيع المكونات الإلكترونية والدفاعات الفضائية.
س: تركيب لويس لثلاثي فلوريد النيتروجين؟
ج: يتكون هيكل لويس لـ NF3 من ذرة نيتروجين مرتبطة بثلاث ذرات فلور من خلال روابط تساهمية واحدة. يوجد أيضًا زوج من الإلكترونات غير المترابطة على ذرة النيتروجين، مما يعطي الجزيء شكلًا هرميًا ثلاثيًا.
س: القوى الجزيئية لثلاثي فلوريد النيتروجين؟
ج: تشمل القوى الجزيئية لـ NF3 تفاعلات ثنائية القطب، والتي تنتج عن الطبيعة القطبية للجزيء. يختبر الجزيئي أيضًا قوى تشتت لندن، وهي قوى ضعيفة بين الجزيئات ناتجة عن تقلبات مؤقتة في كثافة الإلكترون.
س: هل NF3 قطبي أم غير قطبي؟
ج: NF3 قطبي بسبب شكله غير المتماثل وتوزيعه غير المتساوي لكثافة الإلكترون. يمتلك الجزيء عزمًا ثنائي القطب، مما يشير إلى أن له نهاية موجبة وسالبة، مما يجعله جزيءًا قطبيًا.
