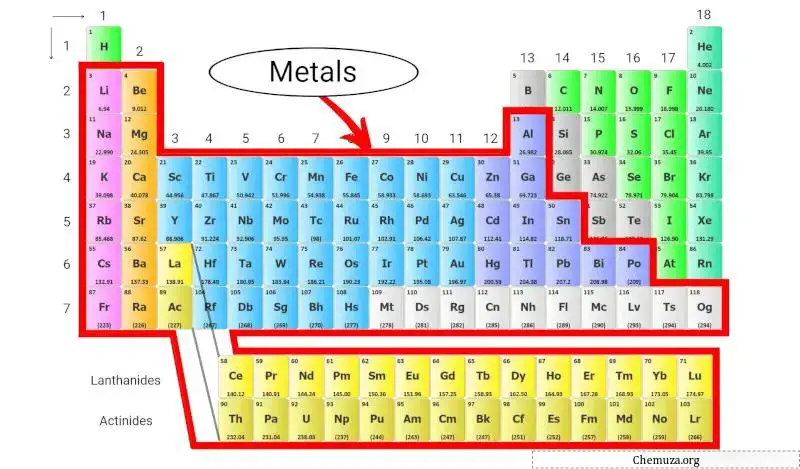
تعد معادن الجدول الدوري عناصر مهمة توجد في كل مكان حولنا، بدءًا من العملات المعدنية الموجودة في جيوبنا وحتى الأسلاك التي تمد منازلنا بالطاقة. في الواقع، معظم العناصر الموجودة في الجدول الدوري هي معادن!
وهي تشترك في بعض الخصائص المشتركة، مثل كونها لامعة، وموصلة جيدة للحرارة والكهرباء، وقابلة للطرق (أي يمكن ثنيها أو تشكيلها دون أن تنكسر). [1]
دعونا نستكشف المزيد عن المعادن وأنواع المعادن المختلفة الموجودة في الجدول الدوري.
ما هي المعادن بالضبط؟
المعادن هي عناصر تميل إلى فقدان الإلكترونات وتكوين الكاتيونات (أيونات موجبة الشحنة) عندما تخضع لتفاعلات كيميائية.
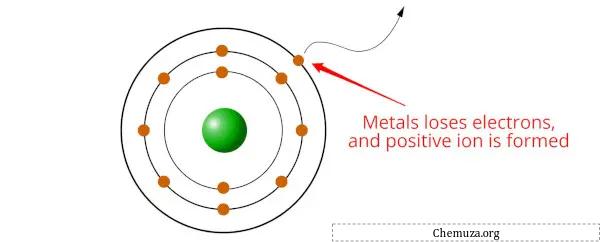
لكن هل تعلم لماذا يحدث هذا؟
وذلك لأن المعادن لديها طاقات تأين منخفضة، مما يعني أن الأمر يتطلب طاقة قليلة نسبيًا لإزالة إلكترون من ذرة المعدن. عندما تفقد ذرة فلز إلكترونًا واحدًا أو أكثر، فإنها تصبح كاتيونًا له شحنة موجبة.
تميل المعادن إلى فقدان الإلكترونات من أجل الحصول على تكوين إلكتروني أكثر استقرارًا، عادةً عن طريق الحصول على ثمانيّة مستقرة (أي 8 إلكترونات في الغلاف الخارجي).
الآن دعونا نلقي نظرة على الأنواع المختلفة للمعادن المصنفة في الجدول الدوري.
الفلزات القلوية
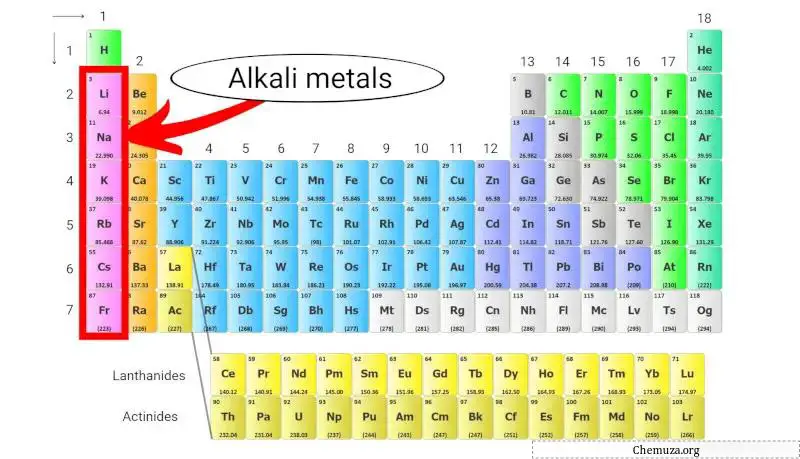
الفلزات القلوية هي مجموعة من العناصر في الجدول الدوري تتكون من الليثيوم (Li)، الصوديوم (Na)، البوتاسيوم (K)، الروبيديوم (Rb)، السيزيوم (Cs)، والفرانسيوم (Fr).
وهي تنتمي إلى المجموعة الأولى من الجدول الدوري، والمعروفة أيضًا باسم “مجموعة الفلزات القلوية”.
الفلزات القلوية شديدة التفاعل بسبب طاقات التأين المنخفضة، مما يجعلها أكثر عرضة لفقد إلكترون التكافؤ الفردي لتكوين كاتيون بشحنة +1. [2]
تعرف على المزيد عن: المعادن القلوية في الجدول الدوري .
المعادن الأرضية القلوية
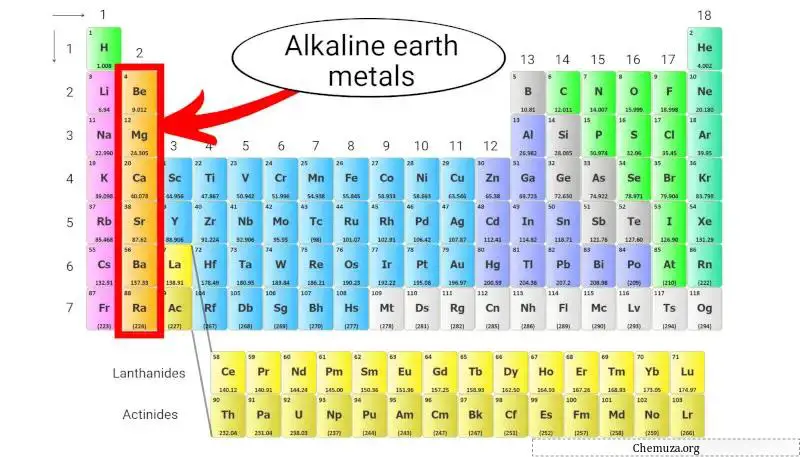
الفلزات القلوية الترابية هي مجموعة من العناصر في الجدول الدوري تتكون من البريليوم (Be)، والمغنيسيوم (Mg)، والكالسيوم (Ca)، والسترونتيوم (Sr)، والباريوم (Ba)، والراديوم (Ra).
وهم ينتمون إلى المجموعة الثانية من الجدول الدوري، والمعروفة أيضًا باسم “مجموعة المعادن الأرضية القلوية”.
الفلزات القلوية الترابية أقل تفاعلاً من الفلزات القلوية، لكنها مع ذلك تمتلك طاقات تأين منخفضة نسبيًا وتميل إلى تكوين كاتيونات بشحنة +2. [3]
تعرف على المزيد عن: المعادن الأرضية القلوية في الجدول الدوري .
المعادن الانتقالية
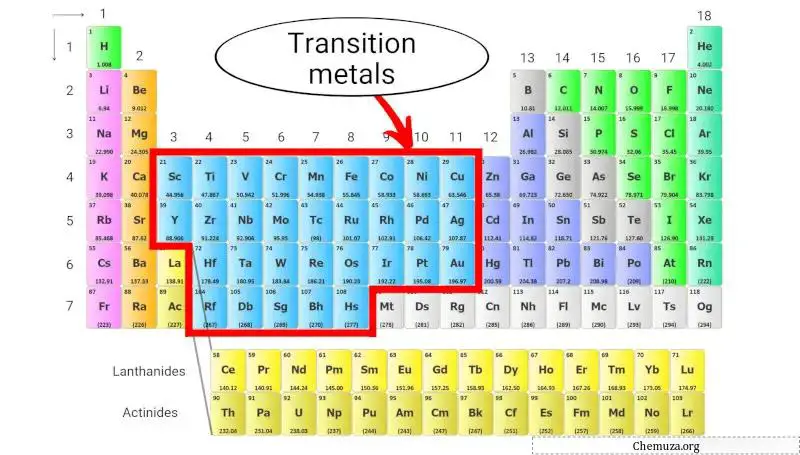
المعادن الانتقالية هي مجموعة من العناصر المعدنية الموجودة في وسط الجدول الدوري، وتحتل المجموعات من 3 إلى 11 (انظر الصورة أعلاه).
وتتميز بقدرتها على تكوين مركبات ملونة، وحالات الأكسدة المتعددة الخاصة بها ، وكثافاتها ونقاط انصهارها العالية نسبيًا.
تُعرف المعادن الانتقالية بتفاعلها الكيميائي، حيث يُستخدم الكثير منها كمحفزات في التفاعلات الكيميائية. كما أنها تستخدم في تطبيقات مختلفة، مثل إنتاج الصلب والسبائك الأخرى والإلكترونيات والبطاريات.
اعرف المزيد عن: المعادن الانتقالية في الجدول الدوري .
المعادن الانتقالية الداخلية
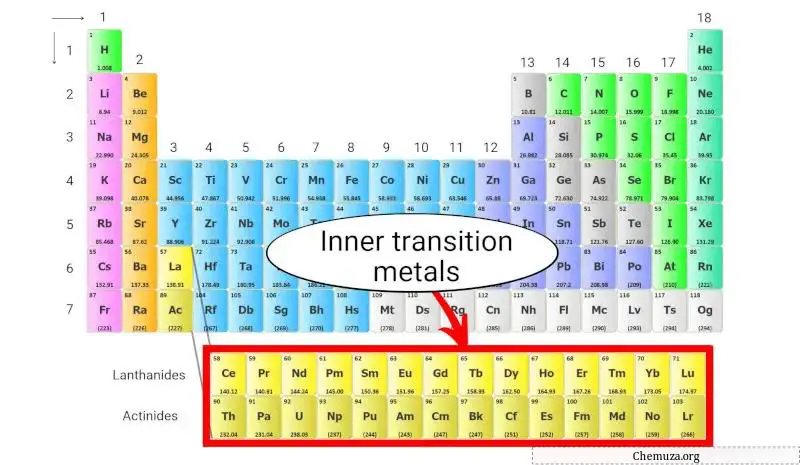
الفلزات الانتقالية الداخلية هي مجموعة من العناصر المعدنية الموجودة في أسفل الجدول الدوري، أسفل الجسم الرئيسي للجدول.
وهي مقسمة إلى مجموعتين فرعيتين:
- اللانثانيدات و
- الأكتينيدات.
يعتبر التكوين الإلكتروني للمعادن الانتقالية الداخلية فريدًا من نوعه، حيث تملأ الإلكترونات المدارات f لذراتها. وينتج عن ذلك خصائص إلكترونية ومغناطيسية مميزة، مما يجعلها مفيدة جدًا في التطبيقات التكنولوجية المختلفة.
اعرف المزيد عن: المعادن الانتقالية الداخلية في الجدول الدوري .
المعادن الأرضية النادرة
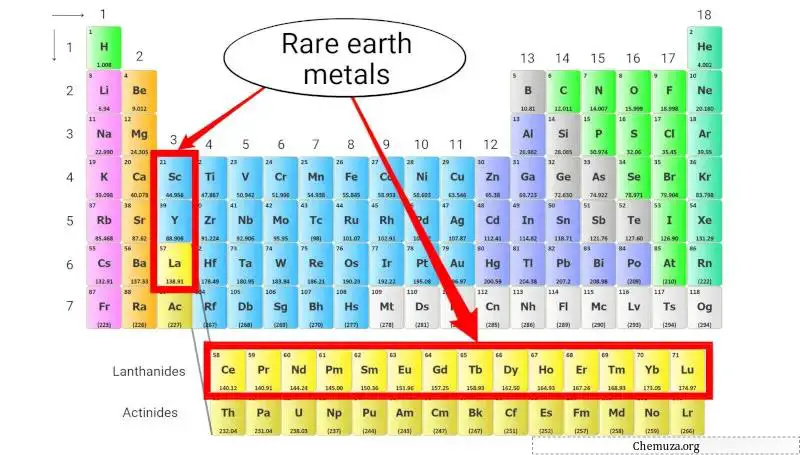
المعادن الأرضية النادرة، والمعروفة أيضًا بالعناصر الأرضية النادرة، هي مجموعة من العناصر المعدنية التي تشمل سلسلة اللانثانيدات (الأعداد الذرية من 57 إلى 71)، والسكانديوم (Sc)، والإيتريوم (Y).
على الرغم من اسمها، إلا أن المعادن الأرضية النادرة ليست نادرة في الواقع، ولكن من الصعب والمكلف استخراجها من الخامات بسبب تركيزاتها المنخفضة وتشابهها الكيميائي. [4]
معادن ثقيلة
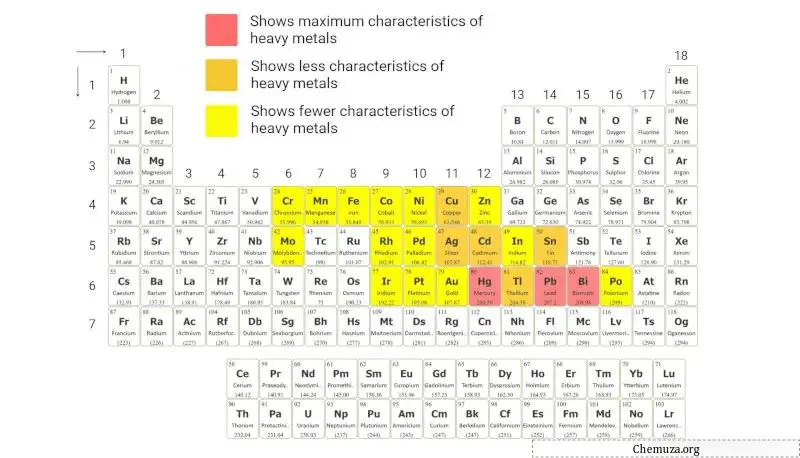
المعادن الثقيلة هي مجموعة من العناصر المعدنية التي لها كتلة وكثافة ذرية عالية نسبيًا.
يتم تحديد المعادن الثقيلة بشكل شائع من خلال معيار كثافتها العالية، والتي تكون عمومًا أكبر من 5 جم / سم مكعب .
ويقدم الجدول الدوري أعلاه تمثيلاً مرئيًا لهذه العناصر بناءً على هذا التصنيف.
تعرف على المزيد عن: المعادن الثقيلة في الجدول الدوري .
ملخص
المعادن هي عناصر تميل إلى فقدان الإلكترونات وتكوين الكاتيونات عندما تخضع لتفاعلات كيميائية. لديهم طاقات تأين منخفضة، مما يجعلها أكثر عرضة لفقد الإلكترونات وتصبح أيونات موجبة الشحنة.
يحتوي الجدول الدوري على عدة أنواع من المعادن، بما في ذلك الفلزات القلوية، والفلزات القلوية الترابية، والفلزات الانتقالية، والفلزات الانتقالية الداخلية، والفلزات الأرضية النادرة، والمعادن الثقيلة.
الفلزات القلوية شديدة التفاعل، في حين أن الفلزات القلوية الأرضية أقل تفاعلا. تُعرف المعادن الانتقالية بقدرتها على تكوين مركبات ملونة وحالات أكسدة متعددة، كما تمتلك المعادن الانتقالية الداخلية خصائص إلكترونية ومغناطيسية فريدة. من الصعب والمكلف استخراج المعادن الأرضية النادرة، في حين أن المعادن الثقيلة لها كثافات عالية.
