خلات النحاس (Cu(CH3COO)2) مركب بلوري أزرق مخضر. ويتكون عندما يتفاعل النحاس مع حمض الأسيتيك. يجد تطبيقات في مختلف الصناعات، مثل المواد الحفازة ومبيدات الفطريات.
| اسم الأيوباك | خلات النحاس (II). |
| الصيغة الجزيئية | النحاس (CH3COO)2 |
| CAS رقم | 142-71-2 |
| المرادفات | خلات النحاسيك، ملح النحاس لحمض الأسيتيك، ثنائي أسيتات النحاس |
| إنتشي | InChI=1S/2C2H4O2.Cu/c2 1-2(3)4;/h2 1H3,(H,3,4);/q;;+2/p-2 |
خصائص خلات النحاس
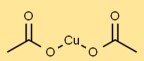
صيغة خلات النحاس
خلات النحاسيك لها الصيغة الكيميائية Cu(CH3COO)2. وتتكون من ذرة النحاس (Cu) المرتبطة بمجموعتي خلات (CH3COO). تمثل الصيغة نسبة العناصر في المركب.
خلات النحاس الكتلة المولية
يمكن حساب الكتلة المولية لخلات النحاسيك عن طريق إضافة الكتل الذرية للعناصر المكونة لها. يمتلك النحاس (Cu) كتلة مولية قدرها 63.55 جم/مول، بينما تبلغ الكتلة المولية للأسيتات (CH3COO) 59.04 جم/مول. وبالتالي، فإن الكتلة المولية لخلات النحاسيك هي 181.63 جم/مول.
نقطة غليان خلات النحاس
تتحلل خلات النحاسيك قبل الوصول إلى نقطة الغليان بسبب عدم استقرارها الحراري. ولذلك فإن نقطة الغليان ليست محددة بشكل جيد. وبدلا من ذلك، فإنه يخضع للتحلل عند تسخينه بشكل كبير.
نقطة انصهار خلات النحاس
تذوب خلات النحاسيك عادة بين 115 درجة مئوية و120 درجة مئوية (239 درجة فهرنهايت و248 درجة فهرنهايت). قد تختلف نقطة الانصهار قليلاً حسب نقاء المركب.
كثافة خلات النحاس جم/مل
تبلغ كثافة خلات النحاسيك حوالي 1.882 جم / مل. تتوافق هذه القيمة مع كتلة خلات النحاسيك لكل وحدة حجم. قد تختلف الكثافة مع التغيرات في درجة الحرارة والضغط.
الوزن الجزيئي لخلات النحاس
يبلغ الوزن الجزيئي لخلات النحاسيك، المحسوب من صيغته، 181.63 جم/مول. وهو يمثل مجموع الأوزان الذرية لجميع الذرات الموجودة في جزيء خلات النحاس.
هيكل خلات النحاس
تحتوي خلات النحاسيك على بنية شبكية بلورية في شكلها الصلب. تنسق ذرات النحاس مع مجموعات الأسيتات لتشكل ترتيبًا مستقرًا. يظهر على شكل بلورات زرقاء وخضراء بسبب هندسة التنسيق الخاصة به.
ذوبان خلات النحاس
خلات النحاسيك لديه ذوبان معتدل في الماء. يمكن أن يذوب في المذيبات القطبية بسبب وجود أيونات الخلات. ومع ذلك، قد تكون قابلية الذوبان محدودة وقد يتأثر ذوبانه بدرجة الحرارة ودرجة الحموضة.
| مظهر | مادة صلبة بلورية زرقاء وخضراء |
| جاذبية معينة | 1,882 جم/مل |
| لون | أزرق أخضر |
| يشم | عديم الرائحة |
| الكتلة المولية | 181.63 جرام/مول |
| كثافة | 1,882 جم/مل |
| نقطة الانصهار | 115 درجة مئوية – 120 درجة مئوية (239 درجة فهرنهايت – 248 درجة فهرنهايت) |
| نقطة الغليان | متحللة |
| نقطة فلاش | غير قابل للتطبيق |
| الذوبان في الماء | معتدلة الذوبان في الماء |
| الذوبان | قابل للذوبان في المذيبات القطبية، قابل للذوبان بشكل طفيف في الأثير والجلسرين |
| ضغط البخار | غير متاح |
| كثافة بخار | غير متاح |
| pKa | غير متاح |
| الرقم الهيدروجيني | حمض (حوالي 4-5) |
السلامة ومخاطر خلات النحاس
تشكل خلات النحاسيك بعض المخاوف والمخاطر المتعلقة بالسلامة. من الضروري التعامل معها بعناية واتباع بروتوكولات السلامة. الاتصال المباشر مع المركب قد يسبب تهيج الجلد والعين. استنشاق غباره أو أبخرةه قد يسبب إزعاجا في الجهاز التنفسي. تجنب ابتلاعه لأنه قد يكون ضارًا. احفظه بعيدًا عن المواد ومصادر الحرارة أو الاشتعال غير المتوافقة لتجنب خطر الحريق. في حالة التعرض العرضي، اشطف المناطق المتضررة على الفور واطلب العناية الطبية. قم بتخزين خلات النحاس في منطقة آمنة وجيدة التهوية بعيدًا عن متناول الأطفال والأشخاص غير المصرح لهم. استخدم دائمًا معدات الحماية الشخصية المناسبة عند العمل مع هذا المركب.
| رموز الخطر | تآكل، سامة حادة، مهيجة |
| وصف الأمان | تجنب الاتصال المباشر مع الجلد والعينين. استخدام في منطقة جيدة التهوية. التعامل مع الرعاية. |
| أرقام تعريف الأمم المتحدة | لا ينسب |
| رمز النظام المنسق | 29152900 |
| فئة الخطر | 6.1 (المواد السامة) |
| مجموعة التعبئة | III (خطر منخفض) |
| تسمم | قد يسبب تهيج الجلد والعين. استنشاق قد يسبب عدم الراحة في الجهاز التنفسي. تجنب تناوله. |
طرق تصنيع خلات النحاس
هناك عدة طرق لتجميع خلات النحاسيك.
يتضمن النهج الشائع التفاعل بين أكسيد النحاس (CuO) أو هيدروكسيد النحاس (Cu(OH)2) مع حمض الأسيتيك (CH3COOH). حيث تقوم بدمج المادتين وتحريكهما مما يؤدي إلى تكوين خلات النحاس والماء. طريقة أخرى هي تفاعل كربونات النحاس (CuCO3) مع حمض الأسيتيك لإنتاج خلات النحاسيك وثاني أكسيد الكربون (CO2) والماء.
تتضمن طريقة التخليق البديلة تفاعل النحاس المعدني مع خليط من حمض الأسيتيك وبيروكسيد الهيدروجين (H2O2). يؤدي هذا التفاعل إلى تكوين خلات النحاس والماء. تنتج خلات النحاسيك من التفاعل بين كبريتات النحاس (II) (CuSO4) وخلات الكالسيوم (Ca(CH3COO)2. وينتج عن هذا التفاعل خلات النحاسيك وكبريتات الكالسيوم (CaSO4).
تسخين وإرجاع خليط من مسحوق النحاس وحمض الخليك الجليدي ينتج خلات النحاسيك. تؤدي هذه العملية إلى تكوين خلات النحاس. إن توفر الكواشف والنقاء المطلوب للمنتج النهائي يحددان المزايا المميزة لكل طريقة.
استخدامات خلات النحاس
تجد خلات النحاس تطبيقات متعددة الاستخدامات في مختلف الصناعات نظرًا لخصائصها الفريدة. فيما يلي بعض الاستخدامات المهمة:
- المحفز: تحفز خلات النحاسيك العديد من التفاعلات العضوية، بما في ذلك تخليق خلات الفينيل وأنهيدريد الخل.
- الطلاء الكهربائي: تساعد خلات النحاس في عمليات الطلاء الكهربائي، حيث تنقل طبقة رقيقة من النحاس إلى الأجسام المعدنية، مما يحسن مظهرها ومقاومتها للتآكل.
- الوسطيات الكيميائية: يلعب المركب دورًا حاسمًا كوسيط في إنتاج المواد الكيميائية المختلفة مثل أكسيد النحاس ونفتينات النحاس وصابون النحاس.
- مادة حافظة للخشب: تعمل أسيتات النحاس كمادة حافظة للخشب، حيث تحمي الخشب من هجوم الفطريات والحشرات، وتستخدم عادة للحفاظ على روابط السكك الحديدية وأعمدة الكهرباء.
- مبيد الفطريات: في الزراعة، تستخدم خلات النحاس كمبيد للفطريات لمكافحة الأمراض الفطرية في المحاصيل، وخاصة في كروم العنب والبساتين.
- الألعاب النارية: يتم استخدام خلات النحاس في تركيبات الألعاب النارية، مما ينتج ألوانًا زرقاء وخضراء نابضة بالحياة في الألعاب النارية والمشاعل.
- صبغ المنسوجات: يعمل كمادة لاصقة في عمليات صبغ المنسوجات، مما يسهل ربط الأصباغ بالألياف.
- الكاشف المختبري: يعمل المركب ككاشف في التجارب المعملية للتحليلات النوعية والكمية.
- الكيمياء التحليلية: تستخدم خلات النحاس ككاشف اختبار في الكيمياء التحليلية للكشف عن غاز كبريتيد الهيدروجين.
- طارد الحيوانات: يعمل كطارد للحيوانات لردع بعض الآفات والحياة البرية من مناطق محددة.
تسلط التطبيقات المتنوعة لخلات النحاسيك الضوء على أهميتها في مختلف الصناعات، بدءًا من التركيب الكيميائي إلى الزراعة وما بعدها. يعد التعامل الدقيق واتباع احتياطات السلامة أمرًا ضروريًا عند استخدام هذا المركب في عمليات مختلفة.
أسئلة:
س: هل خلات النحاس II تساهمية؟
ج: لا، خلات النحاسيك II مركب أيوني.
س: ما هو معامل الانقراض المولي عند 625 نانومتر لمحلول خلات النحاس II؟
ج: إن معامل الانقراض المولي عند 625 نانومتر لمحلول خلات النحاسيك II خاص بتركيز المحلول ويجب تحديده تجريبياً.
س: هل يمكنك وضع مونوهيدرات خلات النحاسيك في خزان الصرف الصحي؟
ج: لا يُنصح باستخدام مونوهيدرات خلات النحاس كخزان للصرف الصحي أو منظف للصرف بسبب المخاطر المحتملة والمخاوف البيئية.
س: هل يحدث تفاعل عند دمج المحاليل المائية لخلات الباريوم وبروميد النحاس الثنائي؟
ج: نعم، يحدث التفاعل عندما يتم دمج المحاليل المائية لخلات الباريوم وبروميد النحاسيك (II)، مما يؤدي إلى تكوين راسب (بروميد الباريوم) وخلات النحاسيك القابلة للذوبان.
س: ما هي درجة انصهار خلات النحاسيك؟
ج: تبلغ نقطة انصهار خلات النحاسيك حوالي 115 درجة مئوية إلى 120 درجة مئوية (239 درجة فهرنهايت إلى 248 درجة فهرنهايت).
س: كيفية صنع خلات النحاس من كبريتات النحاس؟
ج: لتحضير خلات النحاسيك من CuSO4، قم بإذابة CuSO4 في الماء، ثم أضف حمض الأسيتيك إلى المحلول حتى تترسب خلات النحاسيك. تصفية وتجفيف المنتج.
س: ما هو خلات النحاسيك؟
ج: خلات النحاسيك مركب كيميائي له الصيغة Cu(CH3COO)2. وهي مادة صلبة بلورية زرقاء وخضراء ولها تطبيقات صناعية مختلفة.
س: هل خلات النحاسيك قابلة للذوبان في الماء؟
ج: نعم، خلات النحاسيك قابلة للذوبان بشكل معتدل في الماء، وتشكل محلولاً أزرق مخضر.
س: لماذا يكون محلول خلات النحاسيك غائما؟
ج: قد يصبح محلول خلات النحاسيك غائما بسبب وجود شوائب أو تكوين مركبات النحاس غير القابلة للذوبان، خاصة إذا لم يتم تحضير المحلول أو تخزينه بشكل صحيح.
س: أكسدة Cu(OAc)2؟
ج: يمكن لخلات النحاس (II) (Cu(OAc)2) أن تعمل كعامل مؤكسد في بعض التفاعلات، حيث تخضع للاختزال أثناء أكسدة مواد أخرى.
