بورات الصوديوم مركب يستخدم في مختلف الصناعات. له تطبيقات متعددة، كعامل تنظيف، وتدفق في المعادن ومكون في مستحضرات التجميل والمنظفات.
| اسم الأيوباك | بلورات الصوديوم |
| الصيغة الجزيئية | Na2B4O7 |
| CAS رقم | 1330-96-4 |
| المرادفات | البوراكس، رباعي بورات الصوديوم، رباعي بورات الصوديوم، بيبورات الصوديوم |
| إنتشي | InChI=1S/B4O7.2Na/c5-1-7-3-9-2-8-4-10-3;;/q-2;2*+1 |
خصائص بورات الصوديوم
صيغة بورات الصوديوم
الصيغة الكيميائية لبورات الصوديوم هي Na2B4H20O17. وتتكون من ذرتين صوديوم (Na)، وأربع ذرات بورون (B)، وسبع ذرات أكسجين (O). تمثل الصيغة نسبة كل عنصر في المركب.
بورات الصوديوم الكتلة المولية
يتم حساب الكتلة المولية للبوراكس عن طريق إضافة الكتل الذرية لجميع الذرات الموجودة في المركب. تبلغ الكتلة المولية للبوراكس حوالي 381.37 جرامًا لكل مول (جم / مول). ومن المفيد تحديد كمية المادة الموجودة في عينة معينة.
درجة غليان بورات الصوديوم
يحتوي البوراكس على نقطة غليان عالية نسبيًا. عند الضغط الجوي القياسي، فإنه يغلي عند حوالي 1.575 درجة مئوية (C). نقطة الغليان العالية هذه تجعلها مناسبة لمختلف التطبيقات الصناعية التي تنطوي على عمليات ذات درجات حرارة عالية.
نقطة انصهار بورات الصوديوم
تبلغ درجة انصهار البوراكس حوالي 741 درجة مئوية (C). ويخضع لمرحلة انتقالية من الحالة الصلبة إلى الحالة السائلة عند درجة الحرارة هذه. تسمح نقطة الانصهار المنخفضة نسبيًا للبوراكس بالذوبان بسهولة واستخدامه في عمليات التصنيع المختلفة.
كثافة بورات الصوديوم جم/مل
تبلغ كثافة البوراكس حوالي 1.73 جرام لكل ملليلتر (جم / مل). الكثافة هي مقياس لكمية الكتلة الموجودة في حجم معين. إن الكثافة العالية نسبيًا للبوراكس تجعله مركبًا مفيدًا في التطبيقات التي يكون فيها وزنه أو تركيزه مهمًا.
الوزن الجزيئي لبورات الصوديوم
يبلغ الوزن الجزيئي للبوراكس حوالي 381.37 جرامًا لكل مول (جم / مول). وهو يمثل مجموع الأوزان الذرية لجميع الذرات الموجودة في جزيء البوراكس. الوزن الجزيئي ضروري لمختلف العمليات الحسابية، مثل تحديد عدد الشامات أو كتلة المادة.
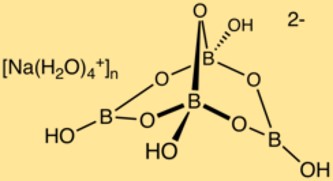
هيكل بورات الصوديوم
يحتوي البوراكس على بنية بلورية معقدة تتكون من متعددات وجوه البورون والأكسجين وأيونات الصوديوم. تشكل ذرات البورون شبكة مع ذرات الأكسجين لتكوين بنية ثلاثية الأبعاد. وتقع أيونات الصوديوم في هذا الهيكل، مما يضمن استقرار المركب.
ذوبان بورات الصوديوم
البوراكس قابل للذوبان بشكل معتدل في الماء. يذوب بسهولة في الماء الساخن وتزداد ذوبانه مع ارتفاع درجة الحرارة. ومع ذلك، فإن قابليته للذوبان في المذيبات العضوية محدودة. إن قابلية ذوبان البوراكس تجعله مفيدًا لمجموعة متنوعة من التطبيقات، بما في ذلك استخدامه كعامل تنظيف وفي صياغة المحاليل والمخاليط.
| مظهر | مسحوق بلوري أبيض |
| جاذبية معينة | 1.73 جم/مل |
| لون | أبيض |
| يشم | عديم الرائحة |
| الكتلة المولية | 381.37 جرام/مول |
| كثافة | 1.73 جم/مل |
| نقطة الانصهار | 741 درجة مئوية |
| نقطة الغليان | 1575 درجة مئوية |
| نقطة فلاش | غير قابل للتطبيق |
| الذوبان في الماء | قابل للذوبان |
| الذوبان | قابل للذوبان في الماء، محدودية الذوبان في المذيبات العضوية |
| ضغط البخار | غير متاح |
| كثافة بخار | غير متاح |
| pKa | غير قابل للتطبيق |
| الرقم الهيدروجيني | حوالي الساعة 9 صباحًا حتى 10 صباحًا |
السلامة ومخاطر بورات الصوديوم
يجب التعامل مع البوراكس بحذر بسبب المخاطر المحتملة على السلامة. قد يسبب تهيج الجلد والعينين والجهاز التنفسي عن طريق الاتصال المباشر أو الاستنشاق. تناول كميات كبيرة قد يسبب اضطراب في الجهاز الهضمي. وينبغي استخدام تدابير الحماية، مثل القفازات والنظارات الواقية، عند العمل مع البوراكس لتجنب التعرض. ومن المهم تخزينه في مكان آمن وجيد التهوية، بعيدًا عن المواد غير المتوافقة. في حالة حدوث ابتلاع أو التعرض العرضي، يجب طلب العناية الطبية الفورية. ينبغي الرجوع إلى أوراق بيانات سلامة المواد المناسبة وتعليمات المناولة للحصول على معلومات مفصلة عن مخاطر البوراكس واحتياطات السلامة.
| رموز الخطر | سامة |
| وصف الأمان | ضارة إذا ابتلعت. يسبب تهيج الجلد والعين. |
| أرقام تعريف الأمم المتحدة | الأمم المتحدة 1458 |
| رمز النظام المنسق | 2840.19.20 |
| فئة الخطر | 6.1 (المواد السامة) |
| مجموعة التعبئة | ثالثا |
| تسمم | سمية معتدلة عن طريق الابتلاع أو ملامسة الجلد/العين. |
طرق تصنيع بورات الصوديوم
هناك عدة طرق لتجميع البوراكس. الطريقة الشائعة هي التفاعل بين البوراكس (رباعي بورات الصوديوم) وكربونات الصوديوم . في هذه العملية، قم بإذابة البوراكس في الماء ثم أضف كربونات الصوديوم إلى المحلول. ويحدث التفاعل، مكونًا البوراكس وترسب المادة الصلبة. افصل المادة الصلبة وجففها للحصول على البوراكس.
هناك طريقة أخرى تتمثل في إذابة حمض البوريك في الماء وإضافة هيدروكسيد الصوديوم تدريجيًا إلى المحلول. يحدث التفاعل ويشكل البوراكس. قم بتبخر المحلول لإزالة الماء الزائد والحصول على بلورات البوراكس.
بالإضافة إلى ذلك، قم بخلط أكسيد البورون مع هيدروكسيد الصوديوم في مذيب مناسب وقم بتسخين الخليط. يحدث التفاعل ويشكل البوراكس. قم بتصفية الخليط لفصل الشوائب واترك المرشح ليبرد ويتبلور، مما ينتج عنه البوراكس.
توفر هذه الطرق الاصطناعية طرقًا للحصول على البوراكس بطريقة خاضعة للرقابة. ومع ذلك، فمن المهم اتباع احتياطات السلامة المناسبة والتعامل مع المواد الكيميائية بطريقة مسؤولة أثناء عملية التوليف.
استخدامات بورات الصوديوم
للبوراكس، المعروف أيضًا باسم البوراكس، نطاق واسع من الاستخدامات في مختلف الصناعات نظرًا لخصائصه المتنوعة. فيما يلي بعض تطبيقاته الشائعة:
- التدفق في علم المعادن: يعمل بمثابة تدفق في تطبيقات اللحام والنحاس، مما يساعد على تقليل درجة انصهار المعادن وتسهيل تدفق المعدن المنصهر.
- مثبطات اللهب: يتم تطبيقها كمثبطات للهب في مواد مختلفة بما في ذلك عزل السليلوز والمنسوجات والمنتجات الخشبية.
- الزجاج والسيراميك: يعتبر البوراكس عنصراً أساسياً في صناعة الزجاج والسيراميك. فهو يساعد على خفض درجة الانصهار وتحسين المتانة وتحسين الخصائص البصرية لهذه المواد.
- المخزن المؤقت للأس الهيدروجيني: يعمل كمخزن مؤقت للأس الهيدروجيني في المختبرات والتجارب العلمية.
- عامل التنظيف: تستخدم المنتجات المنزلية مثل منظفات الغسيل وصابون الأطباق والمنظفات متعددة الأغراض البوراكس بشكل فعال كعامل تنظيف.
- مستحضرات التجميل: تستخدم مستحضرات التجميل ومنتجات العناية الشخصية البوراكس كعامل تخزين مؤقت وضبط درجة الحموضة ومستحلب.
- المواد الحافظة: تحتوي المنتجات الخشبية على مادة البوراكس كمادة حافظة لمنع الإصابة بالفطريات والحشرات.
- الزراعة: يعمل البوراكس كسماد من المغذيات الدقيقة لتصحيح نقص البورون في المحاصيل، وبالتالي تعزيز نمو النبات الصحي.
- التطبيقات الطبية: تشتمل التركيبات الطبية على البوراكس لخصائصه المطهرة والقابضة.
- معالجة المياه: تستخدم عمليات معالجة المياه البوراكس لمنع نمو الطحالب والتحكم في مستويات الرقم الهيدروجيني.
تسلط هذه التطبيقات المتنوعة الضوء على أهمية البوراكس في مختلف الصناعات، مما يجعله مركبًا قيمًا ومتعدد الاستخدامات.
أسئلة:
س: ما هي استخدامات بورات الصوديوم؟
ج: يستخدم البوراكس كعامل تنظيف، وتدفق في علم المعادن، ومكون في مستحضرات التجميل، ومثبطات اللهب، وفي صناعة الزجاج/السيراميك، كمادة حافظة للخشب، وما إلى ذلك.
س: أين يمكن شراء بورات الصوديوم؟
ج: يمكن شراء البوراكس من العديد من موردي المواد الكيميائية ومتاجر الأجهزة والأسواق عبر الإنترنت وبعض متاجر البقالة.
س: ما هو الكاتيون عندما يذوب بورات الصوديوم؟
ج: الكاتيون المنطلق عند ذوبان البوراكس هو الصوديوم (Na+).
س: هل بورات الصوديوم هو نفس حمض البوريك؟
ج: لا، البوراكس وحمض البوريك مركبان مختلفان، على الرغم من أن كلاهما يحتوي على البورون.
س: هل بورات الصوديوم هو نفسه البوراكس؟
ج: نعم، يُسمى البوراكس عادةً بالبوراكس.
س: هل يعتمد بورات الصوديوم؟
ج: يعمل البوراكس كقاعدة ضعيفة في المحاليل المائية.
س: هل بورات الصوديوم آمنة للشرب؟
ج: لا ينبغي تناول البوراكس، لأنه قد يكون سامًا. ليس المقصود للاستهلاك.
س: هل يقوم بورات الصوديوم بتحييد حمض الكبريتيك؟
ج: لا، لا يقوم البوراكس بتحييد حمض الكبريتيك. يمكن أن تتفاعل ولكنها لن تحييدها تمامًا.
س: ما هي وظيفة بورات الصوديوم في محلول الشطف ذو الرقم الهيدروجيني 10؟
ج: يسهل البوراكس الموجود في محلول الشطف ذو الرقم الهيدروجيني 10 شطف الجزيئات الحيوية سالبة الشحنة من أعمدة التحليل اللوني.
س: ما هو البوراكس؟
ج: البوراكس، المعروف أيضًا باسم بورات الصوديوم، هو مركب معدني طبيعي يتكون من جزيئات الصوديوم والبورون والأكسجين والماء.
س: ماذا يحدث عندما يتم تسخين البوراكس بقوة؟
ج: عندما يتم تسخين البوراكس بقوة فإنه يتعرض للجفاف ويفقد جزيئات الماء الخاصة به، مما يؤدي إلى تكوين البوراكس اللامائي.
س: هل البوراكس هو نفسه حمض البوريك؟
ج: لا، البوراكس وحمض البوريك مركبان مختلفان. البوراكس هو بورات الصوديوم، في حين أن حمض البوريك هو شكل حمضي من البورون.
س: ما هو مسحوق البوراكس؟
ج: يشير مسحوق البوراكس إلى الشكل المسحوق للبوراكس، والذي يستخدم في مجموعة متنوعة من الأغراض مثل التنظيف والغسيل والحرف اليدوية.
