ثلاثي كلوريد الفوسفور هو مركب كيميائي يتكون من الفوسفور وثلاث ذرات الكلور. يستخدم عادة ككاشف في التفاعلات الكيميائية وكمقدمة لمركبات الفسفور العضوي.
| اسم الأيوباك | ثلاثي كلوريد الفوسفور |
| الصيغة الجزيئية | PCl3 |
| CAS رقم | 7719-12-2 |
| المرادفات | ثلاثي كلوروفوسفين، كلوريد الفوسفور، ثلاثي كلوريد الفوسفور، كلوريد الفوسفور (III). |
| إنتشي | إنتشي = 1S/Cl3P/c1-4(2)3 |
خصائص ثلاثي كلوريد الفوسفور
صيغة ثلاثي كلوريد الفوسفور
صيغة ثلاثي كلوريد الفوسفور هي PCl3. وتتكون من ذرة فسفور مرتبطة بثلاث ذرات كلور. يستخدم هذا المركب الكيميائي على نطاق واسع في مختلف الصناعات والمختبرات لتفاعله وتعدد استخداماته.
ثلاثي كلوريد الفوسفور الكتلة المولية
يمكن حساب الكتلة المولية لثلاثي كلوروفوسفين عن طريق إضافة الكتل الذرية للعناصر المكونة له. تبلغ الكتلة الذرية للفوسفور حوالي 31.0 جرامًا لكل مول، بينما تبلغ الكتلة الذرية للكلور حوالي 35.5 جرامًا لكل مول. وبالتالي، تبلغ الكتلة المولية لـ PCl3 حوالي 137.3 جرامًا لكل مول.
نقطة غليان ثلاثي كلوريد الفوسفور
تبلغ درجة غليان ثلاثي كلوروفوسفين حوالي 76.1 درجة مئوية. وهذا يعني أنه عند تسخينه يتحول من سائل إلى غاز. تعتبر نقطة الغليان خاصية مهمة يجب مراعاتها عند التعامل مع ثلاثي كلوروفوسفين واستخدامه في التفاعلات والعمليات الكيميائية المختلفة.
نقطة انصهار ثلاثي كلوريد الفوسفور
تبلغ نقطة انصهار ثلاثي كلوروفوسفين حوالي -112.7 درجة مئوية. ويخضع لمرحلة انتقالية من الحالة الصلبة إلى الحالة السائلة عند درجة الحرارة هذه. تعتبر نقطة الانصهار خاصية حاسمة لتحديد الحالة الفيزيائية لثلاثي كلوروفوسفين في ظل ظروف مختلفة.
كثافة ثلاثي كلوريد الفوسفور جم/مل
تبلغ كثافة ثلاثي كلوروفوسفين حوالي 1.574 جرام لكل مليلتر. تمثل الكثافة كتلة المادة لكل وحدة حجم وتوفر نظرة ثاقبة على تماسك المادة وثقلها. غالبًا ما تستخدم كثافة ثلاثي كلوروفوسفين في الحسابات والتركيبات الكيميائية.
الوزن الجزيئي لثلاثي كلوريد الفوسفور
يبلغ الوزن الجزيئي لثلاثي كلوروفوسفين، المحسوب عن طريق إضافة الأوزان الذرية لمكوناته، حوالي 137.3 جرامًا لكل مول. يعد الوزن الجزيئي معلمة قيمة لتحديد كمية المادة في التفاعلات الكيميائية وصياغة قياسات دقيقة.
هيكل ثلاثي كلوريد الفوسفور
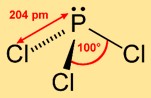
يعتمد ثلاثي كلوروفوسفين على هيكل هرمي ثلاثي، حيث تحتل ذرة الفوسفور القمة وتشكل ذرات الكلور الثلاث قاعدة مثلثة. يساهم هذا الترتيب الجزيئي في تفاعله الكيميائي ويؤثر على سلوكه في التفاعلات المختلفة.
ذوبان ثلاثي كلوريد الفوسفور
ثلاثي كلوروفوسفين قابل للذوبان بشكل سيئ في الماء، لكنه يذوب بسهولة في المذيبات العضوية مثل البنزين ورابع كلوريد الكربون. تعتبر خصائص ذوبان ثلاثي كلوروفوسفين من الاعتبارات الأساسية عند تحديد المذيبات المناسبة لاستخدامه في العمليات والتطبيقات الكيميائية المختلفة.
| مظهر | سائل عديم اللون أو أصفر شاحب |
| جاذبية معينة | 1,574 جم/مل |
| لون | عديم اللون |
| يشم | فدان |
| الكتلة المولية | 137.3 جرام/مول |
| كثافة | 1,574 جم/مل |
| نقطة الانصهار | -112.7 درجة مئوية |
| نقطة الغليان | 76.1 درجة مئوية |
| نقطة فلاش | غير قابل للتطبيق (غير قابل للاشتعال) |
| الذوبان في الماء | يتفاعل مع الماء |
| الذوبان | قابل للذوبان في المذيبات العضوية مثل البنزين ورابع كلوريد الكربون |
| ضغط البخار | 105 ملم زئبق عند 25 درجة مئوية |
| كثافة بخار | 4.83 (الهواء = 1) |
| pKa | غير قابل للتطبيق |
| الرقم الهيدروجيني | حمض (الرقم الهيدروجيني <7) |
السلامة ومخاطر ثلاثي كلوريد الفوسفور
يشكل ثلاثي كلوروفوسفين العديد من مخاطر السلامة ويجب التعامل معه بحذر. وهو شديد التآكل للجلد والعينين والجهاز التنفسي. الاتصال المباشر يمكن أن يسبب حروقا شديدة وتلف العين. استنشاق أبخرةه قد يسبب تهيج الجهاز التنفسي وتلف الرئة. بالإضافة إلى ذلك، يتفاعل ثلاثي كلوروفوسفين بعنف مع الماء، ويطلق أبخرة حمض الهيدروكلوريك السامة. إنه قابل للاشتعال في ظل ظروف معينة وقد يؤدي الاتصال بالعوامل المؤكسدة إلى حدوث حرائق أو انفجارات. وينبغي استخدام معدات الحماية الشخصية الكافية، مثل القفازات والنظارات الواقية وجهاز التنفس الصناعي، عند العمل مع هذه المادة الكيميائية. تعد التهوية والتخزين المناسبين بعيدًا عن المواد غير المتوافقة أمرًا ضروريًا لتقليل المخاطر.
| رموز الخطر | تآكل، سامة |
| وصف الأمان | – يسبب حروقا جلدية شديدة وتلفا للعين – ضار في حالة البلع أو الاستنشاق أو الامتصاص – يتفاعل بعنف مع الماء وينبعث منه أبخرة سامة – قابل للاشتعال في ظل ظروف معينة |
| معرفات الأمم المتحدة | UN1809 |
| رمز النظام المنسق | 2812.10.00 |
| فئة الخطر | 8 (تآكل)، 6.1 (سام) |
| مجموعة التعبئة | ثانيا |
| تسمم | سام جدا |
طرق تصنيع ثلاثي كلوريد الفوسفور
طرق مختلفة لتجميع ثلاثي كلوروفوسفين. الطريقة الشائعة هي تسخين الفوسفور بغاز الكلور الزائد، مما يؤدي إلى تكوين ثلاثي كلوروفوسفين.
تتضمن الطريقة الأخرى تسخين خماسي كلوريد الفوسفور (PCl5) مع ثلاثي كلوروفوسفين (PCl3) لإنتاج ثلاثي كلوروفوسفين.
التفاعل بين أكسيد الفوسفور (P2O5) وحمض الهيدروكلوريك (HCl) يجمع بين المادتين، عادة مع مكثف راجع، لتسهيل تخليق ثلاثي كلوروفوسفين.
بالإضافة إلى ذلك، يؤدي تسخين ثلاثي بروميد الفوسفور (PBr3) مع ثلاثي كلوروفوسفين إلى إنتاج ثلاثي كلوروفوسفين.
ومن المهم أن نلاحظ أن تصنيع ثلاثي كلوروفوسفين يجب أن يتم مع احتياطات السلامة المناسبة، لأنه ينطوي على التعامل مع المواد المتفاعلة والخطرة. ضمان السلامة أثناء عملية التوليف من خلال استخدام معدات الحماية المناسبة والحفاظ على ظروف المختبر جيدة التهوية.
بشكل عام، توفر هذه الطرق الاصطناعية المختلفة طرقًا مختلفة للحصول على ثلاثي كلوروفوسفين، وبالتالي توفر المرونة في إنتاجه لمجموعة واسعة من التطبيقات الصناعية والبحثية.
استخدامات ثلاثي كلوريد الفوسفور
يستخدم ثلاثي كلوروفوسفين على نطاق واسع في العديد من التطبيقات بسبب طبيعته المتنوعة وتفاعله. فيما يلي بعض الاستخدامات الرئيسية:
- الكاشف الكيميائي: يعمل ككاشف مهم في التركيب العضوي، وخاصة في إنتاج مركبات الفسفور العضوي. ويشارك في ردود الفعل مثل رد فعل فيلسماير-هاك ورد فعل بودوفيك.
- المحفز: يعمل ثلاثي كلوروفوسفين كمحفز في التفاعلات الكيميائية المختلفة، بما في ذلك تصنيع الأدوية والأصباغ والمبيدات الحشرية.
- مصدر الفوسفور: يعمل كمصدر للفوسفور في إنتاج المواد الكيميائية القائمة على الفوسفور مثل حمض الفوسفور وأوكسي كلوريد الفوسفور.
- مثبطات اللهب: يضيف المصنعون ثلاثي كلوروفوسفين كمثبط للهب إلى البوليمرات، مما يساعد على تقليل القابلية للاشتعال وتحسين سلامة المواد من الحرائق.
- الوسيط الكيميائي: يتم إنتاج مواد كيميائية مختلفة، بما في ذلك الأدوية ومبيدات الأعشاب والمبيدات الحشرية والملدنات، باستخدام ثلاثي كلوروفوسفين كمادة وسيطة حاسمة.
- الكاشف المختبري: تستخدم المختبرات على نطاق واسع ثلاثي كلوروفوسفين ككاشف متعدد الاستخدامات للتفاعلات الكيميائية، بما في ذلك تكوين كلوريد الأسيل وتحويل الكحوليات إلى كلوريد الألكيل.
- معالجة المياه: خصائص الأكسدة والكلور القوية لثلاثي كلوروفوسفين تجعله عنصرًا قيمًا في عمليات معالجة المياه، مما يزيل الشوائب والملوثات بشكل فعال.
- المستحضرات الصيدلانية: يلعب ثلاثي كلوروفوسفين دورًا في تركيب المركبات الصيدلانية، بما في ذلك أدوية علاج السرطان والالتهابات والاضطرابات العصبية.
- التطبيقات الزراعية: له تطبيقات في الزراعة كأحد مكونات بعض المبيدات الحشرية ومبيدات الأعشاب، مما يساهم في حماية المحاصيل ومكافحة الأعشاب الضارة.
- تصنيع البلاستيك: يستخدم المصنعون ثلاثي كلوروفوسفين في إنتاج البلاستيك ومضافات البوليمر لتحسين خصائص المواد وجعلها مثبطات للهب.
تسلط هذه التطبيقات المختلفة الضوء على أهمية ثلاثي كلوروفوسفين في مختلف الصناعات والأبحاث والتطبيقات اليومية.
أسئلة:
س: هل ثلاثي كلوريد الفسفور قاعدة أم حمض؟
ج: ثلاثي كلوروفوسفين حمض.
س: ما عدد ذرات الكلور الموجودة في جزيء ثلاثي كلوريد الفوسفور PCl3؟
ج: هناك ثلاث ذرات كلور في جزيء ثلاثي كلوروفوسفين.
س: ما النسبة المئوية للتفاعل الذي يتفاعل فيه 200 جم من ثلاثي كلوريد الفوسفور؟
ج: لا يمكن تحديد نسبة الإنتاج دون معلومات عن كمية المنتج الذي تم الحصول عليه.
س: كم عدد الشامات الموجودة في 15 جرام من ثلاثي كلوريد الفوسفور؟
ج: يوجد ما يقرب من 0.116 مول من ثلاثي كلوروفوسفين في 15 جرام.
س: ما الصيغة التي تمثل المركب الجزيئي الثنائي ثلاثي كلوريد الفوسفور؟
ج: الصيغة PCl3 تعني ثلاثي كلوروفوسفين.
س: ما هي صيغة ثلاثي كلوريد الفوسفور؟
ج: صيغة ثلاثي كلوريد الفوسفور هي PCl3.
س: هل ثلاثي كلوريد الفوسفور أيوني أم تساهمي؟
ج: ثلاثي كلوروفوسفين مركب تساهمي.
س: ما عدد ذرات الكلور الموجودة في جزيء ثلاثي كلوريد الفوسفور PCl3؟
ج: هناك ثلاث ذرات كلور في جزيء ثلاثي كلوروفوسفين.
س: تركيب لويس لثلاثي كلوروفوسفين؟
ج: يحتوي تركيب لويس لثلاثي كلوروفوسفين على ذرة فوسفور مركزية مرتبطة بثلاث ذرات كلور، مع وجود أزواج وحيدة على ذرة الفوسفور.
س: الفوسفور (P4) (ق) + الكلور (ز) → ثلاثي كلوروفوسفين (ل)؟
ج: تمثل المعادلة المتوازنة التفاعل بين الفوسفور الصلب (P4) وغاز الكلور (Cl2) لتكوين PCl3 السائل.
س: ما هو شكل ثلاثي كلوريد الفوسفور؟
ج: ثلاثي كلوروفوسفين له شكل هرمي ثلاثي بسبب وجود زوج من الإلكترونات الحرة على ذرة الفسفور.
س: هل ثلاثي كلوريد الفوسفور مركب أيوني؟
ج: لا، ثلاثي كلوروفوسفين ليس مركبًا أيونيًا؛ وهو مركب تساهمي.
س: هل يحتوي ثلاثي كلوريد الفوسفور على مستويات انعكاس؟
ج: لا، لا يحتوي ثلاثي كلوروفوسفين على مستويات انعكاس.
