خماسي كلوريد الفوسفور مركب كيميائي له الصيغة PCl5. يتم استخدامه ككاشف في التفاعلات الكيميائية المختلفة. يتفاعل بقوة مع الماء، ويطلق غاز كلوريد الهيدروجين.
| اسم الأيوباك | خامس كلوريد الفوسفور |
| الصيغة الجزيئية | PCl5 |
| CAS رقم | 10026-13-8 |
| المرادفات | خماسي كلوروفوسفوران، كلوريد الفوسفور (V)، كلوريد الفوسفور، كلوريد الفوسفور (V) |
| إنتشي | InChI=1S/Cl5P/c1-6(2,3,4)5 |
خصائص خامس كلوريد الفوسفور
صيغة خماسي كلوريد الفوسفور
صيغة خماسي كلوريد الفوسفور هي PCl5. وتتكون من ذرة فسفور مرتبطة بخمس ذرات كلور. تمثل الصيغة نسبة الذرات في المركب.
خماسي كلوريد الفوسفور الكتلة المولية
يتم حساب الكتلة المولية لكلوريد الفوسفور (V) عن طريق إضافة الكتل الذرية لجميع العناصر المكونة له. يحتوي الفوسفور على كتلة مولية تبلغ حوالي 30.97 جرامًا لكل مول، ولكل ذرة كلور كتلة مولية تبلغ حوالي 35.45 جرامًا لكل مول. إضافتها تعطي كتلة مولية تبلغ حوالي 208.24 جرام لكل مول لكلوريد الفوسفور (V).
نقطة غليان خامس كلوريد الفوسفور
كلوريد الفوسفور (V) لديه نقطة غليان تبلغ حوالي 167.8 درجة مئوية. عند درجة الحرارة هذه، يخضع المركب لتحول طوري من السائل إلى الغاز. تتأثر نقطة الغليان بالقوى الجزيئية الموجودة في المركب.
نقطة انصهار خامس كلوريد الفوسفور
تبلغ نقطة انصهار كلوريد الفوسفور (V) حوالي -93.6 درجة مئوية. هذه هي درجة الحرارة التي يتحول عندها المركب من الحالة الصلبة إلى الحالة السائلة. تعتبر نقطة الانصهار خاصية مهمة في تحديد السلوك الفيزيائي للمركب.
كثافة خماسي كلوريد الفوسفور جم/مل
تبلغ كثافة كلوريد الفوسفور (V) حوالي 2.1 جرام لكل ملليلتر. تمثل الكثافة كتلة المادة لكل وحدة حجم. تساعد كثافة كلوريد الفوسفور (V) على فهم ترتيبه وضغط جزيئاته.
الوزن الجزيئي لخماسي كلوريد الفوسفور
يبلغ الوزن الجزيئي لكلوريد الفوسفور (V) حوالي 208.24 جرامًا لكل مول. وهو مجموع الأوزان الذرية لجميع الذرات الموجودة في المركب. الوزن الجزيئي مفيد في العديد من الحسابات، مثل تحديد كمية المادة في كتلة أو حجم معين.
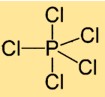
هيكل خامس كلوريد الفوسفور
يحتوي كلوريد الفوسفور (V) على بنية جزيئية تكون فيها ذرة فوسفور واحدة محاطة بخمس ذرات كلور. يتم ترتيب ذرات الكلور بشكل متناظر حول ذرة الفسفور المركزية، لتشكل هندسة هرمية ثنائية مثلثية.
ذوبان خامس كلوريد الفوسفور
كلوريد الفوسفور (V) قليل الذوبان في الماء. يتفاعل بقوة مع الماء، ويطلق غاز كلوريد الهيدروجين. ومع ذلك، فإنه يذوب بسهولة في المذيبات القطبية مثل البنزين ورابع كلوريد الكربون. تتأثر ذوبان كلوريد الفوسفور (V) بالقطبية والخواص الكيميائية للمذيب.
| مظهر | بلورات عديمة اللون |
| جاذبية معينة | 2.1 جرام/مل |
| لون | عديم اللون |
| يشم | فدان |
| الكتلة المولية | 208.24 جم/مول |
| كثافة | 2.1 جرام/مل |
| نقطة الانصهار | -93.6 درجة مئوية |
| نقطة الغليان | 167.8 درجة مئوية |
| نقطة فلاش | غير قابل للتطبيق |
| الذوبان في الماء | يتفاعل بقوة |
| الذوبان | قابل للذوبان في المذيبات القطبية مثل البنزين ورابع كلوريد الكربون |
| ضغط البخار | غير متاح |
| كثافة بخار | غير متاح |
| pKa | غير متاح |
| الرقم الهيدروجيني | غير قابل للتطبيق |
السلامة ومخاطر خامس كلوريد الفوسفور
يشكل كلوريد الفوسفور (V) العديد من المخاطر المتعلقة بالسلامة. وهو مادة أكالة ويمكن أن يسبب حروقًا شديدة في الجلد والعينين والجهاز التنفسي عند ملامسته. استنشاق أبخرتها أو غبارها قد يسبب تهيجاً وتلفاً في الجهاز التنفسي. يتفاعل المركب بعنف مع الماء، ويطلق غاز كلوريد الهيدروجين السام. كما أنه شديد التفاعل مع المواد العضوية، مما قد يسبب حرائق أو انفجارات. وينبغي اتخاذ الاحتياطات المناسبة عند التعامل مع كلوريد الفوسفور (V)، بما في ذلك استخدام معدات الحماية مثل القفازات والنظارات الواقية وجهاز التنفس. وينبغي تخزينها والتعامل معها في منطقة جيدة التهوية، بعيدا عن المواد غير المتوافقة، لمنع وقوع الحوادث وتقليل المخاطر.
| رموز الخطر | تآكل |
| وصف الأمان | التعامل مع الودائع. استخدم معدات الحماية المناسبة. |
| أرقام تعريف الأمم المتحدة | UN1806 |
| رمز النظام المنسق | 2812.20.00 |
| فئة الخطر | 8 (المواد المسببة للتآكل) |
| مجموعة التعبئة | الثاني (خطر معتدل) |
| تسمم | سامة عن طريق الابتلاع أو الاستنشاق. قد يسبب تهيجا خطيرا. |
طرق تصنيع خماسي كلوريد الفوسفور
تسمح الطرق المختلفة بتخليق كلوريد الفوسفور (V). تتضمن الطريقة الشائعة التفاعل بين ثلاثي كلوريد الفوسفور (PCl3) وغاز الكلور (Cl2) . في هذه العملية، يجمع وعاء التفاعل بين كل من المركبات والحرارة أو يبدأ التفاعل بمحفز مثل الحديد. يعمل غاز الكلور كعامل مؤكسد، حيث يحول PCl3 إلى PCl5. يستمر التفاعل على النحو التالي:
PCl3 + Cl2 → PCl5
هناك طريقة أخرى لتصنيع كلوريد الفوسفور (V) تتضمن التفاعل بين الفوسفور وغاز الكلور . هذه الطريقة أكثر مباشرة وتتضمن التفاعل التالي:
P4 + 10Cl2 → 4PCl5
في هذا التفاعل، يتفاعل غاز الفوسفور والكلور تحت ظروف مناسبة، مما يؤدي إلى تكوين كلوريد الفوسفور (V).
من المهم ملاحظة أن كلا الطريقتين التوليفيتين تتطلب معالجة دقيقة واحتياطات السلامة المناسبة. تشتمل التفاعلات على مواد شديدة التفاعل ومسببة للتآكل، لذا من الضروري توفير معدات الحماية والتهوية الكافية. بالإضافة إلى ذلك، من الضروري إجراء هذه التفاعلات في بيئة خاضعة للرقابة لمنع وقوع الحوادث وضمان سلامة الموظفين المعنيين.
استخدامات خامس كلوريد الفوسفور
يجد كلوريد الفوسفور (V) تطبيقات مختلفة نظرًا لخصائصه الفريدة وتفاعله. وهذه بعض استخداماته:
- التخليق الكيميائي: يستخدم التخليق العضوي كلوريد الفوسفور (V) على نطاق واسع ككاشف لتحويل الأحماض الكربوكسيلية إلى كلوريدات حمضية والكحولات إلى كلوريدات الألكيل.
- المستحضرات الصيدلانية: يعتمد تصنيع المركبات الصيدلانية، بما في ذلك المضادات الحيوية والأصباغ، بشكل كبير على كلوريد الفوسفور (V) كوسيط رئيسي.
- المحفز: يحفز كلوريد الفوسفور (V) العديد من التفاعلات الكيميائية، مثل أسيلة فريدل-كرافت وإعادة ترتيب بيكمان.
- صناعة البوليمرات: يستخدم إنتاج البوليمرات المختلفة، بما في ذلك كلوريد البولي فينيل (PVC) والبولي كربونات، كلوريد الفوسفور (V) كعامل كلورة.
- التطبيقات المخبرية: في التطبيقات المخبرية، يعمل كلوريد الفوسفور (V) كعامل تجفيف لإزالة آثار الماء من أجهزة المختبر وكعامل معالجة بالكلور وتجفيف في التفاعلات المختلفة.
- مبيدات الأعشاب والمبيدات الحشرية: إنتاج مبيدات الأعشاب والمبيدات الحشرية للسيطرة على نمو الأعشاب الضارة والقضاء على الآفات ينطوي على استخدام كلوريد الفوسفور (V).
- عوامل الحرب الكيميائية: تاريخياً، ساهم كلوريد الفوسفور (V) بشكل فعال في إنتاج عوامل الحرب الكيميائية، لكن استخدامه لمثل هذه الأغراض يخضع الآن لأنظمة وقيود صارمة.
- معالجة الأسطح المعدنية: تستخدم عمليات معالجة الأسطح المعدنية كلوريد الفوسفور (V) لتحسين خصائص الالتصاق وتعزيز مقاومة التآكل.
- مثبطات اللهب: يتضمن إنتاج إضافات مثبطات اللهب للمنسوجات والبلاستيك والمواد الأخرى كلوريد الفوسفور (V).
- تصنيع الأدوية: يستخدم كلوريد الفوسفور (V) في إنتاج العديد من المنتجات الصيدلانية، بما في ذلك تركيب الفيتامينات ومشتقات الهرمونات.
من المهم التعامل مع كلوريد الفوسفور (V) بعناية واتباع بروتوكولات السلامة المناسبة بسبب طبيعته المسببة للتآكل والمخاطر الصحية المحتملة.
أسئلة:
س: ما هي الصيغة الصحيحة لخماسي كلوريد الفوسفور؟
ج: الصيغة الصحيحة لكلوريد الفوسفور (V) هي PCl5.
س: ما هي الصيغة الجزيئية لخماسي كلوريد الفوسفور؟
ج: الصيغة الجزيئية لكلوريد الفوسفور (V) هي PCl5.
س: ما كتلة خماسي كلوريد الفوسفور التي ستنتج عن التفاعل الكامل لـ 15.2 جم من P4؟
ج: إن كتلة كلوريد الفوسفور (V) الناتج ستكون حوالي 208.24 جم.
س: ما هو شكل خماسي كلوريد الفسفور؟
ج: شكل كلوريد الفوسفور (V) هو هرمي ثنائي مثلثي.
س: ما كتلة جزيء خامس كلوريد الفوسفور؟
ج: تبلغ كتلة جزيء كلوريد الفسفور (V) حوالي 208.24 جرامًا لكل مول.
س: خواص خامس كلوريد الفوسفور؟
ج: كلوريد الفوسفور (V) مادة أكالة، ويتفاعل بعنف مع الماء، ويستخدم ككاشف في التركيب الكيميائي.
س: زوايا الرابطة لكلوريد الفوسفور (V)؟
ج: تبلغ زوايا الرابطة في خماسي كلوريد الفوسفور حوالي 120 درجة (بين ذرات الكلور الاستوائية) و90 درجة (بين ذرات الكلور المحورية).
س: كيف يتم تحضير خماسي كلوريد الفسفور؟
ج: يمكن تصنيع كلوريد الفوسفور (V) عن طريق تفاعل ثلاثي كلوريد الفوسفور (PCl3) مع غاز الكلور (Cl2) أو عن طريق التفاعل المباشر بين الفوسفور وغاز الكلور.
س: ما هي الهندسة الإلكترونية للفسفور في خامس كلوريد الفسفور؟
ج: الهندسة الإلكترونية للفوسفور في كلوريد الفوسفور (V) هي هرمية ثلاثية الزوايا.
