1- البيوتانول (C4H9OH) هو كحول عديم اللون ذو رائحة حلوة قليلاً. يتم استخدامه كمذيب، في التخليق العضوي وكمصدر للوقود. ويمكن استخدامه أيضًا في مستحضرات التجميل ومنتجات العناية الشخصية.
| اسم الأيوباك | بوتان-1-رأ |
| الصيغة الجزيئية | C4H10O |
| CAS رقم | 71-36-3 |
| المرادفات | ن-كحول بوتيل، بيوتانول، كحول بوتيل، 1-كحول بوتيل، 1-بيوتانول، بيوتانولين، هيدرات بوتيلين، هيدرات بوتيل |
| إنتشي | إنتشي = 1S/C4H10O/c1-2-3-4-5/h5H،2-4H2،1H3 |
خصائص 1-بيوتانول
الصيغة 1-البيوتانول
الصيغة الجزيئية لل1-بيوتانول هي C4H10O. وهذا يعني أنه يحتوي على أربع ذرات كربون وعشر ذرات هيدروجين وذرة أكسجين واحدة. وله هيكل خطي، مع مجموعة الهيدروكسيل (-OH) المرتبطة بذرة الكربون الأولى.
1-الكتلة المولية للبيوتانول
الكتلة المولية لـ C4H9OH هي 74.12 جم/مول. وهذا يعني أن المول الواحد من C4H9OH يزن 74.12 جرامًا. تعد الكتلة المولية خاصية مهمة للمادة لأنها تساعد في تحديد كمية المادة الموجودة في عينة معينة.
نقطة غليان 1-بيوتانول
C4H9OH لديه نقطة غليان تبلغ 117.7 درجة مئوية (243.9 درجة فهرنهايت). وهذا يعني أنه سيتحول من السائل إلى الغاز عند درجة الحرارة هذه. درجة غليان C4H9OH أعلى من درجة غليان الإيثانول بسبب وجود ذرة كربون إضافية.
1- نقطة انصهار البيوتانول
نقطة انصهار C4H9OH هي -90.6 درجة مئوية (-131.1 درجة فهرنهايت). وهذا يعني أنه سيتحول من الحالة الصلبة إلى الحالة السائلة عند درجة الحرارة هذه. درجة انصهار C4H9OH أقل من درجة انصهار حمض البيوتانويك، الذي له وزن جزيئي مماثل.
1-كثافة البوتانول جم/مل
تبلغ كثافة C4H9OH 0.81 جم / مل. وهذا يعني أن الملليلتر الواحد من C4H9OH يزن 0.81 جرام. كثافة C4H9OH أقل من كثافة الماء الذي تبلغ كثافته 1 جم/مل.
1- الوزن الجزيئي للبيوتانول
الوزن الجزيئي لـ C4H9OH هو 74.12 جم / مول. وهو مجموع الأوزان الذرية لجميع الذرات الموجودة في صيغته الجزيئية. يعد الوزن الجزيئي خاصية مهمة لأي مادة لأنه يساعد في تحديد خواصها الفيزيائية والكيميائية.
هيكل 1-بيوتانول
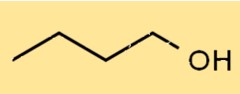
هيكل C4H9OH عبارة عن كحول ذو سلسلة مستقيمة، مع مجموعة الهيدروكسيل (-OH) المرتبطة بذرة الكربون الأولى. وله هيكل خطي، مع أربع ذرات كربون وعشر ذرات هيدروجين وذرة أكسجين واحدة. هيكلها يسمح لها بتكوين روابط هيدروجينية مع جزيئات أخرى.
ذوبان 1-بيوتانول
C4H9OH قابل للذوبان في الماء والمذيبات العضوية. وتقل ذوبانه في الماء مع زيادة درجة الحرارة. كما أنه قابل للذوبان في المذيبات القطبية، مثل الإيثانول والميثانول. قابلية ذوبان C4H9OH في المذيبات العضوية، مثل البنزين والإيثر، أعلى منها في الماء. وهذا يجعله مفيدًا كمذيب في التركيب العضوي.
| مظهر | سائل عديم اللون |
| جاذبية معينة | 0.810 جم/مل عند 25 درجة مئوية |
| لون | عديم اللون |
| يشم | حلو قليلا |
| الكتلة المولية | 74.12 جرام/مول |
| كثافة | 0.81 جرام/مل |
| نقطة الانصهار | -90.6 درجة مئوية (-131.1 درجة فهرنهايت) |
| نقطة الغليان | 117.7 درجة مئوية (243.9 درجة فهرنهايت) |
| نقطة فلاش | 35 درجة مئوية (95 درجة فهرنهايت) |
| الذوبان في الماء | 79 جم/لتر عند 20 درجة مئوية |
| الذوبان | قابل للذوبان في الإيثانول، ثنائي إيثيل الأثير، الأسيتون، البنزين، الكلوروفورم |
| ضغط البخار | 1.16 كيلو باسكال عند 20 درجة مئوية |
| كثافة بخار | 2.55 (بالنسبة للهواء) |
| pKa | 16.06 |
| الرقم الهيدروجيني | محايد (7) |
1-سلامة ومخاطر البيوتانول
يشكل C4H9OH العديد من المخاطر المتعلقة بالسلامة، مما يجعل من الضروري التعامل معه بعناية. وهو سائل قابل للاشتعال ويمكن أن يشتعل بسهولة عند تعرضه للحرارة أو الشرر. كما أنها تنبعث منها أبخرة ضارة يمكن أن تسبب تهيجًا وتلفًا للعينين والجهاز التنفسي والجلد. عند تناوله، يمكن أن يسبب مشاكل صحية خطيرة، بما في ذلك الدوخة، والارتباك، وحتى الغيبوبة. لذلك من الضروري ارتداء معدات الحماية مثل القفازات والنظارات الواقية وأجهزة التنفس عند التعامل مع C4H9OH. في حالة ملامسته للجلد أو العينين، يجب شطفه بالماء واستشارة الطبيب على الفور. يعد التخزين والتعامل والتخلص من C4H9OH بشكل صحيح أمرًا ضروريًا لمنع وقوع الحوادث وضمان السلامة.
| رموز الخطر | ف، شي |
| وصف الأمان | يُحفظ بعيدًا عن الحرارة/الشرر/اللهب المكشوف/الأسطح الساخنة. ارتداء القفازات الواقية / حماية العين / حماية الوجه. إذا كان على الجلد (أو الشعر): قم بإزالة جميع الملابس الملوثة على الفور. شطف الجلد بالماء/الدش. إذا كان في العينين: اشطفيه بحذر بالماء لعدة دقائق. إزالة العدسات اللاصقة، إذا كانت موجودة وسهلة للقيام. استمر في الشطف. يُخزن في مكان بارد وجاف وجيد التهوية بعيدًا عن المواد غير المتوافقة. |
| أرقام تعريف الأمم المتحدة | الأمم المتحدة 1120 |
| رمز النظام المنسق | 2905.16.00 |
| فئة الخطر | 3 |
| مجموعة التعبئة | ثالثا |
| تسمم | الجرعة المميتة 50 (عن طريق الفم، للفئران) 2.46 جم/كجم؛ LC50 (استنشاق، فأر) 37800 جزء في المليون/4 ساعات |
طرق تصنيع 1-بيوتانول
يمكن تصنيع C4H9OH بعدة طرق، بما في ذلك اختزال البوتيرالدهيد، أو معالجة الأكسو، أو التخمير.
التخمير هو طريقة شائعة لإنتاج C4H9OH من الكتلة الحيوية. في عملية التخمير، تكون الكائنات الحية الدقيقة مثل Clostridium acetobutylicum مسؤولة عن إنتاج خليط من الأحماض العضوية والكحوليات، بما في ذلك C4H9OH، عن طريق تخمير السكريات أو النشويات أو السليلوز.
تتضمن عملية الأكسو، المعروفة أيضًا باسم الفورميل الهيدروجيني، تفاعل البروبين مع أول أكسيد الكربون والهيدروجين في وجود محفز مثل الكوبالت أو الروديوم. هدرجة البوتيرالدهيد تنتج C4H9OH. عندما يخضع البيوتيرالدهيد للهدرجة، فإنه يشكل المركب C4H9OH.
هناك طريقة أخرى لتصنيع C4H9OH تتضمن اختزال البوتيرالدهيد بالهيدروجين في وجود محفز مثل البلاديوم أو النيكل. ينتج عن هذا التفاعل C4H9OH مع الماء كمنتج ثانوي.
عملية فيشر تروبش هي طريقة لإنتاج C4H9OH من الوقود الأحفوري. يتضمن ذلك استخدام محفز لتسبب تفاعل أول أكسيد الكربون والهيدروجين، مما يؤدي إلى إنتاج هيدروكربونات مختلفة، بما في ذلك C4H9OH.
استخدامات 1-بيوتانول
C4H9OH له العديد من الاستخدامات في مختلف الصناعات بسبب خصائصه الفريدة. بعض الاستخدامات الشائعة لـ C4H9OH تشمل:
- المذيب: يستخدم كمذيب لمختلف المواد، بما في ذلك الراتنجات والدهون والزيوت والشموع.
- وسيط: يستخدم كوسيط في إنتاج مواد كيميائية أخرى، مثل بوتيل أكريلات وخلات البوتيل.
- المادة المضافة: تستخدم كمادة مضافة في وقود البنزين والديزل لزيادة معدل الأوكتان وتقليل الانبعاثات.
- المستخلص: يستخدم كمستخلص في إنتاج المضادات الحيوية والفيتامينات والهرمونات.
- منتجات التجميل والعناية الشخصية: تستخدم في إنتاج مستحضرات التجميل والعناية الشخصية المختلفة، بما في ذلك المستحضرات والكريمات والعطور.
- النكهات والعطور: يستخدم كمحسن للنكهة والعطور في صناعة الأغذية والمشروبات.
- المستحضرات الصيدلانية: تستخدم في إنتاج المستحضرات الصيدلانية المختلفة، بما في ذلك المهدئات والمنومات.
- المبيدات الحشرية: تستخدم كمكون في إنتاج المبيدات الحشرية ومبيدات الأعشاب المختلفة.
أسئلة:
س: هل البوتانول قطبي؟
ج: نعم، البيوتانول قطبي بسبب وجود مجموعة الهيدروكسيل (-OH) التي تعطيه عزم ثنائي القطب.
س: هل 1- بيوتانول قابل للذوبان في الماء؟
ج: نعم، C4H9OH قابل للذوبان جزئيًا في الماء بسبب وجود مجموعة الهيدروكسيل التي تسمح له بتكوين روابط هيدروجينية مع جزيئات الماء.
س: هل يحتوي 1-بيوتانول على رابطة هيدروجينية؟
ج: نعم، يحتوي C4H9OH على رابطة هيدروجينية بسبب وجود مجموعة الهيدروكسيل (-OH) والتي يمكن أن تشكل روابط هيدروجينية مع جزيئات C4H9OH الأخرى أو مع جزيئات الماء.
س: ما عدد مل من 1- بيوتانول اللازم لتحضير 725 مل من محلول مائي تركيزه 0.350 م من هذا المذاب؟
ج: يتطلب الحساب الكتلة المولية لـ C4H9OH، وهي 74.12 جم/مول. لتحضير محلول 0.350 M من C4H9OH، يلزم 26.12 جم من C4H9OH. باستخدام الصيغة: المولات = التركيز × الحجم، يمكننا حساب حجم C4H9OH المطلوب كما يلي: الحجم = المولات / التركيز. وبالتالي، فإن حجم C4H9OH اللازم لتحضير 725 مل من محلول 0.350 م هو (26.12/0.350) = 74.6 مل.
س: ما هو الكحول الذي يتصرف مثل الماء؟ c2h5oh c4h9oh c10h21oh c7h15oh
ج: من بين الخيارات المقدمة، يتصرف الإيثانول (C2H5OH) مثل الماء نظرًا لصغر حجمه الجزيئي ووجود مجموعة الهيدروكسيل (-OH)، مما يسمح له بتكوين روابط هيدروجينية قوية مع جزيئات الماء.
س: ما نواتج المعادلة الموزونة لاحتراق c4h9oh؟
ج: المعادلة المتوازنة لاحتراق C4H9OH هي: C4H9OH + 6O2 → 4CO2 + 5H2O. منتجات التفاعل هي ثاني أكسيد الكربون (CO2) والماء (H2O).
س: ما هي الكتلة المولية للبيوتانول (c4h9oh)؟
ج: الكتلة المولية للبيوتانول (C4H9OH) هي 74.12 جم/مول.
س: هل يحتوي C4h9oh على رابطة هيدروجينية؟
ج: نعم، يحتوي C4H9OH على رابطة هيدروجينية بسبب وجود مجموعة الهيدروكسيل (-OH) التي تسمح له بتكوين روابط هيدروجينية مع جزيئات C4H9OH الأخرى أو مع جزيئات الماء.
س: ما عدد جرامات كحول البوتيل (c4h9oh) الموجودة في محلول سعة 2500 مل، أو 2.22 م؟
ج: لحساب عدد جرامات كحول البوتيل في المحلول، نحتاج إلى استخدام الصيغة: المولات = التركيز × الحجم. تركيز المحلول هو 2.22 مول/لتر والحجم 2.5 لتر (2500 مل محول إلى لتر). إذن، عدد مولات كحول البوتيل في المحلول هو: 2.22 × 2.5 = 5.55 مول. لحساب كتلة كحول البوتيل، اضرب عدد الشامات في كتلته المولية (74.12 جم/مول): 5.55 × 74.12 = 411.4 جم. وبالتالي يوجد 411.4 جرامًا من كحول البوتيل في محلول سعة 2500 مل، أو 2.22 م.
