هيدريد ألومنيوم الليثيوم (LiAlH4) هو عامل اختزال قوي يستخدم في الكيمياء العضوية لتحويل مركبات الكربونيل إلى كحولات. يتفاعل بقوة مع الماء.
| اسم الأيوباك | هيدريد ألومنيوم الليثيوم |
| الصيغة الجزيئية | LiAlH4 |
| CAS رقم | 16853-85-3 |
| المرادفات | رباعي هيدرو ألومينات الليثيوم (III)، هيدريد ألومنيوم الليثيوم (III). |
| إنتشي | InChI=1S/Al.Li.4H |
خواص هيدريد ألومنيوم الليثيوم (LiAlH4)
صيغة هيدريد ألومنيوم الليثيوم (LiAlH4).
تمثل صيغة رباعي هيدرو ألومينات الليثيوم (LiAlH4) تركيبته. ويتكون من ذرة ليثيوم واحدة (Li) وذرة ألومنيوم واحدة (Al) وأربع ذرات هيدروجين (H). الصيغة مكتوبة LiAlH4، مما يدل على وجود هذه العناصر.
هيدريد ألومنيوم الليثيوم (LiAlH4) الكتلة المولية
الكتلة المولية لرباعي هيدرو ألومينات الليثيوم (LiAlH4) هي مجموع الكتل الذرية للعناصر المكونة له. يتم حسابه على النحو التالي:
- يحتوي الليثيوم (Li) على كتلة مولية تبلغ حوالي 6.94 جم / مول.
- الألومنيوم (آل) لديه كتلة مولية تبلغ حوالي 26.98 جم / مول.
- يحتوي الهيدروجين (H) على كتلة مولية تبلغ حوالي 1.01 جم/مول.
وبجمع هذه القيم معًا، تبلغ الكتلة المولية لـ LiAlH4 حوالي 37.95 جم/مول.
هيدريد ألومنيوم الليثيوم (LiAlH4) نقطة الغليان
ليس لدى رباعي هيدرو ألومينات الليثيوم (LiAlH4) نقطة غليان مميزة لأنه يتحلل قبل الوصول إلى نقطة غليان أي من مكوناته الفردية. عند التسخين، يخضع LiAlH4 لتفاعل تحلل، مما يؤدي إلى إطلاق غاز الهيدروجين.
هيدريد ألومنيوم الليثيوم (LiAlH4) نقطة الانصهار
يحتوي رباعي هيدرو ألومينات الليثيوم (LiAlH4) على نقطة انصهار منخفضة نسبيًا. يذوب عند حوالي 150-160 درجة مئوية (302-320 درجة فهرنهايت). عند درجة الحرارة هذه، يتحول LiAlH4 الصلب إلى حالة سائلة، مما يسمح له بالمشاركة في التفاعلات الكيميائية.
هيدريد ألومنيوم الليثيوم (LiAlH4) الكثافة جم/مل
تبلغ كثافة رباعي هيدرو ألومينات الليثيوم (LiAlH4) حوالي 0.917 جم/مل. تشير قيمة الكثافة هذه إلى كتلة LiAlH4 الموجودة في حجم معين، بوحدة الجرام لكل ملليلتر.
هيدريد ألومنيوم الليثيوم (LiAlH4) الوزن الجزيئي
يتم حساب الوزن الجزيئي لرباعي هيدرو ألومينات الليثيوم (LiAlH4) عن طريق إضافة الأوزان الذرية لجميع العناصر المكونة له. يبلغ الوزن الجزيئي لـ LiAlH4 حوالي 37.95 جم/مول.
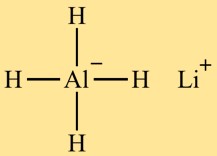
هيكل هيدريد ألومنيوم الليثيوم (LiAlH4)
يحتوي رباعي هيدرو ألومينات الليثيوم (LiAlH4) على هيكل رباعي السطوح. توجد ذرة الألومنيوم في المنتصف، وتحيط بها أربع ذرات هيدروجين. وتتصل ذرة الليثيوم أيضًا بذرة الألومنيوم، لتكتمل البنية.
ذوبان هيدريد ألومنيوم الليثيوم (LiAlH4)
رباعي هيدرو ألومينات الليثيوم (LiAlH4) غير قابل للذوبان في معظم المذيبات العضوية مثل الإيثرات والهيدروكربونات. ومع ذلك، فهو شديد التفاعل مع الماء، ويخضع لتفاعل طارد للحرارة قوي وينتج غاز الهيدروجين. لذلك، تتم معالجة LiAlH4 بشكل عام وتخزينه تحت ظروف لا مائي لتجنب أي تفاعل سلبي مع الرطوبة.
| مظهر | بودرة بيضاء |
| جاذبية معينة | 0.917 جم/مل |
| لون | عديم اللون |
| يشم | عديم الرائحة |
| الكتلة المولية | 37.95 جرام/مول |
| كثافة | 0.917 جم/مل |
| نقطة الانصهار | 150-160 درجة مئوية |
| نقطة الغليان | متحللة |
| نقطة فلاش | غير قابل للتطبيق |
| الذوبان في الماء | يتفاعل بقوة مع الماء |
| الذوبان | غير قابل للذوبان في المذيبات العضوية مثل الإيثرات والهيدروكربونات |
| ضغط البخار | غير قابل للتطبيق |
| كثافة بخار | غير قابل للتطبيق |
| pKa | غير قابل للتطبيق |
| الرقم الهيدروجيني | غير قابل للتطبيق |
سلامة ومخاطر هيدريد ألومنيوم الليثيوم (LiAlH4).
يشكل رباعي هيدرو ألومينات الليثيوم (LiAlH4) مخاطر كبيرة على السلامة ويجب التعامل معه بحذر شديد. وهو مركب شديد التفاعل يتفاعل بعنف مع الماء، ويطلق غاز الهيدروجين القابل للاشتعال. LiAlH4 قابل للاشتعال، مما يعني أنه يمكن أن يشتعل تلقائيًا في الهواء. يجب أن يتم تخزينه بعيدا عن الرطوبة وتخزينه في حاويات مغلقة بإحكام. يمكن أن يسبب الاتصال المباشر بـ LiAlH4 حروقًا شديدة وتهيجًا في الجلد والعينين والجهاز التنفسي. استنشاق غبارها أو أبخرتها قد يسبب ضيقاً في التنفس. يجب ارتداء معدات الحماية الشخصية المناسبة، مثل القفازات والنظارات الواقية، عند العمل مع LiAlH4، ويجب التعامل معها فقط في مناطق جيدة التهوية مع تطبيق تدابير السلامة المناسبة.
| رموز الخطر | ف، ج |
| وصف الأمان | شديدة الاشتعال. يتفاعل بعنف مع الماء. تعامل بحذر شديد. |
| أرقام تعريف الأمم المتحدة | الأمم المتحدة 1410 |
| رمز النظام المنسق | 2850.00.00 |
| فئة الخطر | 4.3 |
| مجموعة التعبئة | أنا |
| تسمم | سامة جدًا، ويمكن أن تسبب حروقًا شديدة وضيقًا في التنفس. |
ملحوظة: رموز الخطر المستخدمة هي “F” للمواد القابلة للاشتعال و”C” للمواد المسببة للتآكل. يسلط وصف السلامة الضوء على التفاعل مع الماء ويؤكد على ضرورة توخي الحذر الشديد. معرفات الأمم المتحدة ورمز النظام المنسق هي رموز تعريف محددة تستخدم لأغراض النقل والتجارة. تشير فئة الخطر إلى تصنيف المادة بناءً على خصائصها. تمثل مجموعة التعبئة مستوى الخطر أثناء النقل. يعتبر رباعي هيدرو ألومينات الليثيوم (LiAlH4) شديد السمية ويمكن أن يسبب حروقًا شديدة وضيقًا في التنفس عن طريق التلامس أو الاستنشاق.
طرق تصنيع هيدريد ألومنيوم الليثيوم (LiAlH4)
تسمح الطرق المختلفة بتخليق رباعي هيدرو ألومينات الليثيوم (LiAlH4).
إحدى الطرق الشائعة لتصنيع رباعي هيدرو ألومينات الليثيوم (LiAlH4) هي تسخين AlCl3 ودمجه مع هيدريد الليثيوم (LiH) في مذيب مثل ثنائي إيثيل إيثر . ويحدث التفاعل في وجود الحرارة، مما يؤدي إلى تكوين LiAlH4.
هناك طريقة أخرى وهي خلط مسحوق معدن الألومنيوم مع هيدريد الليثيوم ثم تسخين الخليط. يحدث التفاعل مما يؤدي إلى تكوين LiAlH4.
لتجميع LiAlH4 باستخدام نهج مختلف، الجمع بين ديوتريد ألومنيوم الليثيوم (LiAlD4) مع LiH في مذيب مثل رباعي هيدروفوران (THF) . قم بتسخين الخليط، مما يسبب تفاعلًا بين LiAlD4 وهيدريد الليثيوم، مما يؤدي إلى تكوين LiAlH4.
تجدر الإشارة إلى أن هذه الأساليب الاصطناعية تتطلب معالجة دقيقة بسبب تفاعل المركبات المعنية. تعتبر الاحتياطات مثل العمل في ظروف خاملة، واستخدام معدات السلامة المناسبة، وإجراء التفاعلات في مناطق جيدة التهوية ضرورية لضمان التوليف الآمن والناجح.
استخدامات هيدريد ألومنيوم الليثيوم (LiAlH4)
يحتوي رباعي هيدرو ألومينات الليثيوم (LiAlH4) على العديد من التطبيقات في الكيمياء العضوية نظرًا لخصائصه الاختزالية القوية. فيما يلي بعض الاستخدامات الشائعة:
- اختزال مركبات الكربونيل: يقوم LiAlH4 بتحويل مركبات الكربونيل المختلفة بشكل ملحوظ، مثل الألدهيدات والكيتونات والإسترات والأحماض الكربوكسيلية، إلى كحولات مقابلة لها. يعد تفاعل الاختزال هذا أمرًا بالغ الأهمية في تركيب المستحضرات الصيدلانية والمواد الكيميائية الدقيقة والوسائط العضوية.
- اختزال مركبات النيترو: يمكن لـ LiAlH4 اختزال مركبات النيترو إلى الأمينات الأولية. يعتبر هذا التحول ذا قيمة في تركيب مجموعة واسعة من المركبات العضوية، بما في ذلك المستحضرات الصيدلانية والأصباغ والكيماويات الزراعية.
- إزالة الأكسجين: يمكن لـ LiAlH4 إزالة ذرات الأكسجين بشكل انتقائي من مجموعات وظيفية مختلفة، مثل الكحوليات والأحماض والأكسيمات. تعتبر عملية إزالة الأكسجين هذه مفيدة في تحضير المركبات الحساسة للأكسجين أو عندما يلزم إزالة وظيفة الأكسجين.
- تفاعلات البلمرة: يعمل LiAlH4 كعامل اختزال في بعض تفاعلات البلمرة، مما يسهل تكوين البوليمرات. يستخدم الباحثون LiAlH4 في إنتاج مواد عالية الأداء، بما في ذلك البوليمرات الموصلة والمواد البلاستيكية المتخصصة.
- التطبيقات الاصطناعية: يستخدم LiAlH4 في تخليق المركبات العضوية المختلفة، بما في ذلك الهيدرازين والفوسفينات والمركبات المعدنية العضوية. هذه المركبات ضرورية في البحوث الصيدلانية والحفز الكيميائي وعلوم المواد.
- عامل الاختزال في المختبر: يعمل LiAlH4 كعامل اختزال متعدد الاستخدامات في المختبر. فهو يسمح للكيميائيين بتقليل مجموعات وظيفية محددة بشكل انتقائي، وبالتالي تمكين تركيب جزيئات معقدة بدقة عالية.
بشكل عام، يلعب رباعي هيدرو ألومينات الليثيوم (LiAlH4) دورًا حاسمًا في التخليق العضوي، حيث يوفر للكيميائيين أداة قوية لتفاعلات الاختزال المختلفة ويتيح إعداد مجموعة واسعة من المركبات القيمة.
أسئلة:
س: هل يقلل هيدريد ألومنيوم الليثيوم من الروابط المزدوجة؟
ج: نعم، يمكن لرباعي هيدرو ألومينات الليثيوم أن يقلل الروابط المزدوجة ويحولها إلى روابط مفردة.
س: ما هو الغاز الذي يطلقه هيدريد ألومنيوم الليثيوم عندما يتفاعل مع مذيب بروتي؟
ج: عندما يتفاعل رباعي هيدرو ألومينات الليثيوم مع مذيب بروتي، فإنه يطلق غاز الهيدروجين.
س: أين يمكنني شراء هيدريد ألومنيوم الليثيوم؟
ج: يمكن شراء رباعي هيدرو ألومينات الليثيوم من موردي المواد الكيميائية أو موردي معدات المختبرات المتخصصة.
س: هل يعتمد على هيدريد ألومنيوم الليثيوم؟
ج: لا، لا يعتبر رباعي هيدرو ألومينات الليثيوم قاعدة بل عامل اختزال قوي.
س: ما الذي يقلله LiAlH4؟
ج: يمكن لرباعي هيدرو ألومينات الليثيوم أن يقلل من المجموعات الوظيفية المختلفة، بما في ذلك مركبات الكربونيل، ومجموعات النيترو، والكحوليات.
س: هل هيدريد ألومنيوم الليثيوم محب للنواة؟
ج: نعم، يعمل رباعي هيدرو ألومينات الليثيوم كمادة محبة للنواة في العديد من التفاعلات العضوية بسبب وجود أيون الهيدريد.
س: هل يقلل هيدريد ألومنيوم الليثيوم من الكحوليات؟
ج: نعم، يمكن لرباعي هيدرو ألومينات الليثيوم أن يقلل الكحولات لإنتاج كحولات أولية أو ثانوية.
س: هل هيدريد ألومنيوم الليثيوم يقلل الألكينات؟
ج: لا، رباعي هيدرو ألومينات الليثيوم لا يتفاعل بشكل عام مع الألكينات.
س: أي من المذيبات التالية لا يتفاعل معها هيدريد ألومنيوم الليثيوم؟
ج: لا يتفاعل رباعي هيدرو ألومينات الليثيوم عمومًا مع المذيبات غير القطبية مثل الهكسان أو ثنائي إيثيل إيثر.
س: هل يؤثر هيدريد ألومنيوم الليثيوم على الكحولات؟
ج: نعم، يمكن أن يقلل رباعي هيدرو ألومينات الليثيوم من الكحوليات، ولكن يجب استخدامه بحذر لأنه قد يكون شديد التفاعل وربما يكون خطيرًا.
