كبريتات الصوديوم مركب بلوري أبيض له الصيغة Na2SO4. يتم استخدامه في صناعات المنظفات وصناعة الورق وصناعة الزجاج كمواد حشو وعامل تجفيف ومزيل للرغوة.
| اسم الأيوباك | كبريتات الصوديوم |
| الصيغة الجزيئية | Na2SO4 |
| CAS رقم | 7757-82-6 |
| المرادفات | كبريتات الصوديوم، كبريتات الصوديوم اللامائية، كبريتات الصوديوم |
| إنتشي | InChI=1S/2Na.H2O4S/c;;1-5(2,3)4/h;;(H2,1,2,3,4)/q2*+1;/p-2 |
Na2So4 الكتلة المولية
تحتوي كبريتات الصوديوم على كتلة مولية تبلغ 142.04 جم/مول. وهو مركب أيوني يتكون من كاتيونين صوديوم (Na+) وأنيون كبريتات (SO42-). يتم حساب الكتلة المولية عن طريق إضافة الكتل الذرية لجميع الذرات الموجودة في جزيء كبريتات الصوديوم. في هذه الحالة، لدينا ذرتان صوديوم كتلة كل منهما 22.99 جم/مول، وذرة كبريت واحدة كتلتها 32.06 جم/مول وأربع ذرات أكسجين كتلة كل منها 15.99 جم/مول. وبجمعهما معًا نحصل على الكتلة المولية لكبريتات الصوديوم.
درجة غليان كبريتات الصوديوم
كبريتات الصوديوم لديها نقطة غليان عالية تبلغ 1429 درجة مئوية (2604 درجة فهرنهايت). ويرجع ذلك إلى الطبيعة الأيونية للمركب، والتي تخلق قوى جذب إلكتروستاتيكية قوية بين أيونات الصوديوم الموجبة وأيونات الكبريتات سالبة الشحنة. ويتطلب التغلب على هذه القوى كمية كبيرة من الطاقة، ولهذا السبب تكون درجة غليان كبريتات الصوديوم مرتفعة جدًا.
نقطة انصهار كبريتات الصوديوم
تختلف درجة انصهار كبريتات الصوديوم حسب محتواها المائي. كبريتات الصوديوم اللامائية (بدون ماء) لديها نقطة انصهار تبلغ 884 درجة مئوية (1623 درجة فهرنهايت). ومع ذلك، فإن ديكاهيدرات كبريتات الصوديوم (مع عشرة جزيئات ماء) تذوب عند درجة حرارة أقل تبلغ 32.4 درجة مئوية (90.3 درجة فهرنهايت). إن وجود جزيئات الماء في التركيب البلوري لديكاهيدرات كبريتات الصوديوم يضعف الروابط الأيونية بين أيونات الصوديوم والكبريتات، مما يقلل من درجة الانصهار.
كثافة كبريتات الصوديوم جم/مل
تختلف كثافة كبريتات الصوديوم حسب شكلها. تبلغ كثافة كبريتات الصوديوم اللامائية 2.664 جم / سم 3، بينما تبلغ كثافة ديكاهيدرات كبريتات الصوديوم 1.464 جم / سم 3. ويعود الاختلاف في الكثافة إلى وجود جزيئات الماء في التركيب البلوري للعشاري الماء مما يزيد حجمه ويقلل كثافته.
الوزن الجزيئي لكبريتات الصوديوم
الوزن الجزيئي لكبريتات الصوديوم هو 142.04 جم / مول. هذه هي كتلة جزيء كبريتات الصوديوم، الذي يتكون من أيونين صوديوم وأيون كبريتات واحد.
هيكل كبريتات الصوديوم
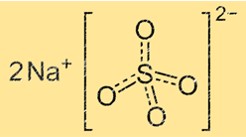
تحتوي كبريتات الصوديوم على بنية بلورية تتكون من وحدات متكررة من أيونات الصوديوم والكبريتات. أيون الكبريتات عبارة عن رباعي الأسطح يحتوي على أربع ذرات أكسجين في الزوايا وذرة كبريت واحدة في المركز. أيون الصوديوم عبارة عن كرة صغيرة تقع بين أيونات الكبريتات. يمكن أن يختلف التركيب البلوري لكبريتات الصوديوم اعتمادًا على محتواه المائي. كبريتات الصوديوم اللامائية لها بنية بلورية مختلفة عن ديكاهيدرات كبريتات الصوديوم.
صيغة كبريتات الصوديوم
الصيغة الكيميائية لكبريتات الصوديوم هي Na2SO4. وهذا يعني أن كل جزيء من كبريتات الصوديوم يحتوي على أيوني صوديوم (Na+) وأيون كبريتات واحد (SO42-). تمثل الصيغة أبسط نسبة صحيحة للذرات في جزيء المركب.
| مظهر | مادة صلبة بلورية بيضاء |
| جاذبية معينة | 2664 جم/سم3 (لا مائي)، 1464 جم/سم3 (ديكاهيدرات) |
| لون | أبيض |
| يشم | عديم الرائحة |
| الكتلة المولية | 142.04 جرام/مول |
| كثافة | 2664 جم/سم3 (لا مائي)، 1464 جم/سم3 (ديكاهيدرات) |
| نقطة الانصهار | 884 درجة مئوية (لا مائي)، 32.4 درجة مئوية (ديكاهيدرات) |
| نقطة الغليان | 1,429 درجة مئوية |
| نقطة فلاش | غير قابل للتطبيق |
| الذوبان في الماء | 44.1 جم/100 مل (لا مائي)، 47.6 جم/100 مل (ديكاهيدرات) |
| الذوبان | قابل للذوبان في الماء، غير قابل للذوبان في الإيثانول |
| ضغط البخار | 0.01 ملم زئبق عند 20 درجة مئوية |
| كثافة بخار | غير قابل للتطبيق |
| pKa | الأول: 2.01، الثاني: 7.20، الثالث: 9.41 |
| الرقم الهيدروجيني | 9-11 (محلول 10%) |
سلامة ومخاطر كبريتات الصوديوم
تعتبر كبريتات الصوديوم آمنة للاستخدام بشكل عام، ولكنها قد تسبب تهيجًا أو ضررًا في ظروف معينة. قد يهيج الجلد والعينين والجهاز التنفسي عن طريق الاتصال أو الاستنشاق. تناول كميات كبيرة قد يسبب الغثيان والقيء والإسهال. كما يمكن أن يكون ضارًا بالحياة المائية إذا تم إطلاقه في المجاري المائية. لا تعتبر كبريتات الصوديوم مادة قابلة للاشتعال أو الانفجار. ومع ذلك، عند تسخينها أو تعرضها لدرجات حرارة عالية، قد تنبعث أبخرة سامة. من المهم اتباع إجراءات التعامل الصحيحة، وارتداء معدات الحماية، وتخزين كبريتات الصوديوم في مكان آمن.
| رموز الخطر | لا أحد |
| وصف الأمان | S24/25: تجنب ملامسة الجلد والعينين. S36/37: ارتداء الملابس الواقية والقفازات المناسبة. |
| أرقام تعريف الأمم المتحدة | الأمم المتحدة 2118 |
| رمز النظام المنسق | 2833.11.00 |
| فئة الخطر | ليست خطيرة |
| مجموعة التعبئة | غير قابل للتطبيق |
| تسمم | الجرعة المميتة 50 (عن طريق الفم، للفئران): 5900 ملغم/كغم |
طرق تصنيع كبريتات الصوديوم
هناك طرق مختلفة لتصنيع كبريتات الصوديوم، بما في ذلك تفاعل كلوريد الصوديوم مع حمض الكبريتيك أو تفاعل هيدروكسيد الصوديوم مع حمض الكبريتيك.
لإنتاج كبريتات الصوديوم، فإن تفاعل كلوريد الصوديوم وحمض الكبريتيك يولد كبريتات الصوديوم وغاز كلوريد الهيدروجين. تقلل هذه العملية من الأبخرة الضارة عن طريق إجراء التفاعل الطارد للحرارة تحت ظروف خاضعة للرقابة. بعد ذلك، يخضع المحلول للترشيح قبل التبخر لإنتاج بلورات كبريتات الصوديوم.
يتضمن تخليق كبريتات الصوديوم أيضًا الجمع بين حمض الكبريتيك وهيدروكسيد الصوديوم لتكوين كبريتات الصوديوم والماء. رد الفعل طارد للحرارة ويتطلب معالجة دقيقة لتجنب الفائض. بعد تصفية الخليط، يتم تعريض المحلول الناتج للتبخر لإنتاج بلورات كبريتات الصوديوم.
تتضمن الطريقة الأخرى تفاعل كربونات الصوديوم مع حمض الكبريتيك لإنتاج كبريتات الصوديوم والماء وثاني أكسيد الكربون. تتطلب هذه الطريقة استخدام غطاء الدخان بسبب إطلاق أبخرة سامة. ثم يتم ترشيح المحلول وتبخيره للحصول على بلورات كبريتات الصوديوم.
العمليات الصناعية الأخرى، مثل إنتاج الحرير الصناعي والمنظفات والزجاج، تنتج أيضًا كبريتات الصوديوم كمنتج ثانوي. تنتج هذه العمليات كبريتات الصوديوم كنفايات، والتي يمكن تنقيتها وإعادة استخدامها لأغراض أخرى.
استخدامات كبريتات الصوديوم
لكبريتات الصوديوم مجموعة واسعة من الاستخدامات في مختلف الصناعات، بما في ذلك:
- المنظفات: تستخدم كمادة حشو في مساحيق المنظفات، مما يساعد على زيادة الحجم وتحسين تدفق المنتج.
- الزجاج: يستخدم كصهيرة في صناعة الزجاج، مما يساعد على تقليل درجة الانصهار وتحسين وضوح المنتج النهائي.
- المنسوجات: تستخدم في إنتاج الألياف الاصطناعية، مثل الرايون، لتحسين قوة ومتانة المادة.
- الورق: يستخدم كعامل طحن في إنتاج الورق، مما يساعد على تحطيم ألياف الخشب وإزالة الشوائب.
- الغذاء: يستخدم كمضاف غذائي، في المقام الأول كمكثف ومستحلب في الأطعمة المصنعة.
- المستحضرات الصيدلانية: تُستخدم في إنتاج بعض الأدوية، مثل المُسهلات، للمساعدة في علاج الإمساك.
- المواد الكيميائية: تستخدم في إنتاج المواد الكيميائية المختلفة، بما في ذلك كبريتيد الصوديوم، وسيليكات الصوديوم، وبيكربونات الصوديوم.
- معالجة المياه: تستخدم في محطات معالجة المياه لإزالة أيونات الكالسيوم والمغنيسيوم من الماء العسر.
- التنقيب عن النفط: يستخدم في التنقيب عن النفط كعامل ترجيح، مما يساعد على التحكم في كثافة مائع الحفر.
أسئلة:
س: ما هي صيغة كبريتات الصوديوم؟
ج: الصيغة الكيميائية لكبريتات الصوديوم هي Na2SO4.
س: ما هي كبريتات الصوديوم؟
ج: كبريتات الصوديوم هي مادة صلبة بلورية بيضاء تستخدم عادة في مجموعة متنوعة من التطبيقات الصناعية، بما في ذلك المنظفات والزجاج والمنسوجات والورق والمواد الغذائية.
س: هل كبريتات الصوديوم حمضية أم قاعدية؟
ج: كبريتات الصوديوم ليست حمضية ولا قاعدية؛ إنه مركب محايد.
س: ما هو لون كبريتات الصوديوم؟ ج: كبريتات الصوديوم مادة صلبة بلورية بيضاء ولذلك فهي عديمة اللون.
