فوسفات الصوديوم ثنائي القاعدة أو Na2HPO4 هو مركب شائع الاستخدام كعامل عازل في المختبر. ويمكن العثور عليه أيضًا في بعض منتجات الأطعمة والمشروبات كمضافات غذائية.
| اسم الأيوباك | فوسفات هيدروجين الصوديوم |
| الصيغة الجزيئية | Na2HPO4 |
| CAS رقم | 7558-79-4 |
| المرادفات | فوسفات هيدروجين الصوديوم، فوسفات ثنائي الصوديوم، فوسفات الصوديوم ثنائي القاعدة، فوسفات الصوديوم ثنائي القاعدة لا مائي، فوسفات الصوديوم ثنائي القاعدة سباعي هيدرات |
| إنتشي | InChI=1S/2Na.H3O4P/c;;1-5(2,3)4/h;;(H3,1,2,3,4)/q2*+1;/p-2 |
Na2HPO4 الكتلة المولية
الكتلة المولية لفوسفات الصوديوم ثنائي القاعدة هي 141.96 جم / مول. يتم حساب هذه القيمة عن طريق جمع الكتل الذرية لكل عنصر من العناصر الموجودة في المركب وهي الصوديوم (Na) والفوسفور (P) والأكسجين (O). الكتلة المولية هي معلمة مهمة تستخدم في الحسابات المختلفة، على سبيل المثال لتحديد كمية المادة اللازمة لإجراء تفاعل أو لإعداد محلول بتركيز معين.
صيغة فوسفات الصوديوم
الصيغة الكيميائية لفوسفات الصوديوم ثنائي القاعدة هي Na2HPO4. تمثل هذه الصيغة نسبة كل عنصر من العناصر الموجودة في المركب. الصيغة مهمة في تحديد الخواص الكيميائية للمركب، مثل تفاعله وقابليته للذوبان.
نقطة غليان ثنائي القاعدة لفوسفات الصوديوم
ليس لدى فوسفات الصوديوم ثنائي القاعدة نقطة غليان محددة لأنه يتحلل قبل الوصول إلى نقطة الغليان. ومع ذلك، فإن درجة حرارة تحلل فوسفات الصوديوم ثنائي القاعدة ستكون حوالي 155 درجة مئوية. عند درجات حرارة أعلى من هذه القيمة، يبدأ المركب في التحلل إلى الأيونات المكونة له، الصوديوم والفوسفات. هذه الخاصية تجعلها غير مناسبة للاستخدام في التطبيقات التي تتطلب التسخين لدرجات حرارة عالية.
نقطة انصهار فوسفات الصوديوم ثنائي القاعدة
تختلف درجة انصهار Na2HPO4 حسب الشكل الذي يوجد به. يحتوي الشكل اللامائي للمركب على نقطة انصهار تبلغ 358 درجة مئوية، في حين أن الشكل السباعي الهيدرات له نقطة انصهار أقل تبلغ 93 درجة مئوية. نقطة الانصهار هي خاصية فيزيائية مهمة تستخدم لتحديد وتوصيف المواد.
الكثافة ثنائي القاعدة لفوسفات الصوديوم جم/مل
تعتمد كثافة Na2HPO4 على الشكل الذي يوجد به. تبلغ كثافة الشكل اللامائي للمركب 1.7 جم/مل، في حين أن كثافة شكل سباعي الهيدرات تبلغ 1.68 جم/مل. الكثافة هي خاصية فيزيائية تصف كمية الكتلة الموجودة في حجم معين من المادة.
الوزن الجزيئي ثنائي القاعدة لفوسفات الصوديوم
الوزن الجزيئي لـ Na2HPO4 هو 141.96 جم/مول. يتم حساب هذه القيمة عن طريق جمع الكتل الذرية لكل عنصر من العناصر الموجودة في المركب. الوزن الجزيئي هو عامل مهم يستخدم في الحسابات المختلفة، على سبيل المثال لتحديد كمية المادة اللازمة لإجراء تفاعل أو لتحضير محلول بتركيز معين.
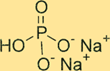
هيكل ثنائي القاعدة من فوسفات الصوديوم
يحتوي Na2HPO4 على بنية بلورية. الشكل اللامائي للمركب هو مسحوق أبيض عديم الرائحة، في حين أن شكل سباعي الهيدرات عبارة عن بلورة شفافة عديمة اللون. وللمركب شكل رباعي السطوح حول ذرة الفوسفور، وتقع كل ذرة أكسجين في زوايا رباعي السطوح. توجد أيونات الصوديوم في الفراغات الخلالية بين رباعيات الأسطح.
| مظهر | مسحوق أبيض أو بلورات شفافة |
| جاذبية معينة | 1.68 – 1.7 جم/مل |
| لون | عديم اللون إلى الأبيض |
| يشم | عديم الرائحة |
| الكتلة المولية | 141.96 جم/مول |
| كثافة | 1.68 – 1.7 جم/مل |
| نقطة الانصهار | لا مائي: 358 درجة مئوية، سباعي هيدرات: 93 درجة مئوية |
| نقطة الغليان | ينهار قبل الغليان |
| نقطة فلاش | غير قابل للتطبيق |
| الذوبان في الماء | قابل للذوبان للغاية |
| الذوبان | قابل للذوبان في الماء، غير قابل للذوبان في الإيثانول |
| ضغط البخار | غير قابل للتطبيق |
| كثافة بخار | غير قابل للتطبيق |
| PKa | 2.15 (أيون الفوسفات) |
| الرقم الهيدروجيني | 8.0 – 11.0 (0.1 م محلول مائي) |
السلامة ومخاطر فوسفات الصوديوم ثنائي القاعدة
يعتبر فوسفات الصوديوم ثنائي القاعدة (Na2HPO4) بشكل عام آمنًا للاستخدام في مجموعة متنوعة من التطبيقات، ولكنه قد يسبب تهيج الجلد والعين. استنشاق المركب في شكل مسحوق قد يسبب تهيج الجهاز التنفسي. يمكن أن يتفاعل Na2HPO4 بعنف مع الأحماض القوية والعوامل المؤكسدة، ويمكن أن يطلق أبخرة سامة عند تسخينه إلى درجات حرارة عالية. كما هو الحال مع جميع المواد الكيميائية، ينبغي اتخاذ الاحتياطات المناسبة عند التعامل مع هذا المركب، مثل ارتداء الملابس الواقية والقفازات والعمل في منطقة جيدة التهوية. في حالة ملامسته للجلد أو العينين، اشطفيه بكمية كبيرة من الماء واستشيري الطبيب إذا لزم الأمر.
| رموز الخطر | لا أحد |
| وصف الأمان | S22 – لا تتنفس الغبار، S24 – تجنب ملامسة الجلد، S37 – ارتد قفازات مناسبة |
| معرفات | UN3077 |
| رمز النظام المنسق | 28352200 |
| فئة الخطر | 9 |
| مجموعة التعبئة | ثالثا |
| تسمم | LD50 (الفئران، عن طريق الفم) – 3400 ملغم / كغم |
طرق تصنيع فوسفات الصوديوم ثنائي القاعدة
يمكن تصنيع فوسفات الصوديوم ثنائي القاعدة (Na2HPO4) بعدة طرق، بما في ذلك تفاعل حمض الفوسفوريك مع هيدروكسيد الصوديوم، ومعادلة حمض الفوسفوريك مع كربونات الصوديوم أو بيكربونات، وتفاعل فوسفات الصوديوم أحادي القاعدة مع هيدروكسيد الصوديوم.
- الطريقة الشائعة هي تفاعل حمض الفوسفوريك مع هيدروكسيد الصوديوم بنسبة 1:2 لإنتاج Na2HPO4 والماء. يمكن إجراء التفاعل عند درجة حرارة الغرفة أو تحت تسخين لطيف، ويتم تنقية المنتج الناتج عن طريق التبلور أو التبخر.
- هناك طريقة أخرى وهي معادلة حمض الفوسفوريك باستخدام كربونات الصوديوم أو بيكربونات، يليها ترسيب Na2HPO4. يتم ضبط الرقم الهيدروجيني لخليط التفاعل إلى حوالي 8-9 باستخدام كربونات الصوديوم أو بيكربونات، ويتم جمع الراسب الناتج وغسله بالماء لإزالة أي شوائب.
- تتضمن الطريقة الثالثة تفاعل فوسفات الصوديوم أحادي القاعدة مع هيدروكسيد الصوديوم بنسبة 1:1، مما يؤدي إلى تكوين Na2HPO4 والماء. ثم تتم تنقية المنتج الناتج عن طريق التبلور أو التبخر.
يعتمد اختيار الطريقة على عوامل مثل النقاء المطلوب والإنتاجية وفعالية التكلفة. يمكن إجراء تخليق Na2HPO4 بعدة طرق، ولكل منها مزاياها وقيودها.
استخدامات فوسفات الصوديوم ثنائي القاعدة
فوسفات الصوديوم ثنائي القاعدة له العديد من التطبيقات في الصناعات المختلفة.
- تستخدمه صناعة المواد الغذائية كمستحلب ومخزن وعامل سماكة. وهو يعمل كعازل، مما يساعد في الحفاظ على جودة الغذاء واستقراره عن طريق منع الأيونات المعدنية من التفاعل مع المكونات الغذائية الأخرى. وهو بمثابة عامل ترك في مسحوق الخبز وكمنظم لدرجة الحموضة في منتجات الألبان.
- تستخدمه الصناعة الطبية كملين لعلاج الإمساك عن طريق زيادة محتوى الماء في القولون. كما أنه يستخدم في تحضير الأدوية والحقن كمعدل ومنظم للأس الهيدروجيني.
- وفي الصناعة الزراعية، يعمل كسماد، حيث يوفر الفوسفور للنباتات.
- كما أنه يعمل كمكمل غذائي في علف الحيوانات.
- تستخدم صناعة معالجة المياه Na2HPO4 كمثبط للتآكل ومثبط للقياس في الغلايات وأنظمة التبريد.
- يعمل كعامل تنظيف، حيث يزيل رواسب الكالسيوم والمغنيسيوم من الأسطح.
أسئلة:
س: هل فوسفات الصوديوم ثنائي القاعدة مادة حافظة؟
ج: لا يُستخدم Na2HPO4 عمومًا كمادة حافظة في المنتجات الغذائية. ومع ذلك، يمكن أن يكون بمثابة عزل، مما يساعد في الحفاظ على جودة الغذاء واستقراره عن طريق منع الأيونات المعدنية من التفاعل مع المكونات الغذائية الأخرى.
س: ما عدد مولات فوسفات الصوديوم ثنائي القاعدة (mw 141.98) الموجودة في 50 مل من محلول 20% وزن/ حجم؟
ج: لحساب عدد المولات في محلول 20% وزن/حجم من Na2HPO4، نحتاج أولاً إلى تحويل نسبة الوزن/الحجم إلى جرام/100 مل. محلول 20٪ وزن / حجم يعني 20 جرامًا من المركب في 100 مل من المحلول. لذلك، 50 مل من المحلول يحتوي على 10 جرام من Na2HPO4. لحساب عدد المولات، قم بتقسيم الكتلة على الوزن الجزيئي:
الشامات = الكتلة / الوزن الجزيئي الشامات = 10 جم / 141.98 جم / مول الشامات = 0.070 مولات
لذلك، يوجد 0.070 مول من Na2HPO4 في 50 مل من محلول 20% وزن/حجم.
س: ما هي كثافة فوسفات الصوديوم ثنائي القاعدة؟
ج: تعتمد كثافة Na2HPO4 على شكل المركب وتركيزه. تبلغ كثافة الشكل اللامائي حوالي 2.36 جم/سم مكعب، بينما تبلغ كثافة شكل سباعي الهيدرات حوالي 1.62 جم/سم3. في الحل، سوف تختلف الكثافة تبعا للتركيز.
