سباعي أكسيد الكلور أو Cl2O7 هو مركب شديد الانفجار والتفاعل. يمكن أن يتحلل بعنف عند ملامسته للمواد العضوية وهو عامل مؤكسد قوي يستخدم في التركيب والتحليل الكيميائي.
| اسم الأيوباك | سباعي أكسيد الكلور |
| الصيغة الجزيئية | Cl2O7 |
| CAS رقم | 12015-53-1 |
| المرادفات | أنهيدريد البيركلوريك، سباعي أكسيد ثنائي الكلور، أكسيد الكلور (السابع)، أكسيد الكلور، بيركلوريل بيركلورات |
| إنتشي | InChI=1S/Cl2O7/c2-1(3,4,5,6)10-7(8,9)11-12-13-14-10 |
الكتلة المولية لسباعي أكسيد الكلور
سباعي أكسيد الكلور، صيغته الكيميائية Cl2O7، لديه كتلة مولية تبلغ 182.9 جم/مول. يتكون هذا المركب من ذرتي كلور وسبع ذرات أكسجين، مما يجعله عامل مؤكسد للغاية. يتم استخدام الكتلة المولية لسابع أكسيد الكلور لحساب كمية المادة في كتلة أو حجم معين من العينة باستخدام ثابت أفوجادرو.
نقطة غليان سباعي أكسيد الكلور
سباعي أكسيد الكلور هو مادة صلبة عديمة اللون إلى صفراء، شديدة التفاعل ومتطايرة. لم يتم تحديد نقطة غليان سباعي أكسيد الكلور بشكل جيد لأنه يتحلل قبل الوصول إلى نقطة الغليان. سباعي أكسيد الكلور هو عامل مؤكسد قوي يمكنه التفاعل مع المواد العضوية والماء والمواد الأخرى لتكوين مركبات متفجرة.
نقطة انصهار سباعي أكسيد الكلور
يحتوي سباعي أكسيد الكلور على نقطة انصهار تبلغ -96 درجة مئوية (-141 درجة فهرنهايت)، مما يجعله مادة صلبة منخفضة الانصهار. يمكن أن يوجد سباعي أكسيد الكلور كسائل مصفر في درجة حرارة الغرفة بسبب نقطة انصهاره المنخفضة وتفاعله العالي. من المهم التعامل مع سباعي أكسيد الكلور بحذر لأنه يمكن أن يسبب حروقًا شديدة وهو عامل مؤكسد قوي.
كثافة سباعي أكسيد الكلور جم/مل
تبلغ كثافة سباعي أكسيد الكلور 2.48 جم / مل عند درجة حرارة الغرفة. الكثافة العالية لسباعي أكسيد الكلور تجعله سائلًا كثيفًا يمكن أن يغوص بسرعة في قاع الحاوية. إن الكثافة العالية وتفاعلية سباعي أكسيد الكلور تجعل من الصعب التعامل معه ويتطلب احتياطات أمان خاصة عند استخدامه في التركيب الكيميائي أو التحليل.
الوزن الجزيئي لساباعي أكسيد الكلور
الوزن الجزيئي لسباعي أكسيد الكلور، المعروف أيضًا بالكتلة الجزيئية النسبية، هو 182.9 جم/مول. يعد الوزن الجزيئي لسباعي أكسيد الكلور مهمًا في الحسابات الكيميائية التي تتضمن كمية المادة والكتلة والحجم. إن الوزن الجزيئي العالي لسابع أكسيد الكلور يجعله مركبًا كثيفًا ومتطايرًا يتطلب معالجة وتخزينًا دقيقًا.
هيكل سباعي أكسيد الكلور
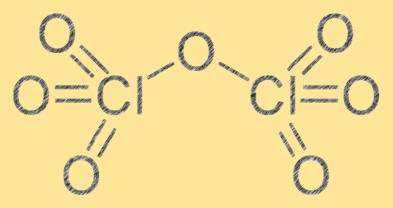
يتكون هيكل سباعي أكسيد الكلور من ذرتين كلور وسبع ذرات أكسجين. له صيغة جزيئية من Cl2O7 وهندسته الجزيئية عبارة عن شكل ثماني السطوح مشوه بسبب التنافر بين ذرات الأكسجين. يعتبر سباعي أكسيد الكلور عامل مؤكسد قوي ويمكن أن يتفاعل مع العديد من المواد العضوية وغير العضوية. يعد هيكل سباعي أكسيد الكلور ضروريًا لفهم خواصه الكيميائية وسلوكه في التفاعلات المختلفة.
صيغة سباعي أكسيد الكلور
الصيغة الكيميائية لسباعي أكسيد الكلور هي Cl2O7. تشير الصيغة إلى أن كل جزيء من سباعي أكسيد الكلور يحتوي على ذرتين كلور وسبع ذرات أكسجين. تُستخدم الصيغة لحساب قياس العناصر الكيميائية للتفاعلات الكيميائية التي تتضمن سباعي أكسيد الكلور. تعتبر صيغة سباعي أكسيد الكلور مهمة أيضًا في تحديد وزنه الجزيئي وكثافته وخواصه الفيزيائية والكيميائية الأخرى.
| مظهر | عديم اللون إلى مصفر الصلبة |
| جاذبية معينة | 2.48 عند 25 درجة مئوية |
| لون | عديم اللون إلى مصفر |
| يشم | حار، حامض |
| الكتلة المولية | 182.9 جرام/مول |
| كثافة | 2.48 جم/مل عند 25 درجة مئوية |
| نقطة الانصهار | -96 درجة مئوية (-141 درجة فهرنهايت) |
| نقطة الغليان | يتحلل قبل نقطة الغليان |
| نقطة فلاش | غير قابل للتطبيق |
| الذوبان في الماء | يتفاعل بعنف مع الماء |
| الذوبان | قابل للذوبان في المذيبات العضوية |
| ضغط البخار | غير متاح |
| كثافة بخار | غير متاح |
| pKa | غير متاح |
| الرقم الهيدروجيني | غير قابل للتطبيق |
السلامة ومخاطر سباعي أكسيد الكلور
يعد سباعي أكسيد الكلور مركبًا شديد التفاعل وخطير ويشكل مخاطر كبيرة على السلامة إذا لم يتم التعامل معه بشكل صحيح. يمكن أن يسبب حروقًا شديدة وأضرارًا للعينين والجلد والجهاز التنفسي عند ملامسته. يمكن أن يتفاعل سباعي أكسيد الكلور أيضًا بعنف مع الماء والمواد العضوية، مما يتسبب في حدوث انفجارات ومخاطر الحرائق. ومن الضروري استخدام معدات الحماية الشخصية المناسبة، بما في ذلك القفازات والنظارات الواقية وأجهزة التنفس عند التعامل مع سباعي أكسيد الكلور. يجب تخزين المركب ونقله في حاوية آمنة مغلقة بإحكام، بعيداً عن مصادر الاشتعال أو الحرارة أو الرطوبة. وينبغي اتباع إجراءات المناولة المناسبة واحتياطات السلامة لتقليل المخاطر المرتبطة بسباعي أكسيد الكلور.
| رموز الخطر | عامل مؤكسد، مسبب للتآكل |
| وصف الأمان | تجنب ملامسة الماء والأحماض والمواد العضوية وعوامل الاختزال. استخدم معدات الحماية الشخصية المناسبة. يخزن في حاوية مغلقة بإحكام بعيدا عن الحرارة والرطوبة ومصادر الاشتعال. في حالة ملامسة العينين أو الجلد أو الجهاز التنفسي، اطلب العناية الطبية على الفور. |
| أرقام تعريف الأمم المتحدة | الأمم المتحدة 3083 |
| رمز النظام المنسق | 28299090 |
| فئة الخطر | 5.1 (المواد المؤكسدة) |
| مجموعة التعبئة | ثانيا |
| تسمم | شديد السمية عن طريق الاستنشاق أو الابتلاع أو امتصاص الجلد. يسبب حروقا شديدة وتلف الأنسجة. قد يسبب انفجارات ومخاطر الحريق عند ملامسة الماء والمواد العضوية والمواد التفاعلية الأخرى. |
طرق تصنيع سباعي أكسيد الكلور
سباعي أكسيد الكلور مركب شديد التفاعل ويصعب تصنيعه.
إحدى الطرق الأكثر شيوعًا لتصنيع سباعي أكسيد الكلور هي تفاعل غاز الكلور والأوزون. هذا التفاعل طارد للحرارة ويمكن أن يؤدي إلى تفاعل متفجر إذا لم يتم التحكم فيه بعناية.
تتضمن الطريقة الأخرى تفاعل غاز الكلور مع كلورات البوتاسيوم، مما ينتج عنه سباعي أكسيد الكلور وكلوريد البوتاسيوم كمنتجات ثانوية. تتطلب هذه الطريقة أيضًا مراقبة دقيقة لظروف التفاعل لمنع تكوين مواد وسيطة متفجرة.
يمكن تصنيع سباعي أكسيد الكلور عن طريق تفاعل غاز الكلور مع خامس أكسيد ثنائي الكلور، الذي ينتج سباعي أكسيد الكلور وسادس أكسيد ثنائي الكلور كمنتجات ثانوية. ومع ذلك، لا يستخدم الباحثون هذه الطريقة عادة بسبب الطبيعة الخطرة لخامس أكسيد ثنائي الكلور.
تشمل الطرق الأخرى لتصنيع سباعي أكسيد الكلور تفاعل غاز الكلور مع مركبات عضوية مختلفة، مثل البنزين أو التولوين، تحت ظروف خاضعة للرقابة. ومع ذلك، تتطلب هذه الطرق تحسينًا دقيقًا لظروف التفاعل وليست موثوقة أو شائعة الاستخدام مثل طرق الكلور والأوزون أو كلورات الكلور والبوتاسيوم.
بشكل عام، يتطلب تصنيع سباعي أكسيد الكلور مراقبة دقيقة لظروف التفاعل ويمثل مخاطر كبيرة على السلامة بسبب الطبيعة شديدة التفاعل للمركب. يجب اتباع احتياطات السلامة وإجراءات التعامل الصحيحة عند العمل مع سباعي أكسيد الكلور أو أي مواد خطرة أخرى.
استخدامات سباعي أكسيد الكلور
- يجد Cl2O7 استخدامه الرئيسي كعامل مؤكسد في التخليق الكيميائي والأبحاث.
- وهو يعمل كمؤكسد قوي، حيث يتفاعل مع مجموعة واسعة من المركبات العضوية وغير العضوية، مما يجعله مفيداً في العديد من التفاعلات الكيميائية.
- أحد الاستخدامات الأكثر شيوعًا لـ Cl2O7 هو إنتاج ثاني أكسيد الكلور، وهو مطهر قوي وعامل تبييض يستخدم في معالجة المياه، وإنتاج اللب والورق، وتصنيع المنسوجات.
- كما أنه يستخدم كعامل مؤكسد قوي في تركيب العديد من المركبات العضوية، بما في ذلك الأدوية والكيماويات الزراعية.
- يستخدم Cl2O7 في الأوساط الأكاديمية والبحثية لدراسة تفاعل المركبات العضوية وغير العضوية المختلفة. كما أنه بمثابة عامل مساعد في تركيب بعض المركبات، مثل راتنجات الايبوكسي وأنهيدريد الخل.
- ونظرًا لطبيعته الخطرة، فإن التطبيقات الصناعية واسعة النطاق عمومًا لا تستخدم Cl2O7. يتطلب التعامل والتخزين الدقيق لتجنب تكوين مواد متفجرة ومخاطر أخرى على السلامة.
بشكل عام، يعد Cl2O7 مركبًا مفيدًا في التركيب الكيميائي والأبحاث، ولكنه يتطلب احتياطات السلامة وإجراءات المعالجة المناسبة لتقليل المخاطر المرتبطة باستخدامه.
أسئلة:
س: ما هو Cl2O7؟
ج: Cl2O7 مركب كيميائي يتكون من ذرتين كلور وسبع ذرات أكسجين، صيغته الكيميائية Cl2O7.
س: ما هو الاسم الصحيح لـ Cl2O7؟
ج: الاسم الصحيح لـ Cl2O7 هو ثنائي الكلور سباعي أكسيد.
س: هل Cl2O7 أيوني أم تساهمي؟
ج: Cl2O7 مركب تساهمي. ويتكون من عنصرين غير معدنيين، الكلور والأكسجين، ويشكل مركبا جزيئيا من خلال تبادل الإلكترونات بين الذرات.
س: ما هو الأكسيد أدناه الذي يتفاعل مع الماء لتكوين حمض ضعيف؟ أهداب الشوق، Cl2O7، P4O10، Bi2O3، N2O5.
ج: الأكسيد الذي يتفاعل مع الماء لتكوين حمض ضعيف هو N2O5. عندما يتفاعل N2O5 مع الماء، فإنه يشكل حمض النيتريك، وهو حمض ضعيف. الأكاسيد الأخرى المذكورة، MgO، P4O10، Bi2O3 وCl2O7، لا تتفاعل مع الماء لتكوين أحماض ضعيفة.
